癌症疫苗,又一新抗癌疫苗研发成功,肿瘤疫苗90%应答率
最近,在美国爆发的麻疹突显了疫苗接种在预防传染病中的重要性。然而,疫苗在癌症的预防和治疗中也起着重要的作用。FDA认可乙肝病毒(HBV)和人乳头瘤病毒(HPV)疫苗均可以预防癌症。
同时,科学家也在致力于研究治疗性疫苗,用于已经确诊为癌症的患者。目前,TICE BCG、sipuleucel-T(Provenge)和talimogene laherparepvec(T-VEC)是仅有的FDA批准的三种治疗性癌症疫苗。而在研的疫苗就非常多了,也与很多已经取得了非常好的数据。
全新个性化癌症疫苗研发成功,90%患者产生应答
Treos Bio公司开发了一种独特的方法来制造癌症疫苗,不仅着眼于疫苗靶标,更着眼于为每个患者免疫系统提供可以特异性应答的抗原靶标。也就是说,要针对个体差异,制备个性化的抗癌疫苗,因为肿瘤治疗需要个性化。
该公司研发成功一种与竞品相比领先的产品平台,即个人抗原选择计算器(PASCal),可解决患者个体差异和肿瘤的异质性。PASCal还支持开发通用性疫苗,基于共享抗原的共同癌症疫苗家族,在共同疫苗家族的基础上开发个性化抗癌疫苗是未来主要的发展方向,这些疫苗能针对19种癌症适应症,无需进行肿瘤活检。
其中一种制备成功的疫苗PolyPEPI1018已经获得了很好的治疗效果,数据在癌症免疫治疗学会第34届年会(SITC 2019)上发表,PolyPEPI1018现成疫苗作为维持疗法的补充,可在微卫星稳定(MSS)转移性结直肠癌患者( mCRC)中获得持久的治疗反应。
PolyPEPI1018是一种针对结直肠癌患者的现成的多肽疫苗,其中包含12种免疫原性表位,这些表位基于对2931次活检组织的分析而得自7种在mCRC中经常表达的保守癌抗原。
PolyPEPI1018疫苗作为MSS,mCRC患者维持治疗的I期研究结果
在一线治疗阶段,用氟嘧啶和靶向药物(贝伐单抗)进行维持治疗后,11例MSS 转移性结直肠癌患者接受了PolyPEPI1018疫苗接种。(A部分:n = 5例,单剂,随访12周;B部分:n = 6例,3剂,Q12W)。
主要终点是安全性和免疫原性。对血液和肿瘤中疫苗诱导的免疫反应进行了多次分析。使用从患者唾液样本中确定的自体HLA基因型,可以预测免疫反应和临床获益。
疫苗安全性
PolyPEPI1018疫苗耐受性良好。
最常见的副作用是短暂的皮肤反应和流感样综合征。
疫苗有效性
90%的患者对7种疫苗抗原中的至少2种具有记忆效应类型的疫苗特异性CD8 + T细胞应答,平均5种疫苗能够引起该应答。
在所有患者中均检测到疫苗特异性CD4 + T细胞反应。接种后,在71%的患者中检测到了效应子类型的离体CD8 + T细胞反应,并且在患者的外周血中检测到了多功能、循环中的CD8 +和CD4 + T细胞的比例增加。
在这11例患者中,有3例根据RECIST v1.1具有客观的肿瘤反应,其中1例接受单剂疫苗治疗,2例接受3剂疫苗治疗。对于研究的另一部分数据,客观缓解率(ORR)为33%(2/6),疾病控制率(DCR)为67%(4/6)。
值得注意的是,在治疗25周后,一名患者的3个靶病变中有2个发生了肿瘤完全萎缩,1个病变中出现了部分应答,符合根治手术的条件。疾病控制的中位时间为9个月(研究期间未达到mPFS),10个月的无进展生存率为50%(3/6)。
小结
体外研究证实了疫苗诱导抗原特异性CD8 + T细胞反应,预测的多抗原免疫反应往往与无进展生存期和肿瘤体积减少相关。
PolyPEPI1018疫苗治疗和维持治疗安全,耐受性良好,并证明了在MSS mCRC肿瘤具有免疫和临床活性,能够有效延缓癌症的进展。
什么是癌症疫苗
近年来,癌症疫苗已经成为免疫疗法的一种形式,通过刺激或恢复人体自身的免疫系统,来防止癌症发展或杀灭现有的肿瘤。
癌细胞表面存在特殊的蛋白质,通过靶向这些蛋白质,免疫系统可以特异性地消除癌细胞,同时不伤害正常的细胞。
癌症疫苗属于生物反应调节剂的一类物质,其原理是通过刺激免疫系统中的树状细胞,使其在细胞表面显现出肿瘤抗原,进而诱导出毒杀性 T 淋巴细胞,达到癌细胞清除效果,同时也会间接刺激辅助型 T 细胞分泌细胞激素,强化毒杀型 T 淋巴细胞对癌细胞的攻击力。
可选择的治疗性疫苗有哪些
打一针,就赶跑癌细胞的梦想已临近!已经问世的癌症疫苗有:
前列腺癌疫苗
树突细胞疫苗
融合细胞疫苗
肺癌疫苗
第一款治疗性疫苗问世
2010年,治疗性疫苗Provenge(sipuleucel-T)获批,这是全球首个也是目前唯一一个获得美国FDA批准的癌症疫苗,也是DC疫苗,治疗转移性前列腺癌,临床研究发现,该药物延长患者平均生存时间为至少4个月,这开创了癌症免疫治疗的新时代。
免疫系统总指挥-树突细胞疫苗
有一种对于人体的免疫系统起着至关重要作用的免疫细胞,即树突状细胞(Dendritic Cell,又称DC细胞),占总体免疫细胞的1%。DC细胞是人体内功能最强的抗原递呈细胞,如果免疫系统中,没有DC细胞携带抗原的T细胞,免疫细胞无法自行找到侵袭人体的异物(病毒、细菌、癌细胞),人体的免疫功能将大打折扣。
树突细胞与诺贝尔奖渊源
2011年,三位科学家被授予诺贝尔生理学或医学奖,以表彰其发现DC细胞并进行适应性免疫研究做出的卓越贡献。斯坦曼被诊断为晚期胰腺癌后,他用自己研发的DC细胞进行治疗,将原本只有数月的生命延长到四年半时间。

新型抗肿瘤疫苗——树突疫苗
人体的免疫系统中本来就有这种树突状细胞,但数量和活力都不够围歼癌变细胞的程度。有潜力成为树突状细胞的前体细胞可以通过一个特定的方法从血液中分离出来。借助于某种特定的信使,在试管中分离出来的细胞可以获得免疫能力。当前体细胞成熟为树突状细胞时,他们即可捕获特定的蛋白质(例如肿瘤抗原)。
由于树突状细胞抗肿瘤特性与疫苗原理一致,因此树突细胞疗法在临床中更多的被称为树突细胞疫苗。
树突疫苗已被国际广泛认可
美国FDA批准首个抗癌疫苗Provenge(sipuleucel-T)就是DC疫苗,治疗转移性前列腺癌;日本厚生劳动省官方宣布将 DC 免疫疗法列入 A 级先进医疗技术,并已用于上万例晚期癌症病症的临床治疗;德国政府认可的 DC 细胞制备实验室,运用 DC 免疫疗法已累积治疗数千名患者。
目前,获得批准的树突细胞疫苗有两种,分别是德国LANEX-DC和日本WT1肽抗原树突细胞疫苗。
1.德国LANEX-DC
适应症:实体肿瘤
上市时间:已上市
德国国家级,目前唯一一所持有德国政府颁发的DC细胞制备资质的实验室LDG研发的LANEX-DC是一种利用肿瘤抗原对患者自体树突(DC)细胞进行特异性免疫刺激培养,以DC细胞为基础的肿瘤疫苗技术。
通过采集患者血液,分离、筛选出高纯度DC细胞,混合了细胞因子GM-CSF、肿瘤特异性抗原(PAP)等物质进行培育,使DC细胞活化,再回输患者,激活患者体内的T淋巴细胞,从而产生针对大量表达PAP的肿瘤细胞的特异性免疫杀伤效应,消灭癌细胞!临床已证实对人类已知的恶性肿瘤,如肺癌、肝癌、肾癌、乳腺癌、皮肤癌等多种肿瘤有效。
这种树突细胞免疫治疗方案在其他国家不是没有,但是收效甚微,目前在国内的顶级医科大学研发的产品其活性因子的生存期只有21天,也就意味着21天内就要进行下一个疗程。而LANEX-DC治疗法采用高度提纯的树突细胞,一个疗程可以维持6个月,更重要的是他们把病患的复发率从50%降低到7%。同时细胞活性因子从培养室到植入患者体内,之间的存活时间可以持续8个小时,目前国内医科大学制备后基本存活时间就在20分钟之内。 技术上存在巨大差距。
一位49岁的男性在2012年诊断为多形性成胶质細胞瘤 WHO Ⅳ級 ,并进行手术治疗。2014年复发后采用LANEX-DC治疗,2017年病情完全缓解。更多案例大家可以登录全球肿瘤医生网医学部了解治疗详情。

2.日本WT1肽抗原树突细胞疫苗
适应症:实体肿瘤
上市时间:已上市(日本厚生劳动省再生医疗法批准)
树突细胞是已知体内功能最强、惟一能活化静息T细胞的专职抗原提呈细胞,相当于是免疫系统的司令部,它能够识别癌细胞,并将癌细胞的抗原呈递给T淋巴细胞,使数量庞大的淋巴细胞能够识别癌细胞,命令更多的淋巴细胞去攻击带有相应抗原的癌细胞。
而树状细胞如何更有效地把癌细胞的标记传授给T淋巴细胞,对癌细胞进行有效攻击,最重要的一点就是使用什么癌抗原刺激树突细胞。人们研究了很多癌抗原,其中由日本的大阪大学开发的“ WT1肽”已在75种癌症抗原中的9个项目中进行了评估,被美国专业学会杂志CLIN CANCER RES评为最优秀的专利技术,排名第一的 癌症抗原。
WT1基因在白血病及各种实体瘤包括:肺癌、胃癌、肝癌、乳腺癌中高表达,在这些肿瘤中起特异性癌基因作用,因此WT1肽是一个新的超表达的肿瘤特异性抗原。
日本东京大学医科学研究所结合“WT1肽抗原”研发新一代树突细胞疫苗技术,与许多我们所知的树突状细胞疗法完全不同。特别根据患者的“HLA(人类白细胞抗原)”类型的检测结果,将最适合患者的WT1肽掺入从患者血液培养的树突状细胞中,制备与患者的HLA相容,最有效的疫苗。
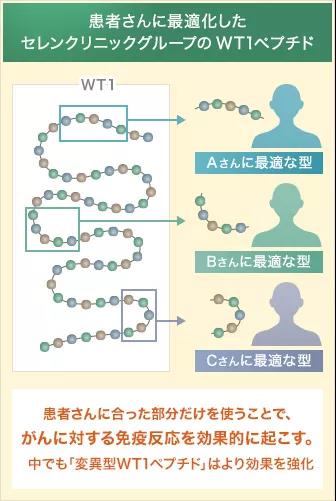
由于这种人造癌症抗原是一项专利技术,因此只能在有限的指定医疗机构中进行治疗。
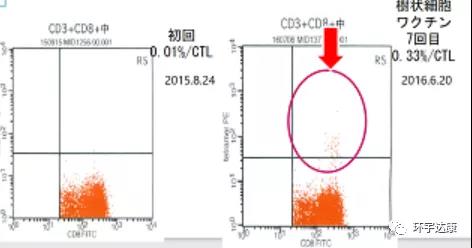
一位晚期肠癌肝转移的患者,选择化疗联合WT1树突细胞疫苗治疗,体内的CTL(细胞毒性T细胞)含量治疗前为0.01%,而在进行7次树突细胞治疗后,体内的CTL的含量竟然达到0.33%!2016年11月,CT扫描结果显示病灶全部消失了,病理检测结果也证实了患者达到了完全缓解状态。
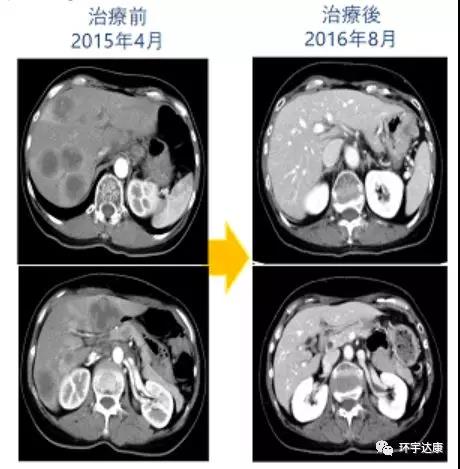
因此,DC疫苗已经被国际医学抗肿瘤领域广泛认可,并已经应用于临床治疗,这是癌症患者治疗的新希望,也是无进展生存癌症的新方法。
融合细胞疫苗适用实体瘤
融合细胞疫苗是一种针对所有实体瘤的治疗性疫苗。
我们知道细胞毒性T细胞(CTL) 负责攻击癌细胞,而树突状细胞(DC)负责递呈给CTL癌细胞的抗原信息。融合细胞疫苗是对目前的DC-CTL疗法进行改良,现在可以使癌细胞携带的多种癌抗原成为免疫系统的攻击目标,特异性更强。经过改良的融合细胞疗法就是能够让全部的肿瘤细胞抗原全部送到CTL面前,技术原理是这样的。
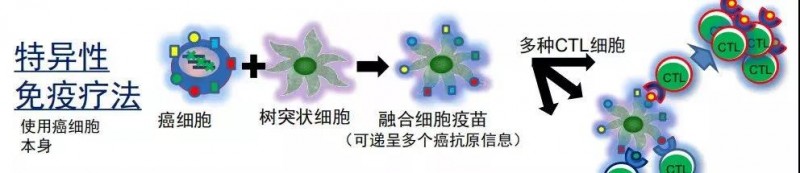
改良前的的DC-CTL疗法是在体外提取癌细胞的抗原(不是全部的癌抗原,仅为一些常规的抗原),再用抗原刺激体外诱导的DC细胞,使其携带抗原信息,去递呈给CTL细胞,让其具有识别癌细胞的能力,进而杀伤癌细胞。但是,DC细胞细胞获取的抗原信息比较有限,会使得一部分癌细胞无法被识别出来。
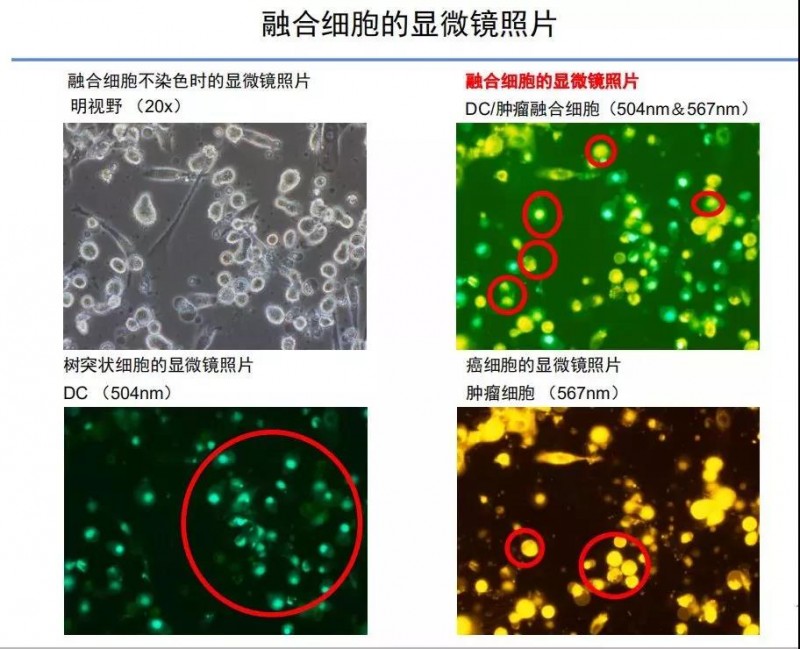
而改良后的融合细胞技术,是将整个癌细胞与DC细胞进行融合,形成的融合细胞具有癌细胞的抗原性,又具有DC细胞的递呈功能。所以,融合后的细胞可以携带着全部种类癌抗原找到CTL细胞,“告知癌细胞就是长这样的,”使其具有癌细胞的识别与杀伤能力。
古巴肺癌疫苗
肺癌疫苗的想法听起来很荒谬。毕竟,肺癌不是流感。但是,古巴研究人员25年的研究,使这种治疗型肺癌疫苗现在已经成为现实!早期的试验表明,这种治疗方法可以帮助60岁以下的晚期肺癌患者平均比未接种疫苗的患者长11个月!
非小细胞肺癌疫苗CIMAvax在古巴和其他国家已经进行了大量的临床试验,但美国的试验目的是要疫苗联合PD-1是否更有效,能否加速免疫系统的反应,这是第一次尝试进行联合治疗。
2018年1月,美国第一组经过初始化疗的晚期肺癌患者开始进行CIMAvax疫苗联合PD-1(Opdivo,纳武单抗)治疗。研究人员Pedro Camilo Rodríguez说,这是一种非常创新的方法,对我们来说,疫苗是一项突破性的成就。
全球首个注册用于晚期非小细胞肺癌的疫苗--CimaVax
近日,罗斯威尔公园综合癌症中心胸部肿瘤科主任,首席研究员Grace Dy医学博士宣布根据第1阶段/第2阶段试验的第一部分的积极结果,肺癌疫苗CIMAvax-EGF进入第二阶段临床试验,将研究这种组合方法作为晚期肺癌患者维持治疗的生存益处。
但是注意,CimaVax EGF不能阻止癌症的发展,更不能无进展生存癌症,而是启动了一种机制,通过这种机制,癌细胞的失控生长和分裂更加受到限制,从而将晚期侵袭性肺癌转变为慢性疾病。目前,古巴肺癌疫苗已经在全球80多个国家获批,国内患者也可以申请从海外购买该疫苗()。
目前,癌症的治疗方法主要包括手术、放疗和化疗及近年来兴起的靶向治疗和免疫治疗,而癌症疫苗是未来癌症研究的重要方向,这是一种从免疫系统上清除癌症的机制,从根本上消灭肿瘤,我们拭目以待。







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城