2020年美国癌症研究协会第111届年会(AACR-2020年)肿瘤癌症消息进展,新疗法,抗癌新药
2020年AACR会议精彩报道
2020年4月27~29日,世界上规模最大的癌症研究会议之一,美国癌症研究协会第111届年会(AACR 2020年)由于新型冠状病毒疫情的影响,采用线上虚拟会议的形式召开。这场国际盛会可谓是饕餮盛宴,会议上国内外研究学者齐聚一堂,分享着各自领域的研究成果,其中不乏惊艳的亮眼数据。尤其是肺癌靶向及免疫治疗,此外其他癌种,如乳腺癌、肾癌、实体瘤等领域也有研究结果展示。那么接下来就跟着小编一起感受抗癌前沿的精彩“脉动”吧!

肺癌篇
ORR达54%,卡马替尼治疗MET 14突变脑转移疗效不俗
Capmatinib (卡马替尼,又名INC280)是一种口服的高选择性小分子MET抑制剂,目前已经获得FDA授予的优先审评资格。在II期临床试验GEOMETRY mono-1中,纳入的97例MET 14 跳跃突变或MET扩增的晚期NSCLC患者,接受卡马替尼进行治疗。
【研究结果】
(1)在初治患者(28例,先前没有接受过治疗)中,独立评审委员会(BIRC)评估的客观缓解率(ORR)为67.9%,疾病控制率(DCR)为96.4%。研究者评估的ORR为60.7%,DCR为96.4%。
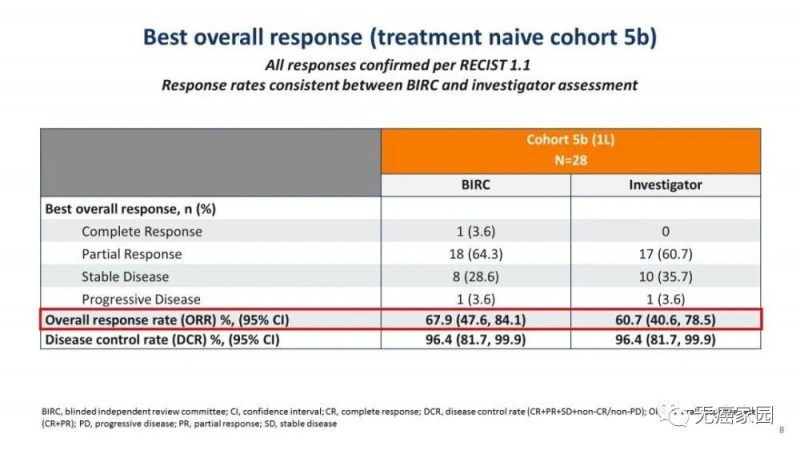
(2)在经治患者(69例,先前已接受过治疗,88.4%含铂化疗)中,BIRC评估的ORR为40.6%,DCR为78.3%。研究者评估的ORR为42.0%,DCR为76.8%。
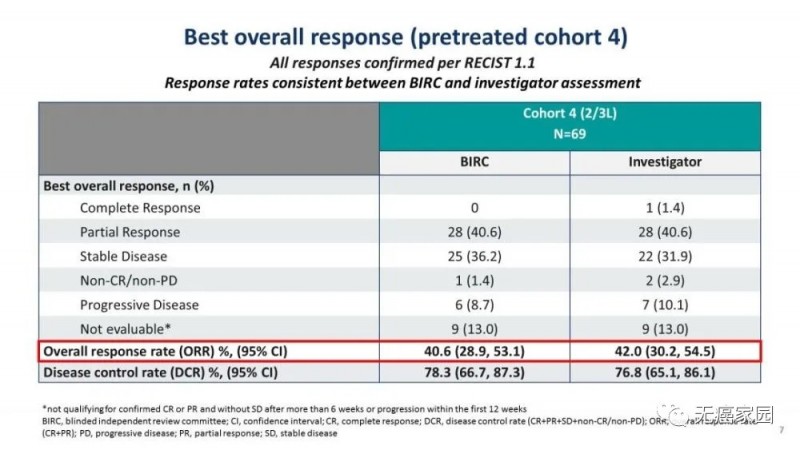
(3)在初治患者中,中位缓解持续时间(DOR)为11.14个月,中位无进展生存期(PFS)为9.69个月。在经治患者中,DOR为9.72个月,PFS为5.42个月。
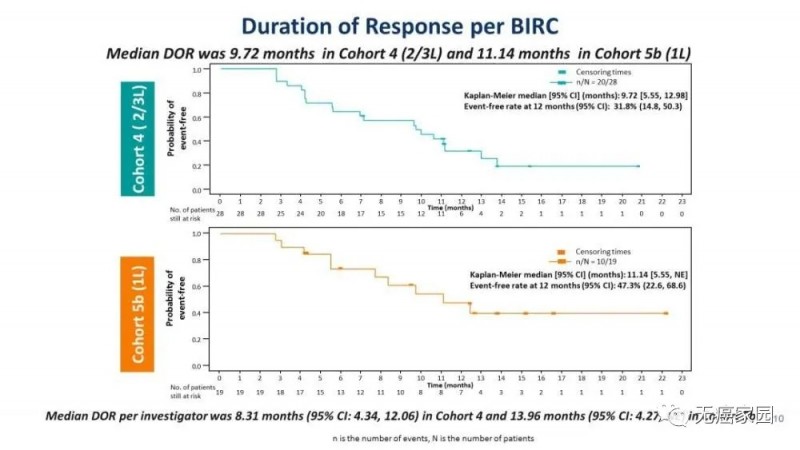
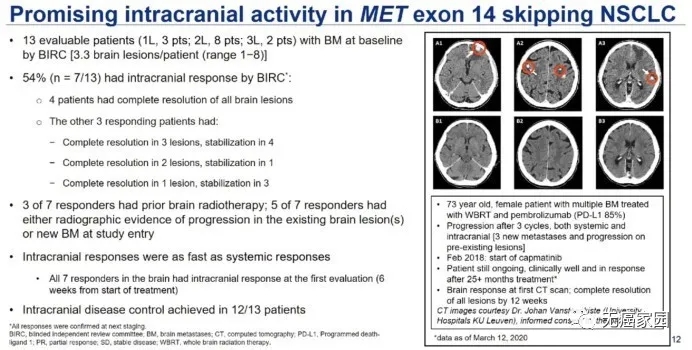
(4)在13例出现脑转移的MET 14突变患者中,约有一半的脑转移患者对卡马替尼应答,颅内ORR达到54%(7/13)。
在这些患者中,有4例完全消除了脑部病变(31%),另外3例部分缓解(PR)患者的情况:1例患者3个病灶完全缓解,4个病灶稳定;1例患者2个病灶完全缓解,1个稳定;1例患者1个病灶完全缓解,3个稳定。所有患者颅内DCR为92.3%(12/13)。
【真实案例】
大会上报道的一个真实案例,1例73岁女性患者患有多处脑转移,既往接受K药和全脑放疗,2018年2月开始接受卡马替尼后首次CT显示达到多病灶完全缓解,目前已经持续了25个月以上的治疗。
截止到目前,MET突变的肺癌仍没有正式获批的靶向药,而卡马替尼是最有希望给患者带来获益的靶向药。卡马替尼一线及后线治疗MET异常的NSCLC患者的疗效不俗,初步数据还显示出其入脑能力喜人。
专家在研究中也指出,建议患者早期治疗时应进行的基因检测,再选择对症的治疗方案。
相关文章:全球首个MET抑制剂,MET基因突变靶向药Capmatinib(卡马替尼治、INC280)获得优先审批资格
TIL疗法小试牛刀,挑战PD-1耐药性非小细胞肺癌
在过继性细胞免疫治疗领域,除了CAR-T细胞疗法,实体肿瘤中最具潜力的当属TILS(肿瘤浸润淋巴细胞)疗法。去年的ASCO会议上,基于TILS细胞的创新型疗法LN-145和LN-144(Lifileucel)在治疗宫颈癌和黑色素瘤的临床结果引起了医学界的广泛关注。
在今年AACR会议上,一项由美国癌症中心莫菲特癌症研究中心(H. Lee Moffitt )开展的基于TIL细胞治疗的Ⅰ期临床结果公布:在12名可评估的非小细胞肺癌患者中,TIL疗法可达到25%的总缓解率,其中两名患者达到持久的完全缓解。值得一提的是,这些患者既往均接受过PD-1抗体(Opdivo)治疗且病情发生进展。
当从这些患者体内的肿瘤病灶中提取出抗癌能力超强的TILs细胞,并在体外扩增培养成数十亿有着精准杀伤能力的免疫大军,回输到体内作战时,大部分患者在首次TIL治疗后进行 CT扫描就开始出现明显的肿瘤消退。
这项试验共有32名患者参加,最终有16名患者接受TILS治疗,其中12名患者可以评估。在平均随访1.4年时,3名患者病情缓解,其中两名完全患者,并且已超过一年。另一名患者的缓解即将得到确认。
大部分患者在接受TILs治疗后,肿瘤病灶都有所缩小,在接受治疗后的第一次CT扫描时,肿瘤病灶直径平均缩小38%!
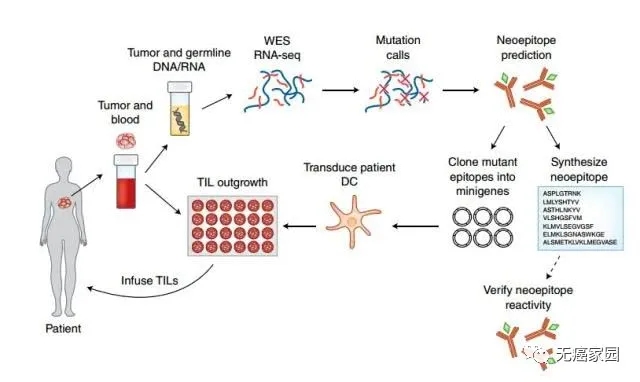
图为TILs新疗法独特的制备方式
因此,在PD-1治疗后,TILs疗法仍具有令晚期转移性非小细胞肺癌达到持久缓解的能力,这是非常了不起的,期待这款疗法能加大研究,早日获批上市,为晚期患者的生命持续续航!
相关文章:胆管癌肿瘤浸润淋巴细胞TILs疗法,TIL治疗完成生存期大逆转
DCR达93.4%,阿美替尼开启晚期肺癌长生存之路
阿美替尼是首个国产上市并研发的第三代EGFR肺癌靶向药,也是全球首个二线治疗中位无进展生存期(PFS)超一年的第三代EGFR肺癌靶向药。
通常在使用第一代或第二代EGFR TKI治疗后,约有50%的NSCLC患者会产生耐药性T790M突变。因此,本次会议报道了阿美替尼临床试验APOLLO Ⅱ期研究的数据更新。该试验共纳入244例患者,其中88例患者在基线合并有中枢神经系统(CNS)转移,23例患者至少有1个可评估的颅内靶病灶。
截止到2019年8月1日,其结果显示,总人数的客观缓解率(ORR)为68.9%,疾病控制率(DCR)高达93.4%,中位无进展生存期(PFS)为12.3个月,中位缓解持续时间(DOR)为12.4个月。
对于基线有CNS转移的患者,确认的CNS ORR和DCR分别为60.9%和91.3%。CNS中位PFS为10.8个月,中位DOR为11.3个月。
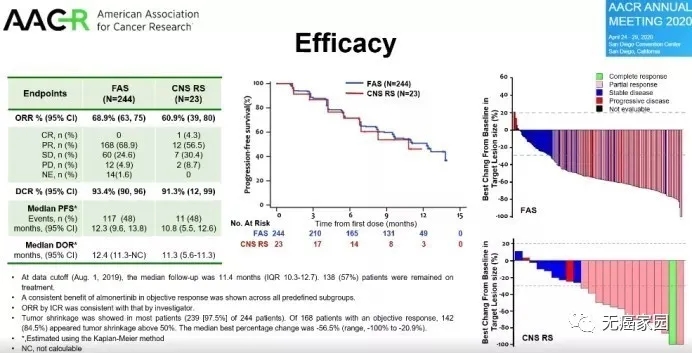
安全性方面,与先前报告的一致。总人群的3级及以上药物相关不良反应发生率为15.6%,药物相关严重AE发生率为5.3%。
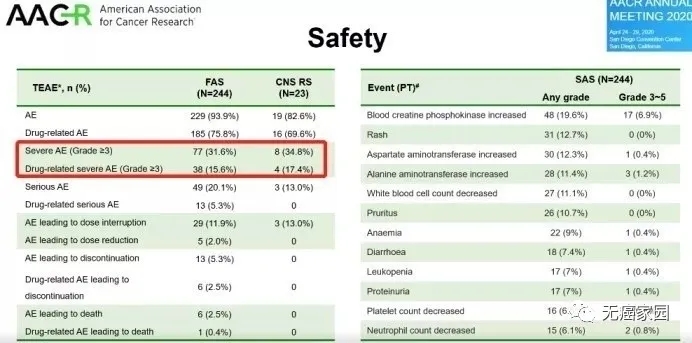
随着随访时间的延长,阿美替尼在先前接受EGFR TKI治疗后进展的EGFR T790M阳性NSCLC患者中显示出无进展生存的获益,尤其是对CNS转移患者具有良好的临床疗效。
DCR达94.4%,伯瑞替尼治疗MET异常NSCLC前景广阔
伯瑞替尼(PLB-1001,CBT-101)是一种有效的高选择性c-MET抑制剂,在体外和体内NSCLC模型中均显示出优异的活性。
在本次大会上报道了伯瑞替尼治疗c-Met 异常的晚期非小细胞肺癌的I期临床试验结果,研究共纳入37例经治但未接受c-Met抑制剂或HGF靶向治疗的局部晚期或转移性晚期NSCLC患者。研究分为剂量递增(19例)和剂量扩展(18例)两个阶段进行。
研究结果显示,8例患者仅检出c-MET过表达,11例仅携带Ex14跳跃突变,8例仅检出MET基因扩增,另外10例患者检出不止一种MET变异。伯瑞替尼总体耐受性良好,未出现剂量限制性毒性。在所有36例可评估疗效的患者中,伯瑞替尼的客观缓解率(ORR)为30.6%(11/36) ,疾病控制率(DCR)为94.4% (34/36)。
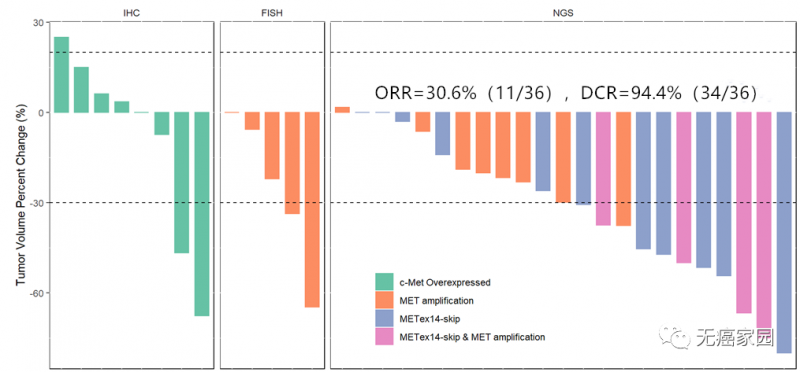
亚组分析中,在携带c-MET过表达、扩增或Ex14跳读变异的患者中,ORR分别为30.6%, 41.2%和66.7%;在携带c-MET过表达且伴随基因扩增的6例患者中的ORR为50%;在携带c-MET基因Ex14跳跃突变且伴随基因扩增的4例患者中,ORR达100%。
综上,伯瑞替尼治疗c-Met 异常的晚期非小细胞肺癌的疗效可观,前景广阔。
新药TAK-788用于NSCLC EGFR 20ins突变疗效突出
Mobocertinib(TAK-788,曾用代号AP32788)是武田制药研发的一款小分子EGFR/HER2抑制剂,日前美国FDA已授予突破性疗法认定(BTD)药物资格。2020年4月28日,AACR年会报道了1/2期临床试验的结果。
Mobocertinib基于奥希替尼的骨架核心改进,大大提高了对EGFR 20外显子插入突变的活性,28例可供评估的EGFR 20外显子插入突变经治NSCLC患者,客观缓解率(ORR)为43%,中位无进展生存期为7.3个月。
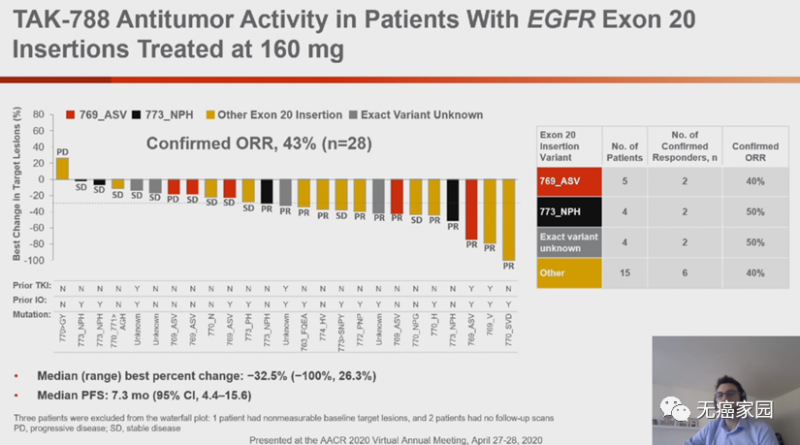
Mobocertinib 160mg每天一次剂量组的多数不良反应为1~2级,常见的不良反应有腹泻、恶心、皮疹、呕吐、食欲下降等。
目前,Mobocertinib对比培美曲塞联合铂类一线治疗EGFR 20外显子插入突变复发性或晚期NSCLC患者的三期临床试验(NCT04129502)已经开展(美国4个临床点,西班牙1个)。
针对EGFR 20ins突变非小细胞肺癌的药物还有JNJ-6372,我们敬请期待这两种药物能够尽快上市,造福更多的癌友!
相关文章:肺癌新药,FDA授予肺癌EGFR靶向药新药JNJ-61186372(JNJ-6372)突破性治疗称号
大展拳脚!卡瑞利珠单抗联合阿帕替尼为小细胞肺癌带来新希望!
卡瑞利珠单抗和阿帕替尼分别为恒瑞医药研发的PD1单抗和口服抗血管多靶点TKI,双药组合在多个癌种都在火热进行研究,初步数据非常亮眼,并且做到了无化疗!
此次大会上报道了关于卡瑞利珠单抗注射液加阿帕替尼治疗广泛期SCLC(小细胞肺癌)的II期PASSION研究结果。
此研究共纳入59例患者,其中阿帕替尼每日服药组中有47例。截止到2019年12月12日,研究结果显示,阿帕替尼每日服药组(试验组)确认的ORR为34.0%,疾病控制率(DCR)为68.1%。中位无进展生存期(PFS)为3.6个月,中位OS为8.4个月。进一步分层分析发现,化疗敏感患者(铂类化疗后疾病复发≥90天)和化疗抵抗患者(铂类化疗后疾病复发<90天)具有相似的ORR(37.5% vs 32.3%)、中位PFS(3.6 vs 2.7个月)和中位OS(9.6 vs 8.0个月)。
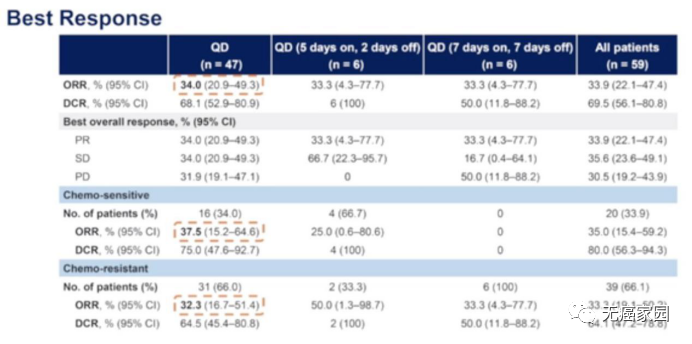
安全性方面主要有43例报告了≥3级的治疗相关不良事件,最常见的为高血压、手足综合征和血小板计数减少。整体而言,报告的不良事件可控。
在含铂化疗失败广泛期小细胞肺癌患者中,卡瑞利珠单抗联合阿帕替尼作为二线治疗对化疗敏感和化疗抵抗患者均显示出强有力的抗肿瘤活性,并具有可接受的毒性。
古巴EGF疫苗联合O药延长生存期至13.7个月
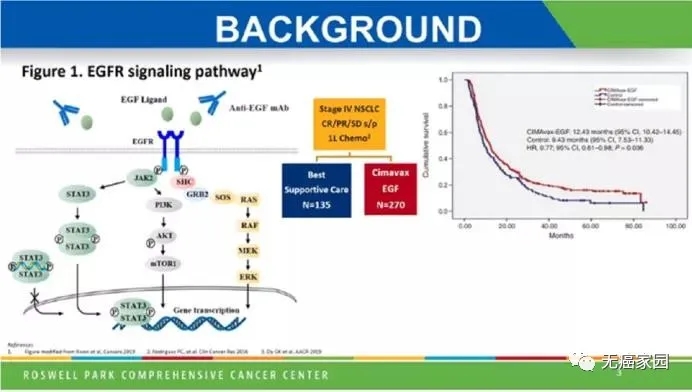
古巴EGF疫苗(CIMAvax-EGF)是一种比较古老的肺癌治疗性疫苗,先前的III期临床研究结果显示晚期NSCLC一线化疗结束后以古巴疫苗维持治疗,中位OS为12.43个月,优于化疗的9.43个月。
此次会议上报道了古巴EGF疫苗联合O药治疗NSCLC的I期研究结果。该研究纳入13例患者,大部分患者PD-L1表达为0。结果显示,古巴EGF疫苗联合O药之后患者可以更快达到足够的抗EGF效果,4剂古巴EGF疫苗联合O药后100%的患者抗EGF抗体滴度> 1:4000,而在以前的研究中单独使用古巴EGF疫苗时为56%。
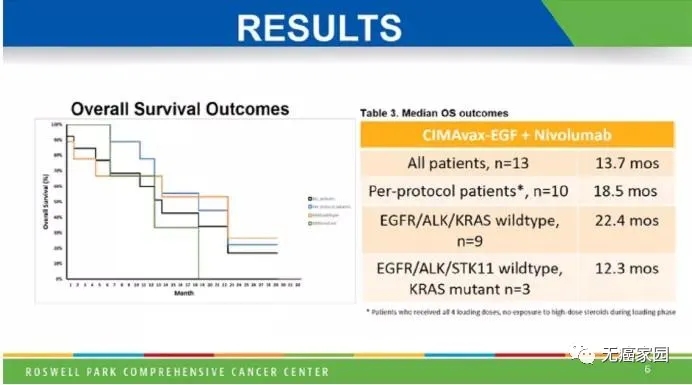
13例患者的中位OS为13.7个月,优于Checkmate 057研究中O药单药治疗PD-L1<10%患者的9.9个月。而完成4剂古巴EGF疫苗注射的10例患者中,中位OS达到18.5个月。
此外,EGFR/ALK/KRAS阴性的9例患者中位OS达22.4个月,而EGFR/ALK/STK11阴性KRAS阳性的3例患者中位OS为12.3个月。这似乎与Checkmate 057研究相反,联合治疗时KRAS阴性患者总生存期获益更大。
乳腺癌篇
OS翻倍,免疫激动剂联合PD1开创乳腺癌新免疫治疗时代
既往的研究都证实乳腺癌治疗的单药疗效一般,因此乳腺癌的免疫疗法更倾向于联合用药。在大会上就公布了关于IMPRIME I期的研究,主要是采用一种免疫激动剂PGG联合K药进行三阴乳癌的后线用药。
结果显示,与单独用药相比,纳入患者各项疗效指标均有显著的提升,无进展生存率达15.9%,OS提升到16.4个月,且安全性可靠。
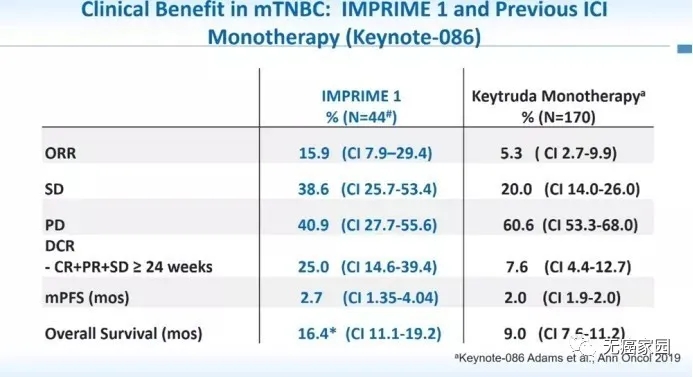
而在入组治疗的44例三阴性乳腺癌患者中,有12例既往伴有激素受体阳性,经过内分泌治疗后转化为三阴乳癌的患者。对于在这类既往内分泌型转化而来的三阴乳癌患者,该新方案的无进展生存率高达50%,中位OS为17.1个月,疗效很突出。

高危HER2阴性乳癌闻风丧胆!三药联合创37%高病理完全缓解率
如何高危HER2阴性乳腺癌的新辅助治疗的疗效一直是医学研究者们所关注的焦点,鉴于此前PDL1单抗durvalumab+奥拉帕尼在BRCA突变HER2阴性乳腺癌的高无进展生存率,此次大会上公布了一项关于2期高危乳腺癌患者术前新辅助疗法I-SPY2的研究结果。
患者的纳入标准:II/III期HER2阴性的高危乳腺癌患者,必须有明确的靶病灶(大小≥2.5cm),ECOG评分<2分。
若激素受体呈阳性,需要经Mamma Print评分评估为高复发风险患者。所有患者整体治疗计划为术前新辅助+手术+术后辅助的治疗方式。
最终结果显示,单纯紫杉醇新辅助治疗组的病理完全缓解率(pCR)率为20%,durvalumab+奥拉帕尼+紫杉醇的pCR率为37%,完全缓解率将近翻倍。在HER2阴性/ER阳性(高复发风险)人群中,两组的pCR率分别为14%、28%;在三阴性乳腺癌中,两组的pCR率分别为27%、47%。
肾癌篇
75%的肿瘤缩小,溶瘤病毒+PD1治疗肾癌显奇效!
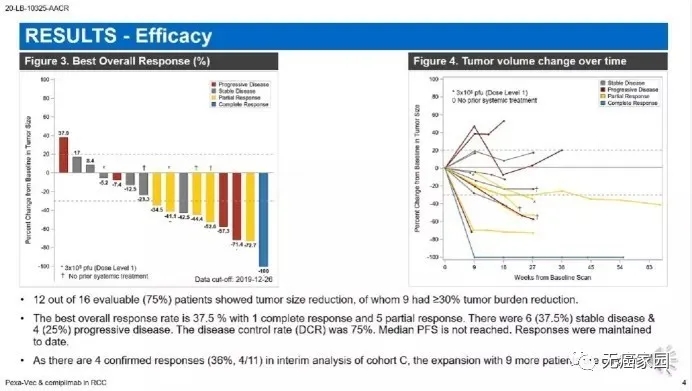
此次会议上报道的一则关于REN026的试验,主要对初治或经治的晚期肾细胞癌患者使用Pexa-Vec联合PD1单抗Cemiplimab进行治疗。其中,Pexa-Vec是一款经工程化表达GM-CSF(重要的免疫细胞因子)的溶瘤性病毒疫苗。
结果显示,16例可评估患者中,共有75%患者都出现肿瘤减小,9例患者肿瘤负荷缩小了≥30%。 ORR为37.5%,其中1例达到完全缓解。疾病控制率(DCR)为75%。中位无进展生存时间(PFS)未达到。
广谱抗癌篇
双靶点治疗KRAS突变实体瘤疗效提升,ORR高达67%
VS-6766是RAF/MEK抑制剂,defactinib为FAK抑制剂,两者联用在理论上可更全面地抑制癌细胞用来产生耐药性的信号通路。
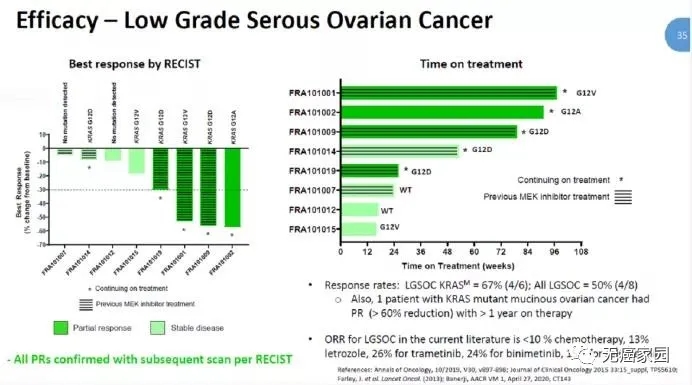
大会上公布了关于RAS突变的晚期实体瘤患者(包括低级别浆液性卵巢癌、KRAS突变NSCLC及RAS突变结直肠癌),接受VS-6766和defactinib联合治疗的1期研究。
结果显示,总体低级别浆液性卵巢癌患者的ORR为50%(4/8),KRAS突变卵巢癌的ORR为67%(4/6),其中1例PR持续了1年以上。与既往的数据相比,这类患者用化疗的ORR<10%,曲美替尼为26%,binimetinib为24%,司美替尼为15%,这意味着双靶治疗带来疗效提升。此外,在携带KRAS突变的10例NSCLC患者中,DCR为80%。
ORR高达79%,不限癌种拉罗替尼攻克NTRK实体瘤
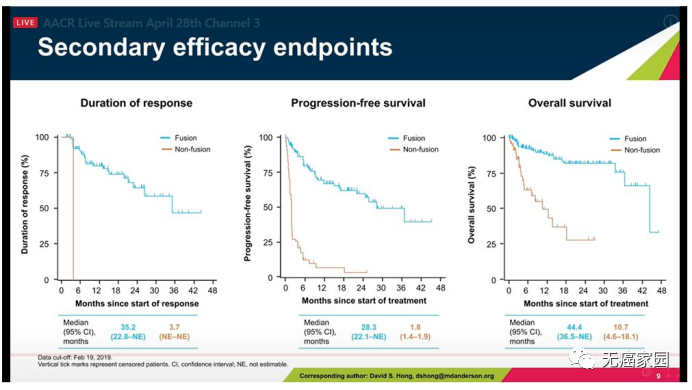
此次大会上更新了广谱抗癌药拉罗替尼治疗NTRK实体瘤的数据。
其中,NTRK融合组的中位DOR为35.2个月,非融合组的DOR为3.7个月.融合组的中位PFS为28.3个月,非融合组的中位PFS为1.8个月。融合组的中位OS为44.4个月,非融合组的中位OS为10.7个月。融合组在中位DOR,中位PFA,以及中位OS表现方面都优于非融合组。
相关文章:广谱抗癌药,广谱靶向药Vitrakvi拉罗替尼中国临床试验正式开展
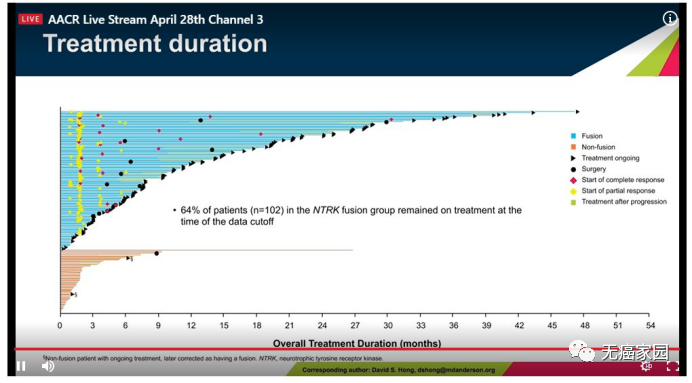
治疗反应:NTRK融合组中64%的患者仍在继续治疗。
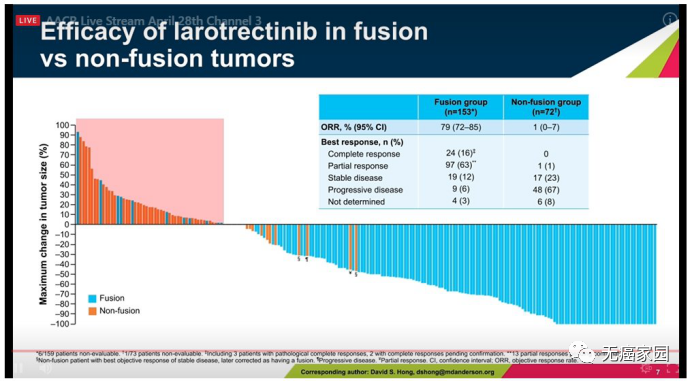
在肿瘤尺寸改变方面,融合组相比非融合组体现了较大的肿瘤大小的缩小。在ORR方面,融合组的ORR为79%,非融合组的ORR为1%,融合组的疗效显著优于非融合组。在 反应方面,融合组中CR率为24%,而在非融合组,CR率为0。从而可以看出融合组在疗效和 反应方面的表现都显著优于非融合组。
参考文献
1.https://www.texascenterforprotontherapy.com/cancers-treated/breast-cancer
2.https://www.nm.org/healthbeat/patient-stories/breast-cancer-at-35
3.https://provisionhealthcare.com/cancers-we-treat/breast-cancer/
4.https://www.ncbi.nlm.nih.gov/pubmed/29437116







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城