广谱抗癌药,广谱靶向药,恩曲替尼(Entrectinib)临床试验志愿者招募进行中
近两年,最火的抗癌药除了PD-1就是NTRK抑制剂。
2019年8月,FDA加速批准了全球第三款广谱“无进展生存系”抗癌药entrectinib上市,用于治疗具有NTRK融合物的12岁及以上患有实体瘤的成人和儿童患者以及ROS1阳性,转移性非小细胞肺癌(NSCLC)的成人。
这款药物之所以让医学界和患者都为之振奋,最大的三个看点在于:
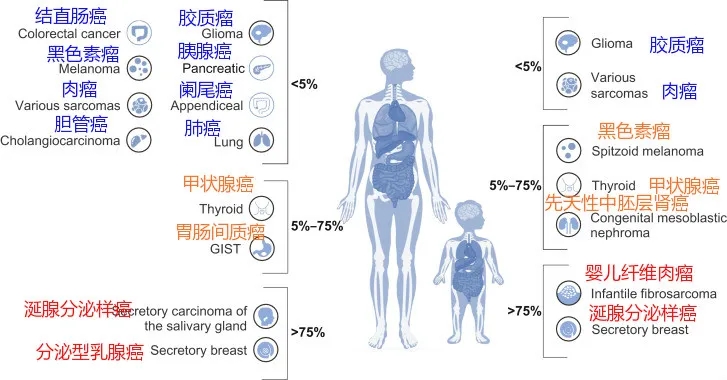
不限癌种,对25种癌症有效
这意味着不管肿瘤发生在什么部位,是否发生了转移,只要存在NTRK融合,就有可能快速起效,目前已发现NTRK融合存在于超过25类癌症中,包括乳腺癌、结直肠癌、肺癌、甲状腺癌等,并且成人和儿童患者都可以使用。
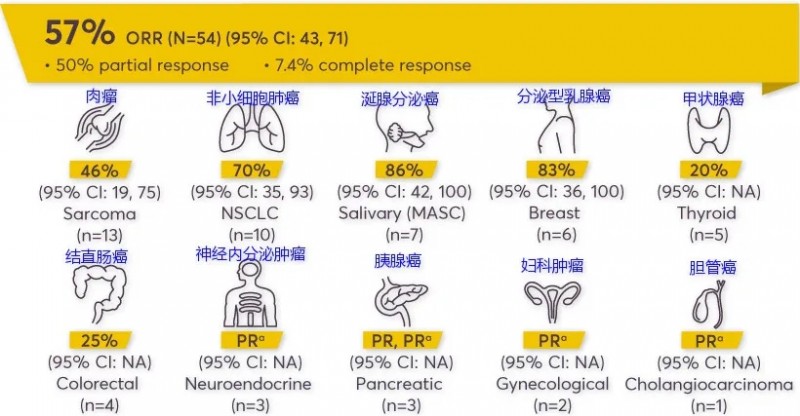
总缓解率高达57%
在TRK融合癌患者的三项大型临床试验汇总数据显示,恩曲替尼的总缓解率ORR为57%,其中7.4%的患者完全缓解(肿瘤全部消退)。并且对于特定的人群,恩曲替尼的无进展生存率能达到100%。
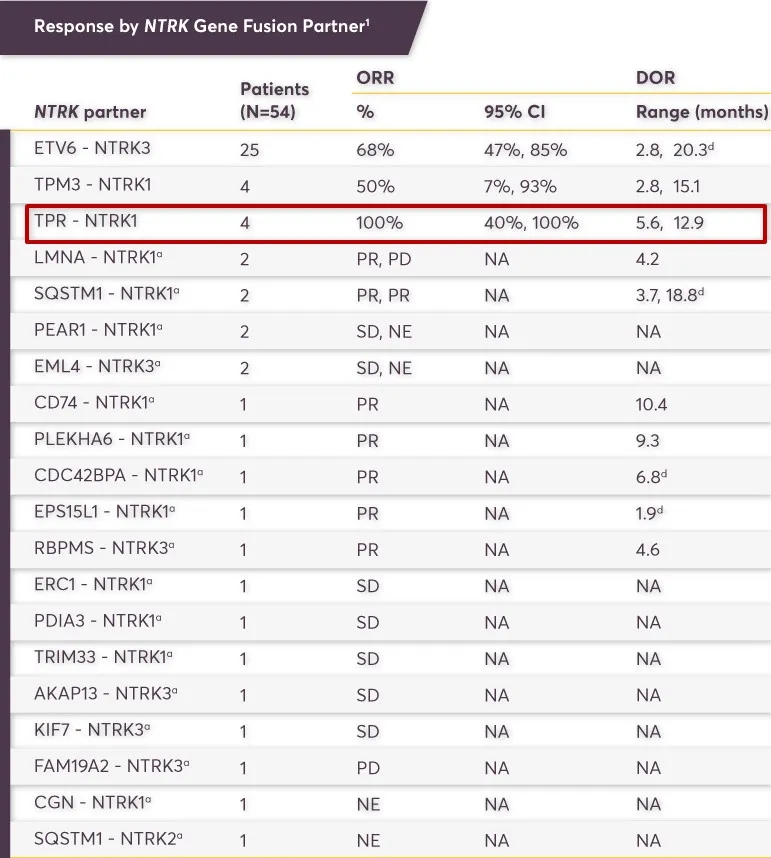
在研究中4例TPR-NTRK1融合的患者,客观缓解率达到了100%。
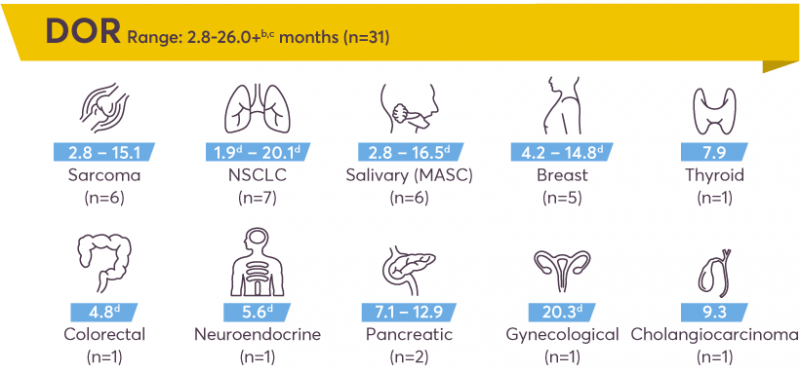
疗效持久
研究的汇总分析显示,68%的患者接受治疗后的持续缓解时间超过6个月,45%的患者持续缓解时间超过一年,也就是在一年的时间里肿瘤都在不断缩小,病情在不断好转。持续缓解时间从2.8个月~26个月不等。
虽然恩曲替尼对于特定癌症患者的效果惊人,但是目前仅在美国上市,并且口服胶囊形式的价格为每月17050美元,每年393600美元(约146万多人民币),此价格对于国内普通家庭的患者来说,堪称天价!很多病友迫切的希望国内能尽快开展这款新药的临床试验。
中国NTRK招募近况公布
近期罗氏公司宣布,“无进展生存系”抗癌药恩曲替尼针对成人实体瘤的临床试验终于正式在国内开始招募患者了!儿童患者的招募也正在协商中。那么国内招募的近况如何呢?
自恩曲替尼在国内开展招募以来,共有103例NTRK融合患者纳入中国NTRK融合真实世界调查研究,这是国内首个对于NTRK融合突变的来自真实的医疗环境,反映实际诊疗过程和真实条件下的患者健康状况的研究,意义非凡。
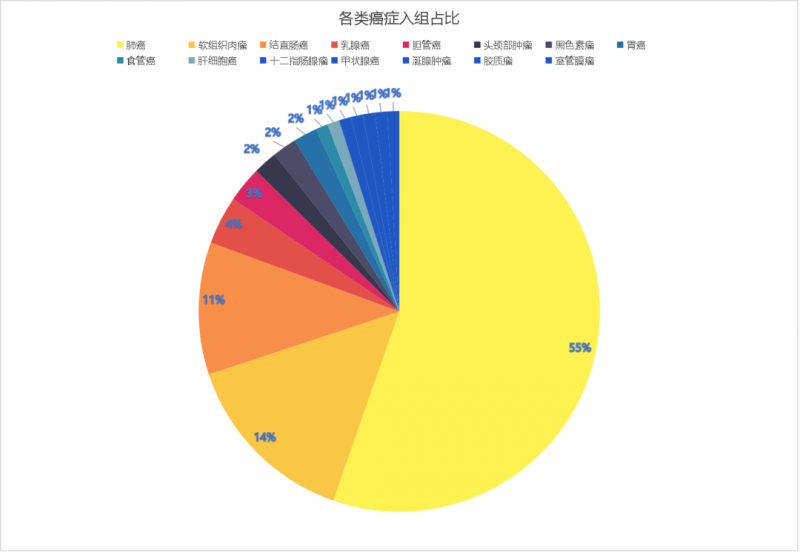
据招募方公布,截止目前,共入组筛查肺癌患者57例,软组织肿瘤患者15例,结直肠癌患者11例,乳腺癌患者4例,胆管癌患者3例,头颈部肿瘤患者2例,黑色素瘤患者2例,胃癌患者2例,食管癌患者1例,肝细胞癌患者1例,十二指肠腺癌患者1例,甲状腺癌患者1例,涎腺肿瘤患者1例,胶质瘤患者1例,室管膜瘤患者1例。
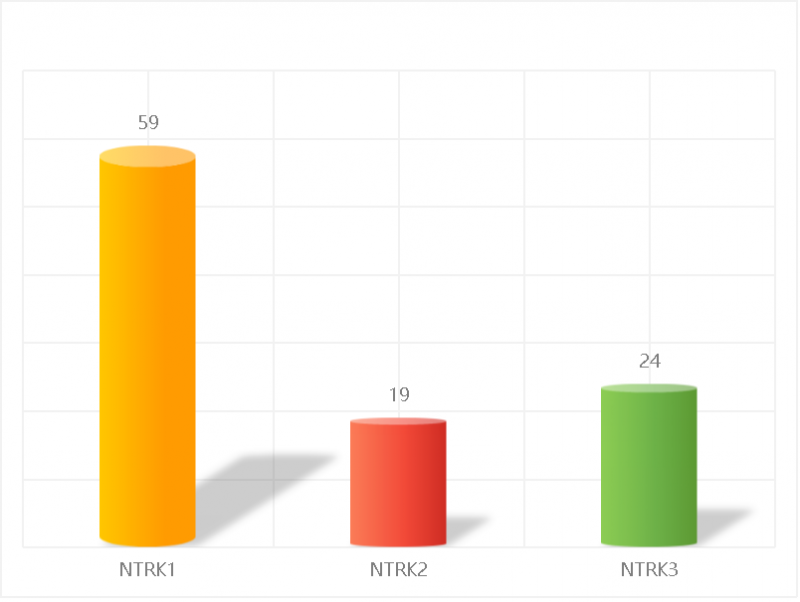
其中最多的为NTRK1融合(59例),其次为NTRK3融合(24例),再次为NTRK2融合(19例)。
实体瘤中NTRK融合各亚型比例分布
首次公布,中国团队NTRK融合真实世界研究
2018年11月,中国在世界肺癌大会(WCLC)年会上以壁报交流形式首次报道中国人群肺癌中NTRK融合的流行病学数据,在2719例肺癌标本中发现只有1名(0.04%),该亚型为TPM3-NTRK1融合,但未发现其他类型NTRK融合。该患者被认为对NTRK抑制剂有部分反应[2018WCLC P2.03-09]。
2020年中国研究团队又在AACR上以壁报交流形式公布至今为止中国人群最大队列40例NTRK融合,其中肺癌18例(0.26%),乳腺癌4例(0.21%),结直肠癌5例(0.38%),软组织肿瘤11例(3.53%),头颈部肿瘤1例(0.38%)和其他肿瘤1例(0.05%),其中大部分已入组对应临床试验[2020AACR #38]。
非常值得一提的是,国内团队在oncologist(IF=5.252)上公布了全球第一例RFWD2-NTRK1和SPATA46-NTRK1融合。

广谱抗癌药恩曲替尼中国招募正式开始
相信很多国内的患者都对这款药物充满期待,目前恩曲替尼在国内的招募已经正式开始,由国内肿瘤领域的几家医院率先开展。这意味着,国内的患者也终于有机会免费用上这款美国的抗癌“特药”!这对于所有国内的患者来说又多了一份“无进展生存”的希望!
成人实体瘤招募信息
这项 Entrectinib治疗携带 NTRK1/2/3、ROS1或 ALK基因重排的局部晚期或转移性实体瘤患者的开放性、多中心、全球性 II期篮式研究,来确定携带NTRK1/2/3、ROS1或ALK基因重排的每类实体瘤患者人群(篮子)接受Entrectinib治疗后的客观缓解率(ORR)。
试验分类:安全性和有效性
试验范围:国际多中心试验
试验分期:II期
主要终点指标:由独立放射学审查委员会测定 总缓解率
入组条件(部分):
1. 经组织学或细胞学确诊为局部晚期或转移性实体瘤,而且根据Foundation Medicine, Inc.或CLIA认证或同等机构认可的当地诊断实验室采用任何核酸类诊断检测方法进行的检测,该肿瘤携带一种预计分别转化成具有一个功能性TrkA/B/C、ROS1 或ALK激酶结构域的融合蛋白的NTRK1/2/3、ROS1或ALK基因重排,且不同时存在第二种致癌因素(例如EGFR、KRAS);
2. 对于通过当地实验室分子检测入组的患者,要求提交存档或新鲜的肿瘤组织(除非存在医学禁忌),在Foundation Medicine, Inc.或该地区其他认可的中心实验室进行独立中心分子检测;
3. 根据当地采用RECIST v1.1进行的评估,疾病可测量。
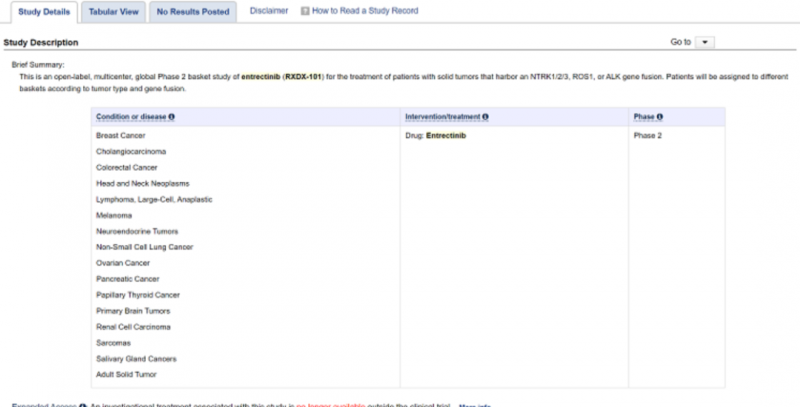
相信恩曲替尼在国内临床试验的开展,无疑让山重水复疑无路的晚期患者多了一份希望,但是想使用这款“无进展生存系”神药有个硬性条件,必须通过基因检测证实存在NTRK1、NTRK2或NTRK3融合基因的局部晚期或转移性恶性肿瘤。注意只能是融合,NTRK突变或扩增都不适合。符合条件的患者现在就可以申请了。
史无前例!无进展生存率100%,震撼肿瘤界
在正式介绍这款药物之前,我们先来看公布的数据,因为,这个数据是目前为止,包括任何靶向药(LOXO-101)和免疫治疗药物(PD-1)在内,都无法比拟的!
entrectinib的I / II期研究显示,所有携带神经营养性酪氨酸受体激酶(NTRK),ROS1或间变性淋巴瘤激酶(ALK)融合的儿童肿瘤类型对治疗的响应率高达100%(完全缓解和部分缓解)!包括难治的中枢神经系统中的肿瘤!这个数字是史无前例的,相信给儿童肿瘤患者打开了一扇全新的希望之门。
横跨十大癌症,客观缓解率57.4%
除了在儿童肿瘤中的疗效卓越,Ⅱ期临床试验STARTRK-2、I期研究STARTRK-1、I期研究ALKA-372-001的53例ROS1激活基因融合患者和54例局部晚期或转移性NTRK融合阳性实体瘤患者以及在儿科患者中开展的I/Ib期研究STARTRK-NG的数据显示:
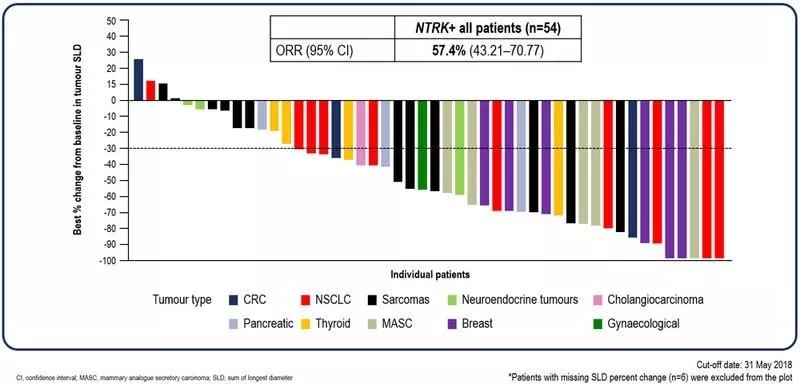
综合分析的结果显示:
1)在NTRK融合阳性实体瘤患者中,entrectinib(恩曲替尼,RXDX-101)的客观缓解率ORR(肿瘤缩小)为57.4%,并且在横跨10种不同类型肿瘤中均观察到了客观缓解(肿瘤缩小)。存在脑转移的患者中,entrectinib的颅内客观缓解率ORR为54.5%,其中超过1/4实现完全缓解(病灶全部消失)。
2)在局部晚期或转移性ROS1阳性非小细胞肺癌NSCLC患者中,临床试验结果表明,在51名ROS1阳性NSCLC患者中,总缓解率达到78%,完全缓解率达到5.9%。在肿瘤缩小的40名患者中,55%患者的缓解持续时间超过12个月。值得一提的是,这些患者包括20名(占总入组患者的37.7%)未治疗和治疗的伴有脑转移患者,反应率为55%!
关于恩曲替尼
一,药品信息
通用名:Entrectinib、恩曲替尼
获批适应症:治疗NTRK基因融合阳性的晚期复发实体瘤的成人和儿童患者,以及ROS1阳性非小细胞肺癌(NSCLC)患者。
研发公司:由生物制药公司Ignyta研发,2017年年底被罗氏耗资17亿收购。
作用机制:
恩曲替尼是一种具有中枢神经系统活性的酪氨酸激酶抑制剂(TKI),能够穿过血脑屏障,是临床上唯一一种被证明针对原发性和转移性脑疾病具有疗效的TRK抑制剂,并且没有不良的脱靶活性(off-target activity,未达到预先设定的目标);
可以阻断ROS1和NTRK激酶活性,并可能导致ROS1或NTRK基因融合的癌细胞死亡。
上市时间及国家:
2019年6月18日,经PMDA批准在日本上市
2019年8月16日,经FDA批准在美国上市
剂型:口服胶囊100/200mg
二,哪些患者可以使用
这个靶向药不仅疗效显著,还是广谱抗癌药物,对很多不同肿瘤都有效!这也这个药品这么吸引眼球的原因。
在实验中,这些患者肿瘤类型包括10种不同的肿瘤:结直肠癌,非小细胞肺癌,胰腺癌,软组织肉瘤,乳腺癌,甲状腺癌,神经系统肿瘤,妇科肿瘤,分泌型乳腺癌,胆管癌。
即使是标准治疗方案失败,也可以尝试进行基因检测,一旦存在NTRK1、NTRK2或者NTRK3基因融合,或者肺癌患者存在ROS1阳性,就可以使用这款无进展生存率超高的“无进展生存系”抗癌药。
三,加快抗癌新药上市步伐,让更多患者获益
近两年,除了免疫检查点抑制剂在肿瘤医患群体中成为焦点,其中KEYTRUDA更是成为首款不区分癌症种类和来源的广谱抗癌药,开启了肿瘤治疗的新时代,另外两款TRK抑制剂Vitrakvi&Rozlytrek也大放异彩,被誉为“无进展生存系”的传奇抗癌药,成为癌症疗法从“基于癌症在体内的起源”转向“基于肿瘤的遗传特征”这一演变过程中的重要里程碑。
以前这些美国研发上市的抗癌新药对于国内的患者来说遥不可及,近两年随着国家的重视,加快了各类抗癌药物研发上市的审批速度,让更多国外的新药好药,也能造福国内的癌症患者。
除了纷纷上市的PD-1抑制剂,2019年1月,FDA批准的第一个不区分肿瘤来源用于初始治疗的传奇抗癌药LOXO-101(Vitrakvi,拉罗替尼)在中国申报临床并获得受理,并在近期正式开展临床试验。而仅在美国上市后的三个月后,这款药物就来到了中国,希望Rozlytrek在国内开展的临床试验,给更多的患者免费用药的机会。








































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城