脑瘤细胞免疫疗法治疗,脑瘤CAR-T细胞免疫疗法治疗
作为最常见的恶性脑肿瘤,脑胶质瘤恶性程度高、生长快、病程短、术后易复发且高致残,被认为是神经外科治疗中最棘手的难治性肿瘤之一。近年来,脑胶质瘤的发病率以每年1%~2%的速度递增,多见于十几岁的青少年和40岁以上人群。
其中,胶质母细胞瘤(GBM)是脑胶质瘤中恶性程度最高的,占所有胶质瘤的一半和所有原发性脑肿瘤的15%。即便手术切除很干净,到肿瘤复发时间的平均时间仅为6.9个月,中位生存期仅为14.6个月,5年生存率只有4.7%,尚不及肺癌5年生存率的1/3,预后极差。
近30年来胶质母细胞瘤患者的临床结果几乎没有改善,采用标准疗法(手术后进行化学疗法(替莫唑胺),放疗辅助治疗),平均总生存期也仅为14.7至16.6个月。
对于这种肿瘤,目前没有任何治愈方法,治疗很困难,一是因为胶质母细胞瘤会将触角伸入大脑,而不是形成医生可以瞄准和移除的固体肿块。所以想将它们完全清除是不可能的。二是因为大脑有一个保护层叫做血脑屏障,因此绝大部分的抗癌药都无法到达脑瘤的部位。临床迫切需要新的治疗方式。让我们一起来看下全球范围内有哪些新型细胞免疫疗法给癌友们带来新的希望。
国际新型细胞免疫疗法或延长脑瘤患者存活期
据新华社8月18日报道,澳大利亚伯格霍弗医学研究所开发出一种新的细胞免疫疗法,在临床试验中延长了多形性胶质母细胞瘤患者的平均存活期。相关论文已发表在新一期美国《Journal of Clinical Investigation(临床检查杂志)》上。
该机构教授拉吉夫·康纳和同事一起开发出一种新的细胞免疫疗法,在临床治疗中先提取患者血液样本,将其中的人体T细胞经人工强化后再重新输入患者体内,使其可以识别并杀灭巨细胞病毒。此前有研究认为,多形性胶质母细胞瘤发病可能与巨细胞病毒感染有关,因为巨细胞病毒在患者癌细胞中表达率极高。
在一期临床试验中,25名已完成手术等常规治疗的多形性胶质母细胞瘤患者接受了这种免疫疗法作为辅助治疗。结果显示,这些患者平均存活期提高至21个月,较目前该类型脑癌患者平均存活期有提升,而且该疗法对于患者是安全的。研究人员表示将进一步改善该疗法。
争奇斗艳,多种CAR-T疗法应用于不同类型的脑瘤效果显著
1、CAR-T应用治疗复发性脑瘤,疗效与安全兼收
靶点:EPHA2、HER2和IL13Rα2
髓母细胞瘤和室管膜瘤是最为常见的儿童恶性脑肿瘤,对脑瘤患者的影响极大,并且在复发时基本无法治愈。
就在2020年4月27日,来自德克萨斯儿童医院和贝勒医学院的研究人员发表在《Nature Medicine》杂志上的报告称,他们开发出一种新方法能够将合适靶点的CAR-T细胞直接输送到脑脊液肿瘤周围,用以治疗脑瘤。

与胶质母细胞瘤不同的是,髓母细胞瘤和室管膜瘤倾向于在中枢神经系统表面复发或转移到软脑膜,在这种情况下它们都与脑脊液相邻。因此研究人员认为,脑脊液和复发位置之间的空间为局部治疗提供了机会。
此项研究共确定3个细胞表面靶标——EphA2、HER 2和IL13Rα2。这3种靶标都在髓母细胞瘤和室管膜瘤上表达,在正常发育的大脑中不表达。在对肿瘤大小、动物存活率进行200天的研究后发现,3种CAR-T细胞的鞘内递送能够有效治疗小鼠模型中原发性、转移性和复发性髓母细胞瘤和颅后窝A(PFA)室管膜瘤。而且研究也证实,将肿瘤特异性CAR-T细胞注入脑脊液比通过血液注入更有效。
研究人员解释道:与通过血液输送不同,脑脊液的输送能克服血脑屏障,而且还能最大限度地减少身体其他组织对CAR-T细胞的暴露,从而减少潜在的副作用。
在他们的一些实验中,研究人员将CAR-T细胞与一种被批准的癌症药物——氮胞苷(azacytidine)结合起来。结果表明,免疫治疗联合氮胞苷治疗明显比单独治疗更有效。
目前,德克萨斯儿童医院和贝勒医学院的一项儿童临床试验正在招募患者来测试这种方法的安全性和抗肿瘤效果(NCT02442297)。
2、脑室内注射CAR-T细胞,首次消灭实体瘤
靶点:IL13Rα2
2016年12月,NEJM曾报道过1例利用CAR-T技术治疗脑胶质瘤的案例。一名50岁的男性,确诊为高级别脑胶质瘤,先后做了手术、放疗、替莫唑胺化疗等常规治疗,6个月后疾病复发。这时他参加了一项临床试验,接受靶向IL13Rα2的CAR-T治疗。不过这个疗法,有些“惊悚”。
主管医生通过核磁共振检查发现:这位病友脑部有5个病灶;因此,先通过手术切掉其中的三个大的,还剩下两个较小的由于位置深,无法切除。主管医生就给他的病灶处直接插了一个管子,然后通过这个管子,把CAR-T细胞打了进去,分3个批次,进行了多次的细胞回输。最终,肿瘤完全消失,疗效维持了8个月左右。
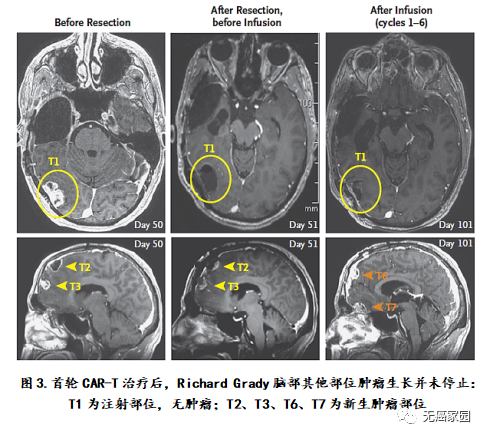
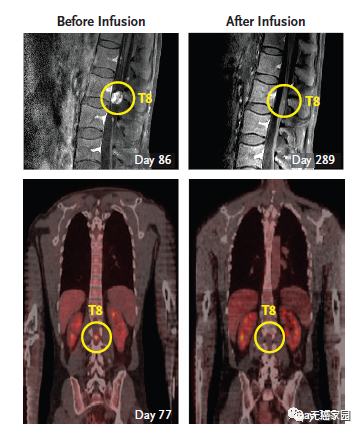
第二轮CAR-T疗法结束后,Richard Grady脊索内肿瘤出现剧烈萎缩
目前,CAR-T疗法治疗脑瘤的前瞻研究国内也在积极的开展临床试验,大家可持续关注无癌家园网站及公众号。
3、黄金搭档出击!CAR-Ts+BiTE双剑合璧"咬死"脑瘤
靶点:EGFRvIII
世界卫生组织统计,按死亡率顺序排位,恶性胶质瘤是34岁以下肿瘤患者的第2位死因,是35~54岁患者的第3位死因。而胶质母细胞瘤(GBM)占所有胶质瘤一半以上。据调查,颅脑肿瘤整体的5年相对生存率为35.8%,而胶质母细胞瘤的5年相对存活率最低,仅为6.8%,甚至低于胰腺癌的8.0%,这恐怕是恶性肿瘤中最低的数字。
2019年下半年发表于《自然》子刊《Nature Biotechnology》上的一篇论文中,来自哈佛医学院麻省总医院的科学家们展示了一项抗击大脑恶性肿瘤的研究结果。他们结合CAR-Ts和BiTEs两种抗癌新技术,对胶质母细胞瘤展开有效攻击。利用可产生双特异性抗体的新型CAR-T细胞进行治疗,在80%的小鼠中,脑内的肿瘤完全消失!

解析小贴士
CAR-Ts是经过基因工程改造的免疫细胞,具有识别能癌细胞分子的受体。已经获得批准的两个,诺华公司(NVS)Kymriah和吉利德(GILD)Yescarta,均是2017年获批,适用于血液癌症中的急性淋巴细胞白血病和特定类型的非霍奇金淋巴瘤。CAR-Ts对抗实体瘤的研究虽然热火朝天,但一直没有实质性进展。
BiTE[Amgen(AMGN)],即双特异性T细胞抗体桥,是一种实验室制造的抗体,具有两个分子钩:一边用于抓住T细胞,另一边抓住肿瘤细胞,从而形成一个分子桥,能刺激T细胞产生杀伤肿瘤细胞的蛋白。
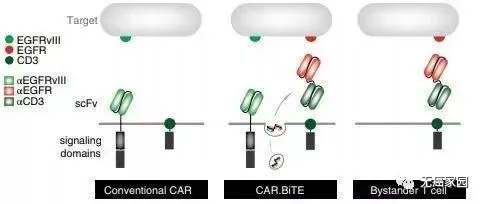
这项研究负责人Marcela Maus教授曾经尝试过让CAR-T细胞去识别EGFRvIII,对胶质母细胞瘤发起攻击。可实体瘤之所以难治,很棘手的原因在于“异质性”,这些癌细胞的分子特征不尽相同。在胶质母细胞瘤中,还有很多细胞不表达突变形式的EGFR,却大量表达正常的EGFR,它们同样会放大生长信号,造成肿瘤疯长。这时候,光靠识别EGFRvIII的CAR-T细胞还不能击退肿瘤。
图示表达双特异性抗体的CAR-T细胞
接下来,研究团队在胶质母细胞瘤小鼠模型中检验了这种新CAR-T细胞的治疗潜力。他们在免疫缺陷型小鼠脑中植入了人脑胶质瘤细胞,然后把分泌BiTE的CAR-T细胞注入小鼠体内,同时靶向表达EGFRvIII和EGFR的肿瘤细胞予以打击。经过3周时间,80%的小鼠表现出了“完全缓解”,体内已经看不到肿瘤!
图示分泌BiTE靶向EGFR的CART-EGFRvIII细胞,让小鼠脑内的肿瘤在3周之内显著缩小甚至完全消失
此外,由于针对EGFR的BiTE会局部地在CAR-T细胞到达的部位起作用,并不影响其他表达EGFR的正常组织,这一点研究者也在小鼠身上通过移植的人体皮肤进行了检验,为这种疗法的安全性提供了数据。同时,研究者还为这种CART.BiTE细胞申请了专利,并希望开展进一步的临床试验。
除了上述提到的比较突出的研究外,CAR-T治疗脑瘤的主要靶点还包括HER2等,由于是临床前研究,小编不一一赘述。目前国内正在积极开展关于实体瘤的CAR-T临床研究,不仅仅适用于脑瘤患者。
小编有话说
恶性脑瘤,尤其是胶质母细胞瘤虽然是最常见的恶性肿瘤,5年相对存活率仅有6.8%,但相信在不久的将来定会涌现出越来越多的治疗新技术和新型药物针对难治性、转移性脑瘤,而且本文中提到的各类新的研究也不会止步于此,我们共同期待未来越来越多意想不到的临床研究成果。








































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城