遗传性乳腺癌BRCA基因突变,BRCA突变靶向药,BRCA靶向药,PARP抑制剂有哪些
关键词:靶向药物,PARP抑制剂,BRCA基因
相信很多患者都发现了,靶向药物与靶标之间是类似“钥匙”和“锁”的关系。通常情况下,一把钥匙对应且只对应一把同名的锁,比如EGFR抑制剂治疗EGFR突变阳性的患者、HER2抑制剂治疗HER2突变阳性的患者。
但有一种“抑制剂”药物却打破了这个规律,成了众多靶向药物当中的“特例”——这就是PARP抑制剂,主要用于治疗BRCA基因突变阳性的患者。“PARP”和“BRCA”这两个靶标怎么看都不太一样。
为何PARP抑制剂有这样的特殊之处?PARP抑制剂治疗BRCA突变患者疗效如何?本次,小汇就来和大家一起聊一聊BRCA突变和它的“克星”PARP抑制剂。
乳腺癌易感蛋白(BRCA)
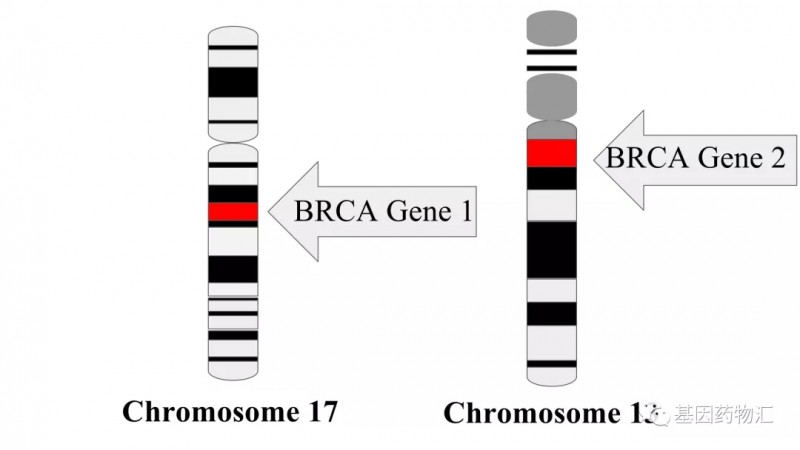
关键词:DNA修复,抑癌基因,非伴性遗传
可能导致的癌症:乳腺癌,卵巢癌,直肠癌,胰腺癌,前列腺癌等
乳腺癌易感蛋白(BRCA)基因属于一种抑癌基因,也被称为看护基因,其编码合成的对应蛋白质有修复DNA的功能。一旦此类基因发生突变,其修复DNA的功能丧失,细胞癌变的风险就会增加。
虽然名字叫“乳腺癌易感蛋白”基因,但BRCA基因突变可能导致的癌症种类远不止乳腺癌,这一基因突变同样可以导致结卵巢癌、直肠癌、胰腺癌和前列腺癌等癌症的风险增加。
BRCA基因分为BRCA1与BRCA2,两者并不相关,但都可参与帮助修复受损DNA的过程,或在无法修复DNA的情况下破坏细胞。它们参与染色体损伤的修复,在DNA双链断裂的无错修复中起重要作用。
BRCA基因突变是一类可以通过遗传的方式传递给后代的突变类型,不论性别的子女都可能从父母处继承此突变型。具有BRCA1或BRCA2有害突变的女性,发生乳腺癌的风险约为健康女性的5倍,发生卵巢癌的风险约为健康女性的10~30倍。一些研究认为,存在BRCA1有害突变的女性,发生乳腺癌或卵巢癌的风险比存在BRCA2有害突变的女性更高。
尽管男性罹患乳腺癌的风险很低,但携带了BRCA基因突变的男性发生乳腺癌的风险仍然高于健康男性,并同样能够将这一突变型遗传给自己的子女。
当然,BRCA突变并非导致这些癌症的唯一原因。在女性乳腺癌患者中,仅有约5%~10%归因于BRCA1或BRCA2突变。流行病学研究认为,BRCA1/2突变的患者同时存在HER2突变的概率更低,BRCA1突变阳性患者的CK5/6突变和EGFR突变概率更高,激素受体阳性率更低,多为三阴性乳腺癌。但由于乳腺癌患者基数庞大,且BRCA突变可能导致的癌种很多,及其不伴性遗传的特点,BRCA突变仍然是威胁人类健康、尤其是女性健康的重要原因。
聚(ADP-核糖)聚合酶(PARP)
关键词:DNA修复,细胞程序性凋亡
聚(ADP-核糖)聚合酶(PARP)指一类蛋白质,由17个成员组成,分别具有不同的结构和功能,涉及许多细胞过程,包括DNA修复、基因组稳定和调控细胞程序性死亡过程。
PARP可以在受到损伤、尤其是DNA损伤的细胞中被激活,消耗细胞中的ATP(腺嘌呤核苷三磷酸,可以为细胞生理活动提供能量)修复受损的DNA,细胞中的ATP耗尽可能导致细胞裂解或死亡(坏死)。同时,PARP还能够通过产生PAR来诱导程序性的细胞死亡,是细胞凋亡的重要途径之一。
关于PARP还有一些非常有趣的研究。针对13种哺乳动物的研究认为,PARP的活性与该物种的最大寿命有关,很可能有助于延长哺乳动物的寿命。其中寿命最长的物种(人类)和寿命最短的物种(大鼠)的PARP活性差了5倍,人类PARP-1的自我修复能力(specific automodification)是大鼠的2倍。寿命达到100岁以上的人类血液样本中淋巴母细胞系具有比年轻个体(20~70岁)更高的PARP活性。
BRCA突变与PARP抑制剂,抗癌三十六计之"围魏救赵"
在一个正常(或者不正常的)细胞周期中,细胞的DNA很可能被破坏了数千次。如果不能及时有效地修复这种破坏,细胞很可能会因此而死亡。
PARP与BRCA共同调控细胞的DNA修复过程。通常情况下,细胞中常见的DNA修复方式包括两种,碱基切除修复(BER)和同源重组修复(HRR)。
PARP与细胞碱基切除修复过程相关,在这一过程中PARP蛋白会与DNA损伤位点结合。使用PARP抑制剂可以阻断PARP蛋白从DNA损伤位点脱落的过程,导致蛋白质无法脱落,DNA复制等过程无法顺利继续。
BRCA(BRCA1、BRCA2和PALB2)与细胞同源重组修复过程相关,发生BRCA突变的细胞无法进行同源重组修复,只能选择采用碱基切除修复的方式。因此,对发生了BRCA突变的癌细胞使用PARP抑制剂,能够导致癌细胞发生“合成致死”,杀灭癌细胞。
简单来说,这是一种通过PARP抑制剂斩断癌细胞的“退路”,迫使它踏入另一条走不通的“死路”中,最终达成将其杀灭的目的的治疗方式。这种方式就如同三十六计当中“围魏救赵”这一计,以逆向思维的方式,以表面来看舍近求远的方式,绕开问题的表面现象,从本源着手解决肿瘤、一招制胜,可以说是精彩至极。
由于这样的特点,PARP抑制剂成为了BRCA突变型肿瘤当之无愧的“克星”。
近期,一些研究也证实,氧气含量更低的细胞(例如正在快速生长的癌细胞)对于PARP抑制剂更加敏感。
已经获批上市的PARP抑制剂有哪些
目前,已经有多款PARP抑制剂获批上市,用于治疗包括乳腺癌、胰腺癌、前列腺癌、卵巢癌、输卵管癌、原发性腹膜癌在内的多个癌种。
奥拉帕利(Olaparib)
适应症:
既往接受过三线以上化疗的BRCA突变阳性晚期卵巢癌;
铂类药物治疗缓解后又复发的卵巢上皮癌、输卵管癌或原发性腹膜癌成年患者的二线维持治疗;
复发性上皮性卵巢癌、输卵管癌或原发性腹膜癌的成年患者;
BRCA突变阳性或疑似阳性、HER2阴性,曾接受过化疗的转移性乳腺癌患者;
BRCA突变阳性胰腺癌患者一线含铂化疗后的维持治疗。
奥拉帕利是首款获批上市的PARP抑制剂药物,于2014年首次获批,用于治疗BRCA突变阳性的乳腺癌患者、胰腺癌患者。奥拉帕利治疗乳腺癌患者,中位无进展生存期7.0个月、客观缓解率达到52%,显著超过化疗组患者的4.2个月和23%;此外,奥拉帕利治疗患者的完全缓解率达到7.8%,而化疗组仅为1.5%。
奥拉帕利治疗胰腺癌,中位无进展生存期7.4个月,与安慰剂组患者的3.8个月相比几乎翻倍;此外,奥拉帕利治疗的整体缓解率达到23%,显著超过安慰剂组的12%。
尼拉帕利(Niraparib)
适应症:
铂类化疗敏感的复发性卵巢癌、输卵管癌或腹膜癌,不论患者PARP状态如何。
尼拉帕利首次于2017年获得FDA批准上市。在针对553例患者的试验中,BRCA突变阳性或疑似阳性的患者,接受尼拉帕利治疗的无进展生存期为21.0个月,接受安慰剂治疗的无进展生存期为5.5个月;BRCA突变阴性的患者,接受尼拉帕利治疗的无进展生存期为9.3个月,接受安慰剂治疗的无进展生存期为3.9个月。
他拉唑帕利(Talazoparib)
适应症:
BRCA突变阳性或疑似阳性、HER2阴性,局部晚期或转移性乳腺癌成年患者。
他拉唑帕利首次于2018年获得FDA批准上市。在Ⅲ期EMBRACA试验中,他拉唑帕利治疗的中位无进展生存期为8.6个月,显著超过化疗组的5.6个月,并且在所有患者亚组中均可观察到获益。此外,试验还发现该药物可以显著延迟在QOL评分中出现具有临床意义的恶化时间,即可以延缓患者病情的恶化,对于控制病情有明显益处。
鲁卡帕利(Rucaparib,Rubraca)
适应症:
经过两线或以上化疗的BRCA基因突变相关的晚期卵巢癌;
对铂类化疗有完全或部分反应的复发性上皮性卵巢癌、输卵管癌或原发性腹膜癌;
既往接受过雄激素受体靶向疗法和紫杉烷类化疗的BRCA突变阳性的转移性去势抵抗性前列腺癌成年患者。
鲁卡帕利为首款靶向BRCA阳性前列腺癌的PARP抑制剂药物,也是全球首款用于卵巢癌三线治疗的PARP抑制剂,于今年上市。该批准基于TRITON2研究的结果,中位随访13.1个月,结果显示,在mCRPC和BRCA1/2突变的患者中,客观缓解率为43.9%,PSA应答率为52.0%;60%的患者缓解持续时间≥24周。
靶向更多实体瘤的试验正在进行中,国内自主研发药物招募患者
整体来说,PARP抑制剂药物的疗效较好,在延长患者无进展生存期方面的优势尤其显著。但目前获批进入国内的PARP抑制剂药物仅有针对乳腺癌的奥拉帕利,国内患者难以获得更多药物,治疗水平仍存在很大的提升空间。
但除了大量引进国外疗效确切的药物,我国药企在新药研发方面同样进展颇丰。由我国自主研发的PARP抑制剂药物CVL218正式离开试验室、步入临床,开始招收患者了!
试验名称:CVL218 在晚期实体瘤患者中的耐受性及药代动力学 Ⅰ期临床试验
研究机构:中山大学附属肿瘤医院
试验分期:Ⅰa/Ⅰb期
试验人数:150人
试验目的:
Ⅰa 期:
确定 CVL218 单次及多次口服给药在晚期肿瘤患者中的安全性和耐受性,探索限制性毒性(DLT)及最大耐受剂量(MTD),确定进一步 临床研究的推荐剂量及给药方案。
Ⅰb 期:
评估 CVL218 的有效性,包括客观缓解率(ORR)、疾病控制率(DCR)、无进展生存期(PFS)。
纳入标准:
1、自愿参与研究,签署知情同意书,能够遵照医嘱完成治疗并配合随访;
2、年龄18~75岁(含两端),性别不限;
3、组织学和/或细胞学确诊为晚期或转移性恶性肿瘤,包括乳腺癌、前列腺癌、肺癌、膀胱癌、胃癌、肠癌、胆道肿瘤、胰腺癌、黑色素瘤、脑胶质瘤等;
4、既往接受过≤2线用于晚期或转移性疾病的化疗;
5、根据 RECIST 1.1 标准,患者至少有一处影像学(CT 或 MRI)可测量或可评估病灶(最大径≥10 mm,若为淋巴结,是短径≥1 5mm);前列腺癌以 PSA、循环肿瘤细胞指标纳入试验可不要求具有可测量或可评估病灶;
6、有证据能证实存在胚系或体系BRCA1或BRCA2基因突变,患者需根据要求提供组织或血液样本进行复核;
7、ECOG评分0~1分;
8、更多详细标准请咨询全球肿瘤医生网医学部。
申请方式:
需要申请临床试验的患者可以将基因检测报告、病理报告提交至全球肿瘤医生网医学部进行初步评估,我们的专家将为您全面分析解读检测报告、推荐新药及用药方案,并匹配适合入组的临床试验项目。
注:请将基因检测报告、诊断报告电子版或拍照发送至doctor.huang@globecancer.com,邮件中留下联系方式,医学部收到报告分析完毕后一个工作日内电话联系。







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城