全新的广谱抗癌靶点NRG1基因,首款NRG1融合突变靶向药Zeno(Zenocutuzumab、MCLA-128)已经获得FDA快速通道资格
2019年拉罗替尼的正式上市为整个癌症医疗界掀起了一阵“广谱抗癌”的热潮,一时间NTRK突变也成为了最为炙手可热的“广谱抗癌靶标”之代表。
越来越多的“旧靶标”被发掘了广谱抗癌的“新功能”,但也有许多“新靶标”被发掘出来,成为了进一步拓展靶向治疗应用范围的“灯塔”。
NRG1正是这些“新靶标”中之一。与NTRK相似,NRG1融合突变在大部分常见癌症中的检出率极低,但是可能发生于各类癌症的患者,因而具有良好的广谱抗癌潜力。
NRG1:非常罕见,但具有广谱抗癌的潜力
神经调节蛋白1(NRG1)的编码基因属于表皮生长因子家族,其合成的蛋白质NRG1属于EGFR受体家族的四种蛋白质之一。
正常生理状态下,NRG1参与神经系统和心脏的正常发育,对于维持心脏的结构、改善心脏效率以及在应急条件下心肌细胞的存活和受损情况下心肌细胞的恢复具有重要的意义。
有证据表明,NRG1是抑癌基因的一种。其最常见的突变类型为融合突变,其融合基因包括CD47、SDC4、SLC3A2和ATP1B1等。NRG1突变已经在非小细胞肺癌、胆囊癌、胰腺癌、肾癌、卵巢癌、膀胱癌、结直肠癌及肉瘤等超过10种常见实体瘤中检出,其中还包括许多对标准治疗方案发生耐药的癌症类型。
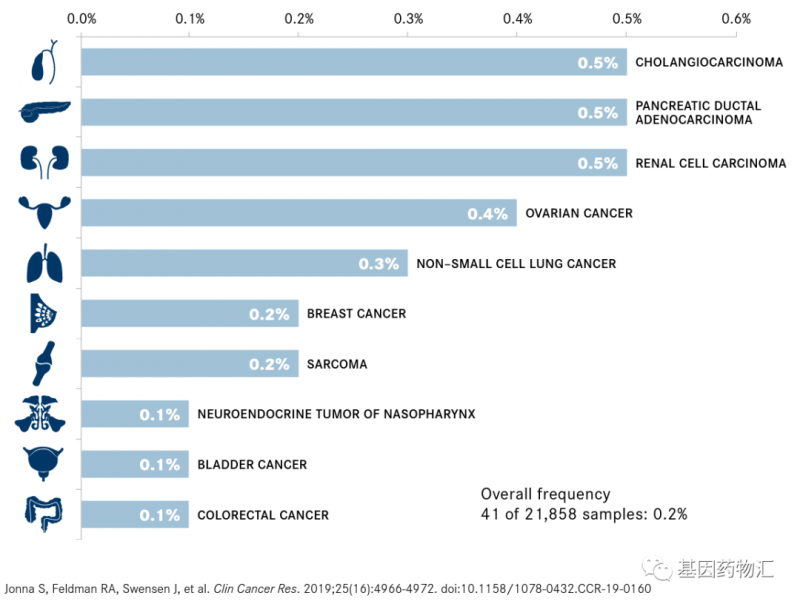
NRG1融合突变在不同类型癌症中的检出率
NRG1与ERBB家族(HER家族,包括HER1/2/3/4)存在一定的交互作用,主要作为一种激动剂或配体与HER2或HER3/4的同二聚体或异二聚体“搭档”。因此,当NRG1发生突变的时候,抑制HER2和(或)HER3/4也能取得一定的疗效。
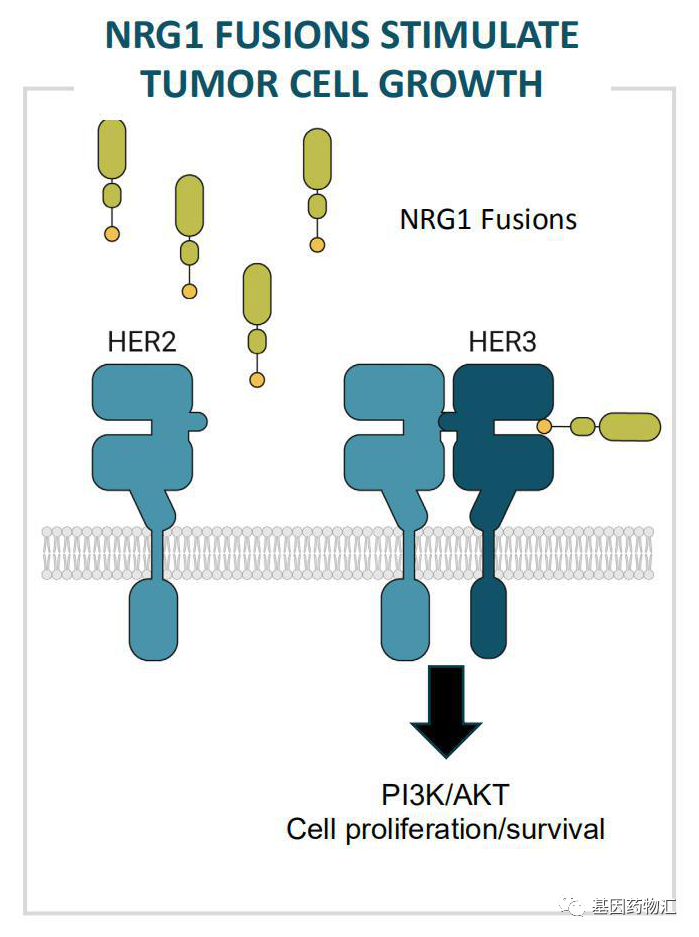
NRG1突变致癌示意图
整体来说,NRG1突变在所有实体瘤中的检出率约为0.2%,与NTRK突变等类似,非常罕见。但在部分特殊的癌症亚型当中,NRG1突变的检出率非常高。如在肺部浸润性粘液性腺癌中,NRG1突变的检出率接近30%,在胰腺导管腺癌中检出率超过5%。
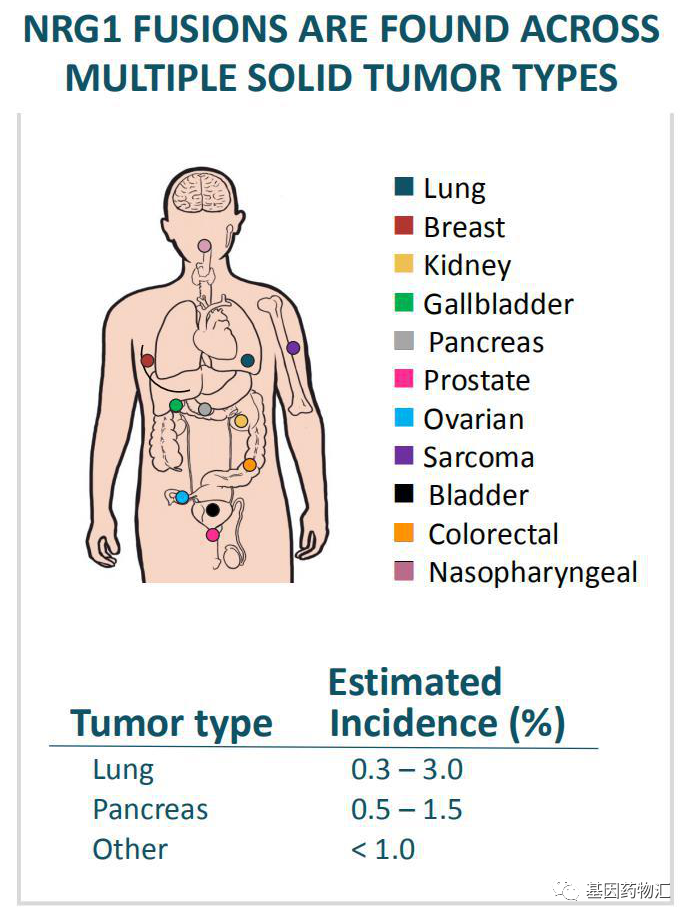
NRG1突变可能导致的癌症类型
当然,一种新兴靶点的检出率是受到基因检测技术的局限性所限制的。融合突变本身检测难度较大,需要进行RNA检测而非通常的DNA检测,且不同检测方案的敏感性存在一定的差异,我们相信,随着下一代检测手段的推广,包括NRG1在内的各类“罕见”突变,都能够得到更加准确的定位与解析。关于基因检测的更多知识,可以联系全球肿瘤医生网医学部(400-666-7998)了解。
随着靶向治疗研究的深入,类似NRG1这样罕见但具有广谱抗癌潜力的突变,正受到越来越多的重视。
Zenocutuzumab:NRG1靶点首款广谱抗癌药,已经获FDA快速通道资格
2021年1月8日,FDA授予Zenocutuzumab(Zeno,MCLA-128)快速通道资格,用于治疗NRG1融合突变的转移性实体瘤患者。
Zenocutuzumab是一款HER2、HER3双靶点特异性抗体,能够与HER2结合,避免HER2与HER3形成异二聚体,因此能够用于治疗发生了NRG1融合突变的癌症患者。
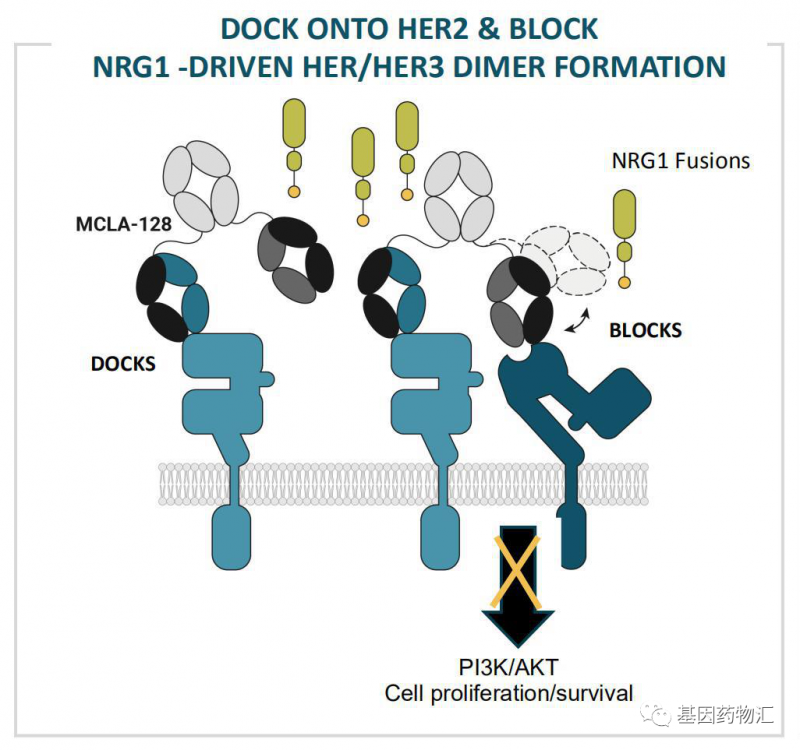
这是首款正式获得FDA认可的、用于治疗NRG1突变患者的广谱抗癌药,是一个全新靶向药物类型的重要里程碑。
该资格的授予基于Ⅰ/Ⅱ期eNRGy试验(NCT02912949)的阶段性结果。该试验中纳入的患者均为NRG1突变患者,包括胰腺癌、非小细胞肺癌及其它各类实体瘤。
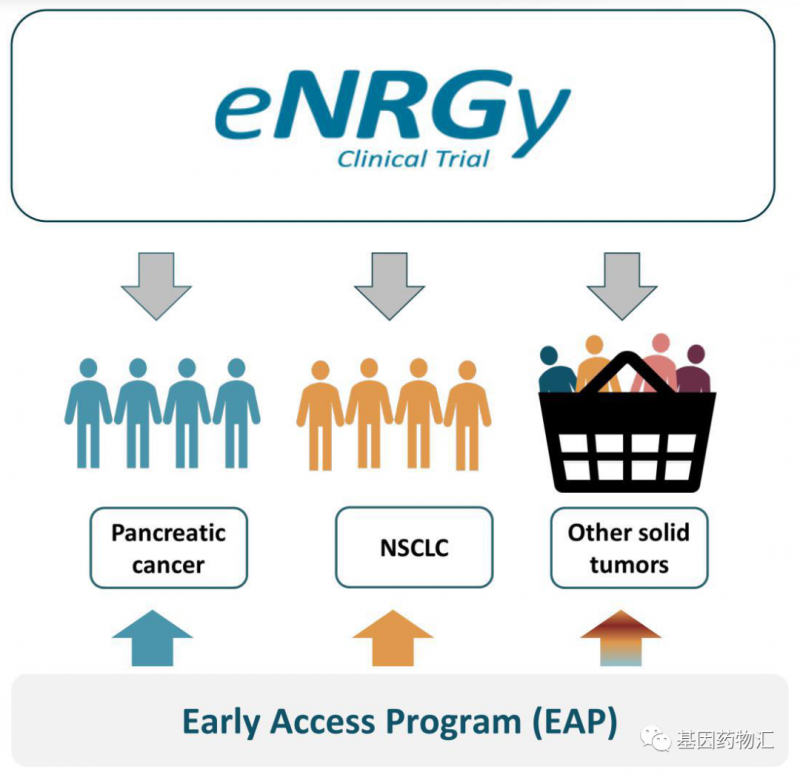
试验分组设计示意图
试验预计观察患者的缓解率、缓解持续时间及安全性和耐受性等指标,以及Zenocutuzumab的抗肿瘤活性,患者的HER2、HER3等相关标志物的水平变化。
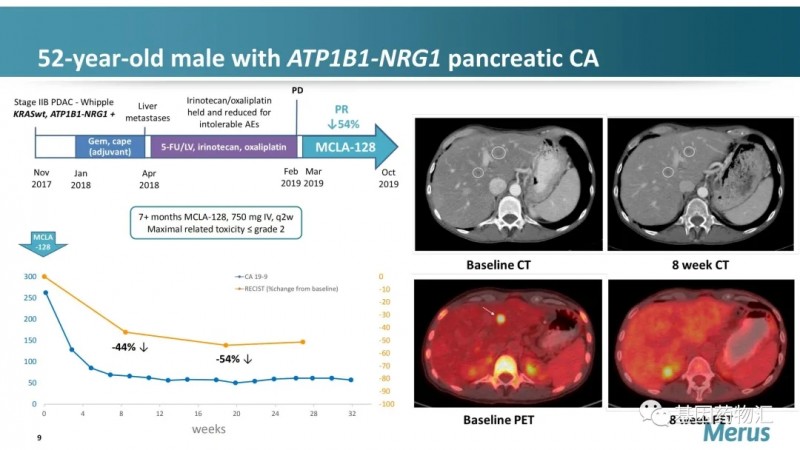
根据2019年公开的初步研究数据,3例接受了Zenocutuzumab治疗的实体瘤患者均表现出了肿瘤体积缩小。
其中,一例胰腺癌患者在接受8周的治疗后,肿瘤直径减小了44%,治疗5个月后肿瘤直径减小了54%,达到了临床部分缓解的标准。
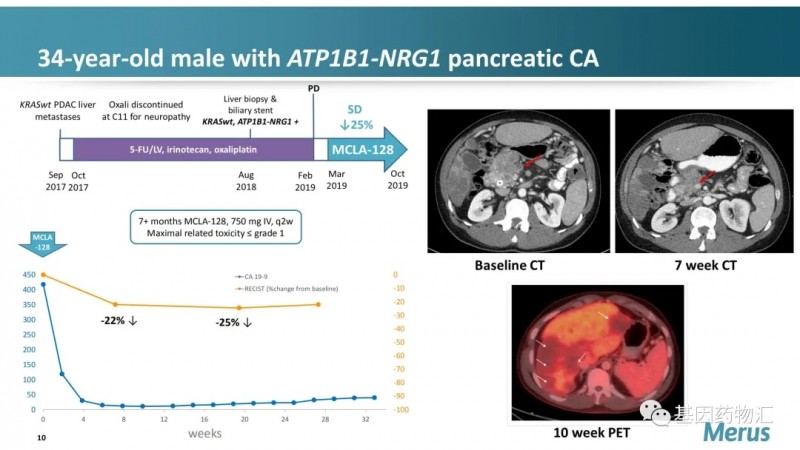
另一例胰腺癌患者在接受治疗5个月后肿瘤直径减小了25%。
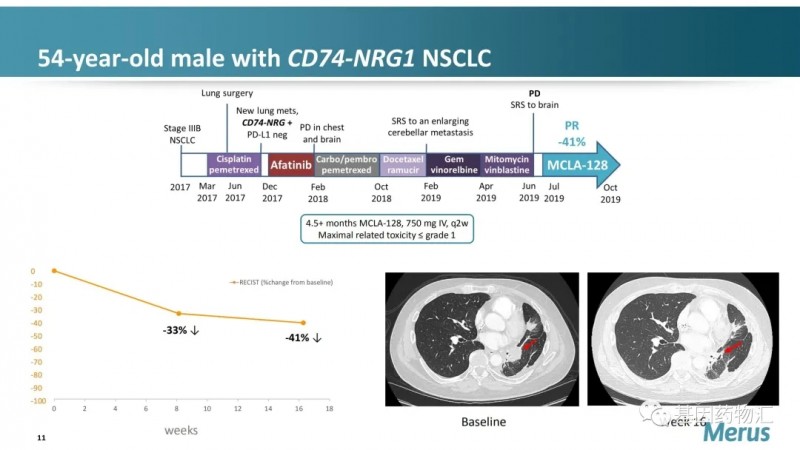
一例非小细胞肺癌患者在接受治疗5个月后,肿瘤直径减小了41%,且其基线脑转移得到了改善。这名患者已经接受过了包括阿法替尼在内的6种不同的前线方案治疗,Zenocutuzumab仍然展现出了其在末线治疗中出色的潜力。
阿法替尼:缓解率64.7%!泛HER抑制剂展现治疗潜力
对于存在NRG1融合突变的非小细胞肺癌患者来说,EGFR抑制剂的治疗效果并不理想。但进一步研究的结果仍然证实,EGFR抑制剂阿法替尼在NRG1突变的非小细胞肺癌患者的治疗中仍能取得一定的疗效。
事实上,阿法替尼不仅是一款EGFR抑制剂,同样也是一款泛HER抑制剂,对于HER家族中各类蛋白质具有比较好的抑制效果。因此,阿法替尼能够有效抑制HER2与HER3产生二聚体,从而发挥治疗效果。
在2019年AACR主办的肿瘤学创新者全球峰会上,报告者总结了迄今为止所有已经发布的病例报告及4个首次公开的病例报告的结果,并指出,在这17例NRG1融合阳性的晚期实体瘤患者(肺腺癌11例,胰腺癌3例,胆管癌1例,卵巢癌1例,结直肠癌1例)的治疗中,阿法替尼使11例患者达到了临床部分缓解,4例患者达到了疾病稳定。
新靶点与新药,共创癌症患者新希望
目前,癌症的治疗手段非常多样。最传统的手术、放疗、化疗被合称为癌症治疗的“三驾马车”,而靶向治疗,则被誉为癌症治疗的“第二次革命”。
靶向治疗为癌症患者们带来的是一次疗效与生存期的“革命”。在靶向治疗药物的帮助之下,越来越多的患者、尤其是晚期的癌症患者,活过了1年、3年、5年。
正是因此,靶向药物的研发已经成为了癌症新药研发的“重头戏”,正逐步占据着不可取代的重要地位。近年里,越来越多的靶向治疗药物投入临床,“好药”、“明星药”层出不穷,似乎正预示着一个“无化疗”时代的到来。
但与化疗不同,靶向治疗更加需要“有的放矢”,只有在患者符合一些特定的突变类型的前提之下,才能发挥出具有优势的疗效。想要真正达到化疗在癌症治疗中的地位,除了更高的缓解率、更长的生存期,靶向治疗还需提升的一个重点方面在于适应症范围。
一个全新的靶标,对于癌症患者来说就意味着一个全新的治疗希望。一名曾经没有机会接受靶向治疗的患者,很可能就能够从一款新药的治疗当中获益。
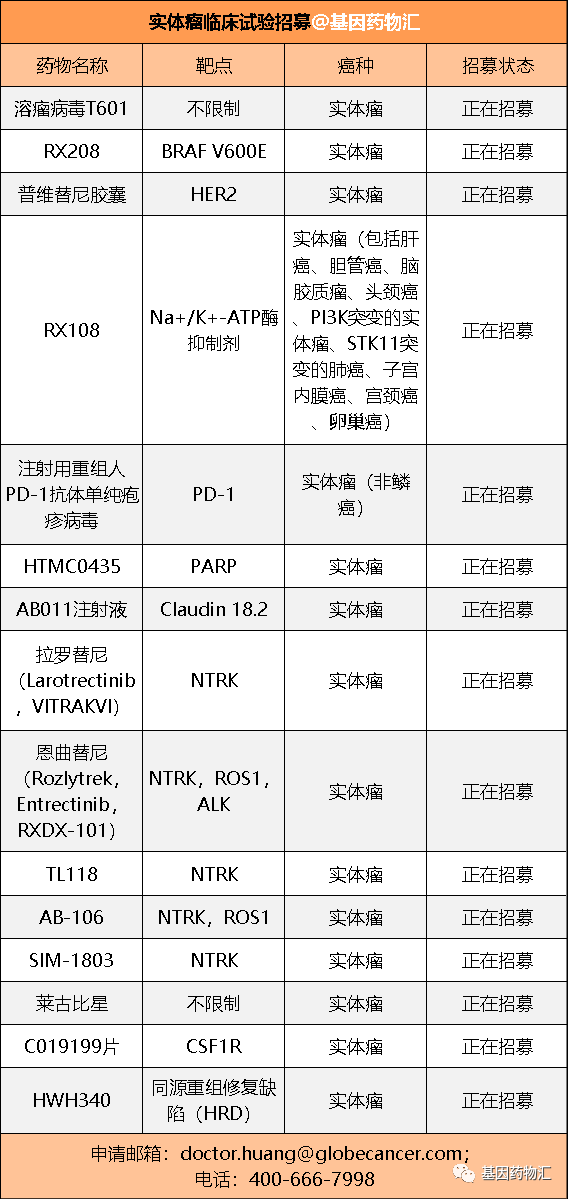
为了帮助大家更好地了解并选择临床试验项目,基因药物汇为大家整理了正在招募各类实体瘤患者的新药试验项目。药物种类很多,大家可以根据癌种及靶点进行筛选,或先行咨询、后在医学顾问的指导下选择适合自己的新药。
符合标准的患者可以将基因检测报告、诊断报告的电子版或清晰照片发送至新药招募中心邮箱(doctor.huang@globecancer.com)进行申请,邮件中留下联系方式;或联系全球肿瘤医生网医学部(400-666-7998)进行详细咨询。








































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城