CAR-T细胞治疗,CAR-T细胞免疫疗法CT041获欧洲优先药物资格,更多CAR-T临床试验招募正在进行中
刚落下帷幕的国家医保谈判中,备受各位癌友关注的“天价药”——中国首款CAR-T细胞疗法阿基仑赛注射液未进入谈判环节,这不免让众多翘首以盼希望能用上新型细胞疗法的患者很惋惜。
就在11月15日,CAR-T疗法针对实体瘤领域的进展又迎来喜讯!科济药业公告称,欧洲药品管理局(EMA)已授予自主研发的CAR-T产品CT041优先药物(PRIME)资格。CT041是一种针对 claudin18.2 蛋白 (CLDN18.2) 的自体 CAR T 细胞候选产品,用于治疗胃/胃食管交界处癌 (GC/GEJ)。据悉,入选PRIME有助于缩短药物上市时间。

值得一提的是,这是全球首个获得优先药物资格的实体瘤CAR-T产品。这意味着,CT041有望成为全球首个获批上市的实体瘤CAR-T产品,从而实现CAR-T在实体瘤领域的突破。消息一经传出,二级市场表现较为振奋,截止当日股市收盘,科济药业涨幅5.75%。
晚期胃癌的新希望!国产CAR-T疗法CT041首次亮相ESMO
嵌合抗原受体修饰T细胞(CAR-T)无疑是最令人期待的治疗手段之一。这项技术近年来在治疗各种恶性肿瘤方面取得了巨大进展,已成功应用于多种血液恶性肿瘤的治疗。
中国也终于在今年6月份也迎来了首款CAR-T疗法——阿基仑赛注射液。9月3日,中国第二款获批的CAR-T产品,也是中国首款1类生物制品的CAR-T产品——瑞基奥仑赛注射液也正式获批。
但是,全球约90%的癌症病例是实体肿瘤,CAR-T疗法在肝癌、胃癌、胰腺癌等消化系统肿瘤中虽然也取得了一定的疗效,但是少之又少,这主要是碍于靶点选择困难、CAR-T细胞进入肿瘤组织困难、CAR-T细胞进入肿瘤组织后容易被其他免疫抑制性的分子或细胞所阻挡无法发挥作用等。
因此,国内外的学者针对CAR-T进行了多种改造,不断地发现新靶点,以用于治疗多种实体肿瘤。
就在9月16~21日召开的欧洲肿瘤内科学会(ESMO)年会上,由科济药业开发的靶向Claudin18.2(CLDN18.2)自体CAR-T候选产品CT041展现了其在消化系统肿瘤中的突出疗效,可谓是大放异彩!
Claudin18.2(CLDN18.2)是一种胃特异性膜蛋白,被认为是胃癌和其他癌症类型的潜在治疗靶点。基于此,中国研究人员开发了国际上首个针对 Claudin18.2的CAR-T细胞。
此项研究为中国开展、多中心、开放标签的I期临床试验,截止到2021年4月8日,纳入的37例CLDN18.2表达阳性的晚期消化道肿瘤患者接受CT041输注并完成至少12周的评估。
其中包括28例胃癌/胃食管结合部癌、5例胰腺癌和4例其他类型的实体瘤,28例患者细胞输注剂量为2.5×108CAR-T细胞,6例患者输注3.75×108,3例患者输注5×108 CAR-T细胞。约84%的患者既往接受过至少2线治疗,中位转移器官数量为3个。
研究数据颇为亮眼
1)总疗效:所有患者的客观缓解率达48.6%,疾病控制率达73%;所有胃癌患者总客观缓解率为57.1%。
2)既往接受至少2线治疗失败的胃癌患者:客观缓解率为61.1%,疾病控制率为83.3%。
3)28例胃癌/胃食管结合部癌各亚组:在既往PD-(L)1抑制剂治疗失败、存在腹膜转移、印戒细胞癌等预后差且已无有效治疗手段的患者中,客观缓解率均可维持在50%或以上。
4)安全性:CT041总体耐受性良好,未发生治疗相关死亡或免疫细胞治疗相关神经系统毒性综合征(ICANS)。
典型病例
01、04号患者 53岁 男性
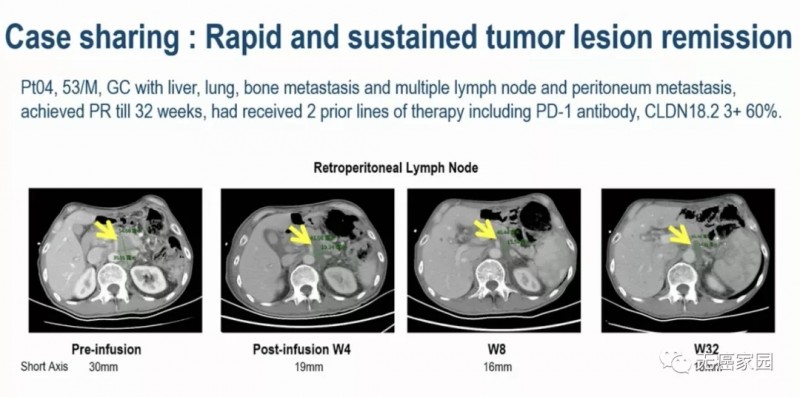
来源 CARsgen Therapeutics
晚期胃癌伴肝、肺、骨转移和多发淋巴结和腹膜转移,已接受包括 PD-1 抗体在内的2种全身治疗,CLDN18.2 60%(3+),接受CAR-T治疗后,肿瘤缩小近50%,持续缓解32周。
02、08号患者 57岁 女性
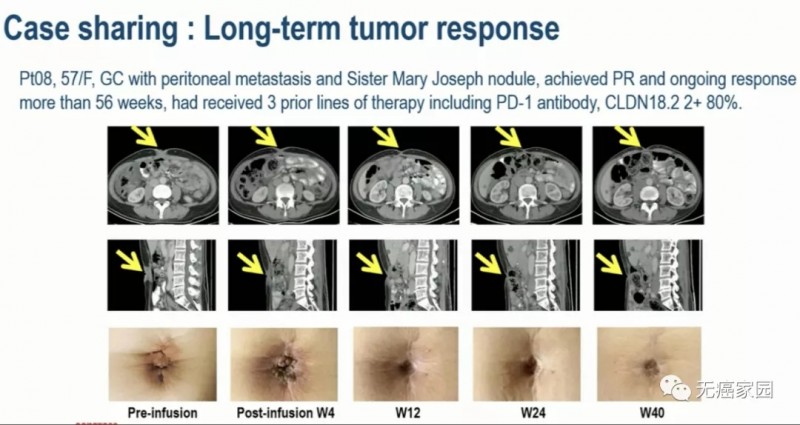
来源 CARsgen Therapeutics
GC 有腹膜转移和玛丽约瑟夫结节(恶性肿瘤转移到脐部形成的结节样病变),之前接受过3线疗包括PD-1抗体,CLDN18.2 80%(2+),接受CAR-T治疗后达到部分缓解,并且持续反应超过56周。
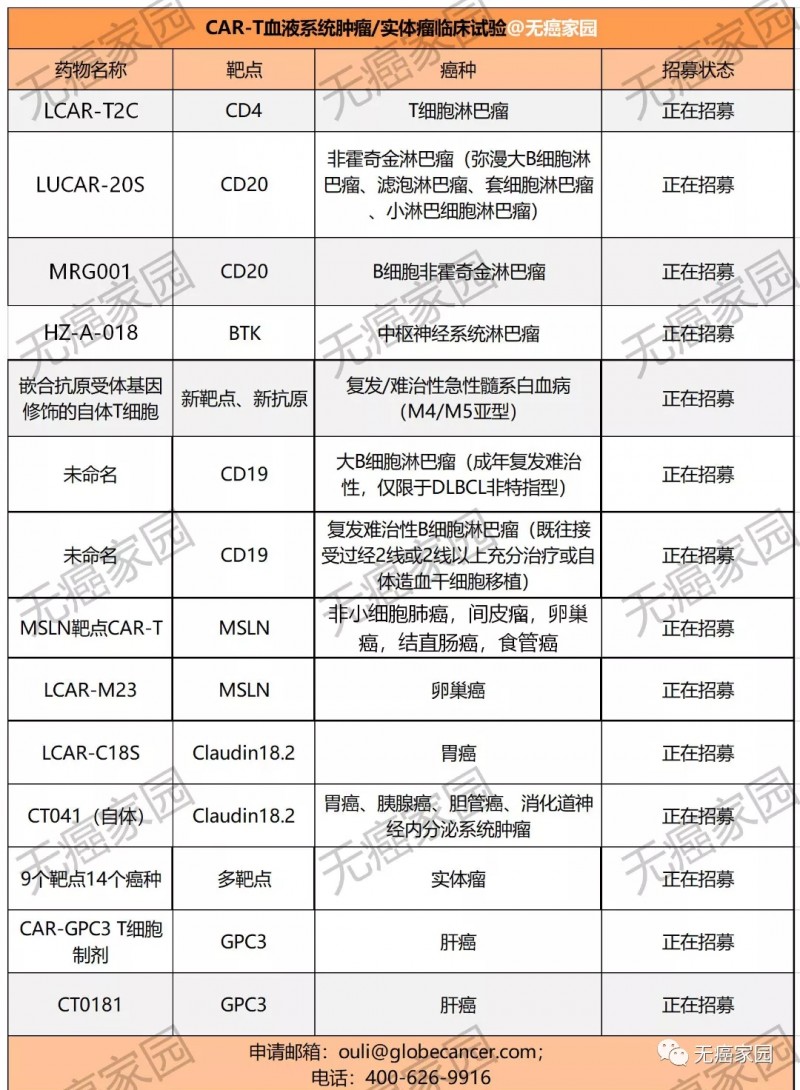
除了CT041目前正在开展临床试验外,另外一款针对既往接受过胃全切除术/胃大部切除术后的复发或转移性晚期胃腺癌(包括胃食管结合部腺癌)的靶向Claudin18.2 的CAR-T细胞制剂,名为LCAR-C18S也在临床招募中。
目前,无癌家园有多款血液肿瘤及实体瘤的CAR-T临床试验正在进行招募,有意向者可咨询医学部具体评估病情!
任重道远,CT041有望为更多实体瘤带来新的希望!未来可期!
作为国际上首个针对 Claudin18.2 的 CAR-T细胞,CT041早在2019年ASCO年会上就崭露头角,当时总客观缓解率为33.3%就已经惊艳世界,如今更加显著的疗效无疑是锦上添花!此次的临床数据展现出对消化系统肿瘤的良好治疗前景!
2020年5月,FDA批准了CT041人源化抗claudin18.2自体嵌合抗原受体CAR-T细胞用于治疗claudin18.2阳性的胃、胃食管连接处或胰腺腺癌患者的研究新药(IND)许可!
CT041为全球唯一获得IND许可的靶向CLDN18.2 CAR-T,在2020年,美国FDA授予其孤儿药认定,用于治疗胃癌/胃食管结合部癌;2021年,CT041获得欧洲药品管理局(EMA)的孤儿药认定,用于治疗胃癌。
国内药企超20多家布局CAR-T细胞疗法,中国或可弯道超车
随着阿基仑赛注射液、瑞基奥仑赛注射液在国内获批上市,CAR-T细胞疗法越来越火,让大家看到治愈肿瘤的希望,因此细胞免疫将逐步解决临床上未满足的重大需求。
据Frost&Sullivan报告显示,中国细胞免疫治疗产品市场规模2021年仅为13亿元,预计2年后涨至102亿元。
根据丁香园Insight数据库统计,国内共有24家企业布局CAR-T疗法,除复星凯特和药明巨诺外,还有传奇生物、科济生物、驯鹿医疗、西比曼生物、信达生物等。
截至目前,国内开展的CAR-T临床试验数量已经超过500项,居世界第一,这也是中国首次在一个新药研发领域走到国际前列。其中,传奇生物的西达基奥仑赛、科济药业的Claudin18.2 CAR-T都达到全球领先水平。此外,还有多公司在布局新一代CAR-T以及异体CAR-T技术,初步数据优异,有望获得全球市场。
今年我国迎来了细胞免疫治疗的元年,作为先锋的CAR-T疗法,是未来发展方向之一。CAR-T疗法主要在于改造T细胞来使其识别肿瘤细胞的特殊靶点,理论上,可以有无数种针对不同靶点的CAR-T疗法,这意味着蕴含着无限可能。
希望不久的将来,能够在国内外医学科研工作者的努力下,降低细胞疗法毒副作用,降低价格,突破实体瘤的瓶颈,让越来越多的晚期癌症患者获益!
参考文献
https://www.prnewswire.com/news-releases/carsgen-announces-car-t-cell-product-candidate-ct041-granted-prime-eligibility-by-the-ema-301424092.html








































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城