速递|靶向CD20的CAR-T疗法ADI-001治疗复发或难治性B细胞非霍奇金淋巴瘤获得FDA快速通道指定
FDA授予ADI-001快速通道资格
2022年4月19日,Adicet Bio发布的公告称,FDA已经授予其主导的细胞疗法项目ADI-001快速通道指定,作为复发或难治性B细胞非霍奇金淋巴瘤的一种潜在治疗手段。
ADI-001是一款针对CD20的CAR-T细胞免疫疗法,为同种异体CD20 CAR Vδ1 γδ T细胞疗法,目前正在Ⅰ期剂量递增试验当中接受评估,以验证ADI-001治疗B细胞非霍奇金淋巴瘤的安全性和耐受性。
截至2021年11月22日,已经有6例患者入组并接受了ADI-001的治疗,其中4例患者接受了疗效评估。3例患者达到了缓解,包括2例患者达到了临床完全缓解,以及1例患者部分缓解。
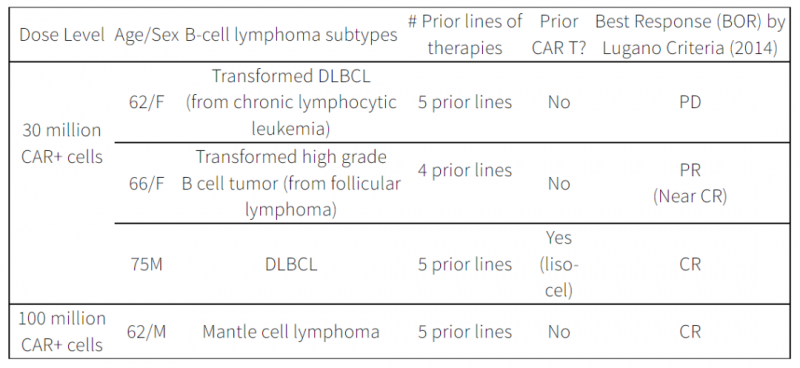
这3例达到缓解的患者当中,1例患者为弥漫性大B细胞淋巴瘤,曾经接受过5种前线方案治疗,包括2个周期的CAR-CD19-T细胞治疗;1例患者为滤泡性淋巴瘤转化为大B细胞淋巴瘤,曾经接受过4种前线方案治疗;1例患者患有套细胞淋巴瘤,并且接受过5种前线方案治疗。
至结果发布时唯一1例在治疗中进展的患者,病理类型由慢性淋巴细胞白血病转化而来,前线曾经接受过5种方案治疗。
根据Adicet Bio发布的公告,ADI-001的Ⅰ期试验预计纳入75例患有B细胞恶性肿瘤的成年患者,目前研究还在推进当中。
CD20:B细胞淋巴瘤的关键性靶标
CD20的全称是B淋巴细胞抗原CD20,这是一种在所有B细胞表面表达的抗原,从pro-B晚期开始出现,且其表达水平随B细胞的成熟逐渐上升。
目前,CD20尚无已知的配体,但在B细胞的免疫应答过程中发挥着重要的作用。有些研究推测,CD20可能是B细胞膜上一个具备钙离子通道功能的抗原。
这样的特点使CD20成为了B细胞恶性肿瘤治疗的关键性靶标。从1997年至今,已经有多款靶向CD20的药物陆续获批上市,用于各类淋巴瘤患者的治疗。其中包括第一代的利妥西单抗(Rituximab)、替伊莫单抗(Ibritumomab)及托西莫单抗(Tositumomab,已经退市),第二代的奥法木单抗(Ofatumumab)、奥瑞珠单抗(Ocrelizumab),以及第三代的阿妥珠单抗(Obinutuzumab)等。
这些药物的问世,为淋巴瘤及白血病患者的治疗开启了一个全新的局面。不过比较遗憾的是,目前获准进入中国市场的进口CD20抑制剂比较少,仅有2000年上市的利妥西单抗,绝大部分国研药物仍在临床研究阶段,国内患者的治疗选择,仍然是比较匮乏的。
根据人源化程度以及Fc片段是否经糖基化修饰,可以将目前临床上的CD20抑制剂分为三代:
01、第一代:利妥昔单抗开启B细胞淋巴瘤靶向治疗时代
全球首款CD20抑制剂利妥昔单抗于1997年正式获得FDA批准上市。这款药物于2000年获批进入中国市场,是首款也是目前唯一一款在中国上市的进口CD20抑制剂,并于2017年进入医保目录,成为了一款国内患者用得起的淋巴瘤靶向药。
利妥昔单抗属于人-鼠嵌合单抗,为第一代CD20抑制剂。与其同类的药物还包括鼠源抗体替伊莫单抗及托西莫单抗,其中托西莫单抗已经于2014年退出市场。
整体来说,第一代CD20抑制剂都属于鼠源抗体或人-鼠嵌合抗体,治疗中容易产生各类不良反应或耐药,但仍然是应用最广的一类CD20抑制剂。
02、第二代:人源化抗体问世,结构进一步优化
作为对第一代药物的优化与改善,以人源化抗体奥法木单抗为代表的第二代CD20抑制剂正式问世。
与第一代药物相比,第二代CD20抑制剂的不良反应发生率降低,但与抗原的特异性亲和力稍有下降。整体来说,同样是非常有潜力的治疗方案。
03、第三代:Fc段修饰,特异性及亲和力更强
目前已经上市的第三代CD20抑制剂为阿妥珠单抗,与利妥昔单抗同为罗氏制药研发。通过Fc段糖基化修饰,阿妥珠单抗有望获得更好的疗效,并减少不良事件的发生。
根据2013年获批时的数据,使用阿妥珠单抗联合苯丁酸氮芥治疗慢性淋巴细胞性白血病患者,中位无进展生存期23个月,显著超过了苯丁酸氮芥单药治疗的11.1个月。
抗癌"黑科技"联手CD20,带来全新希望
尽管已经有了第二代、第三代的CD20抑制剂,且市面上有了众多的仿制药及类似物、同类药,但利妥昔单抗仍然是应用最普遍的CD20抑制剂。国内也有众多CD20抑制剂的临床试验正在进行,其中包括利妥昔单抗的类似物及第二代人源化单克隆抗体等等。
不过,这一靶点的药物再次迎来一个新的“小高潮”,则是得益于细胞疗法的快速进展。
相信大家都听说过CAR-T细胞疗法。CAR的全称是嵌合抗原受体,通过在试验室中为T淋巴细胞嵌合一个抗原受体,研究者们创造出了这种同时具备靶向性以及超强攻击能力的细胞免疫疗法。
目前已经获批上市的CAR-T疗法多达5款,主要为以CD19为靶标的CAR-CD19 T细胞制剂,其最主要的特点就是缓解率超高、临床完全缓解率也超高。
而CD20则是另一个有望为B细胞淋巴瘤患者带来全新“解决方案”的热门靶点,且针对这一靶点的药物及疗法有望克服CD19抑制剂及细胞疗法耐药、复发的困境。
2021年欧洲血液学会年会上公开的CAR-CD20 T细胞疗法MB-106治疗慢性淋巴细胞白血病的整体缓解率高达92%,其中完全缓解率达到58%;治疗滤泡性淋巴瘤整体缓解率89%,其中完全缓解率为67%。
另一款已经获得了FDA授予的RMAT称号以及快速通道资格的C-CAR039则是一款CD19/CD20双靶向嵌合抗原受体-T细胞疗法,在Ⅰ期试验当中,治疗复发或难治性弥漫性大B细胞淋巴瘤患者整体缓解率高达91.7%,其中完全缓解率83.3%。
除了上述这两款疗法,针对同一靶标的国研CAR-T项目也在紧锣密鼓地进行着临床试验,均在招募各类非霍奇金淋巴瘤患者。希望了解临床试验项目详细信息,或申请参与的患者,可以联系基因药物汇。这些项目都会在国家的监管下合规谨慎地进行,是患者尝试新治疗手段很理想的渠道。







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城