胰腺癌靶向治疗,KRAS抑制剂为胰腺癌患者带来新希望
胰腺癌被人们称作“癌王”,因其超高的治疗难度以及恶性程度而令人闻风丧胆。美国国家癌症院的统计数据中,晚期胰腺癌患者的五年生存率,仅有2.9%,为常见癌症中最低。
这一次,基因药物汇将带大家一起了解一个在胰腺癌靶向治疗当中发展较快、效果比较值得期待的靶点,KRAS。
在KRAS抑制剂问世之前,临床上已经在尝试各种各样的手段治疗这类突变的患者。我们将从一些案例入手,带大家了解KRAS突变胰腺癌的各种治疗手段。
多线治疗失败,MEK抑制剂带来稳定
一位56岁的女性,于2016年10月经CT检查发现胰尾占位,侵入腹主动脉。经超声引导下活检,病历显示为腺癌,最终确诊为局部晚期胰腺癌,医生建议先行新辅助治疗。
患者从2016年10月开始接受了10个疗程的GS化疗,2017年1月的CT检查显示无法进行根治性手术,于是患者又接受了25个周期的放疗。2017年7月的疗效评估显示为部分缓解,当月,患者接受了胰脾切除手术,术中组织病理示中低分化腺癌。
患者接受了二代测序(NGS),检测到PALB2(D1168Efs*22)胚系突变和KRAS(G12R)体细胞突变。
从术后开始,2017年9月~11月,患者接受GS化疗,因肝转移而更换方案;2017年12月~2018年5月,患者接受射频消融治疗,使用了6个周期的卡培他滨+白蛋白紫杉醇化疗,但CA19-9急剧上升,且发生了转移、疾病进展。
2018年9月~2019年1月,患者接受了6个周期的伊立替康治疗,但CA19-9上升;2018年10月~2019年11月,患者使用奥拉帕利+伊立替康治疗,病情一直稳定,最后因CA19-9升高而更换方案;2019年11月,患者开始接受SOX化疗,但疾病仍然进展。
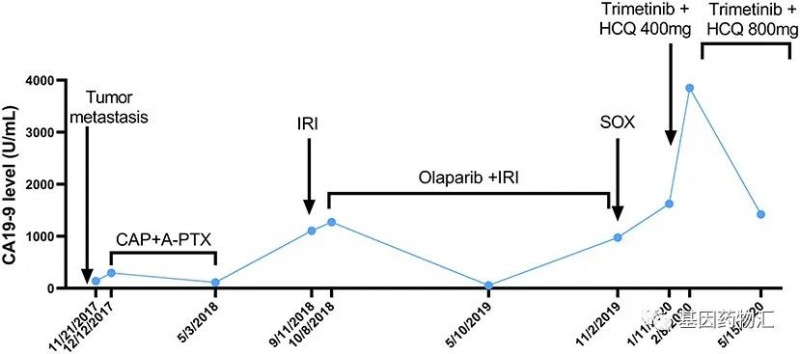
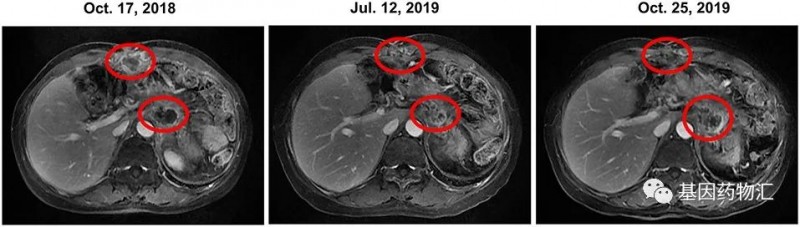
从2019年12月,患者开始接受曲美替尼(2 mg,每日一次)+羟氯喹(Hydroxychloroquine,200 mg,每日两次)方案治疗。治疗的第一个月,患者的CA19-9水平继续上升,于是将羟氯喹的剂量提升至400 mg、每天两次。此后的6个月,患者疾病一直保持稳定。
简单的KRAS介绍:关键性"枢纽"
我们常说的KRAS是一种基因的名字,属于RAS家族,而它编码合成的蛋白质名称为K-ras。在整个细胞生长的信号调控中,RAS家族基因合成的蛋白质起着枢纽的作用。
1、KRAS的上游通路
在上游,EGFR(ErbB1)、HER2(ErbB2)、ErbB3、ErbB4等位于细胞表面的受体,需要依赖RAS家族的蛋白质将外界的信号传递入细胞内。
这样的信号传递机理,导致的正是KRAS突变患者对于EGFR抑制剂原发耐药的结果。以靶向治疗为例,帕尼单抗是首款将KRAS作为预测疗效的生物标志物写入适应症当中的EGFR抑制剂。
大家可以这样理解——污染源在下游,却只治理上游;那么即使上游把水流清理得很干净,经过下游的污染源之后,最终流出来的水仍然是被污染了的。
2、KRAS的下游通路
在下游,RAS家族的蛋白质能够将信号传递给许多条重要通路,包括RAS-RAF-MEK-MAPK-PLA/ETS通路、RAS-PI3K-PDK1-AKT通路等等。
以RAS-RAF-MEK-ERK-MARP通路为例,当上游(RAS或RAF)发生突变、过表达时,阻断下游的MEK,同样可以影响整条通路的作用效果,进而抑制癌细胞的增殖。
基于这样的思路,研究者们进行了使用MEK抑制剂、PIK3CA抑制剂等药物治疗KRAS突变患者的临床试验,收获了一定的效果。
案例当中使用的曲美替尼,就是一款MEK抑制剂。这款药物在部分KRAS突变患者的治疗中有一定的疗效,ASCO大会上曾经公开了多西他赛联合曲美替尼治疗KRAS突变非小细胞肺癌患者的疗效,整体缓解率为33%,中位无进展生存期4.1个月,中位总生存期11.1个月。
KRAS抑制剂:三十年磨一剑
尽管KRAS突变的重要性一直备受关注,但相关药物以及治疗方案的研发进展一直不太理想。自从被确认为原癌突变以后的超过三十年内,KRAS抑制剂的研发都止步不前。并不是没有新药问世,只是各类新药的疗效都不尽理想,很难真正投入临床。
直到2013年,一篇刊登于Nature(《自然》)杂志上的文章,公开了被认为是将KRAS从“不可治”扭转为“可治”的颠覆性研究成果。来自加州大学旧金山分校的研究团队首次发现了KRAS突变蛋白质上能够被小分子药物结合的位点,实现了使用药物使KRAS蛋白质失活的突破。
至2019年,Sotorasib(AMG510)同样在Nature震撼登场,才向所有人证明——KRAS突变的“不可成药”终于成为了历史,KRAS抑制剂的研究终于走上了正轨。
在本年度的ASCO消化道肿瘤分会上,两款经典KRAS抑制剂分别公布了治疗包括胰腺癌在内的多类消化道癌症的最新数据。疗效刷新历史!
1、Adgrasib:疾病控制率100%
根据本年度美国临床肿瘤学会(ASCO)胃肠道肿瘤研讨会上公布的Ⅱ期KRYSTAL-1试验最新数据,Adgrasib(MRTX849)在包括胰腺癌在内的多类消化道肿瘤的治疗当中,都具有非常出色的潜力。
此次Ⅱ期试验涵盖了包括胆道癌、阑尾癌、小肠癌、胃食道结合部癌、食道癌以及胰腺导管腺癌在内的多类消化道肿瘤。目前公开了27例可评估患者的治疗结果,患者均为KRAS G12C突变的患者,先前接受过至少2种系统性抗癌治疗。
结果显示,27例可评估的患者,整体缓解率为41%,疾病控制率高达100%,即全部受试患者均达到了临床疾病稳定。
在10例胰腺癌患者当中,整体缓解率为50%,中位缓解持续时间7.0个月,中位无进展生存期为6.6个月;其它患者的整体缓解率为35%,中位缓解持续时间为7.9个月,中位无进展生存期为7.9个月。
这说明什么?显然,KRAS G12C突变的胰腺癌患者,对于Adgrasib治疗的响应率更高,响应时间也非常不错;其它消化道肿瘤的患者,响应率也不错,响应时间更长。
2、Sotorasib:控制率84.2%
同样是在本年度ASCO-GI上公布的数据,另一款经典的KRAS G12C抑制剂Sotorasib(Lumakras,AMG-510)的疗效也非常出色。
根据Ⅰ/Ⅱ期CodeBreaK100试验的数据,使用Sotorasib治疗曾经接受过大量预处理(多线治疗,其中79%的患者接受过至少2种或更多治疗)的KRAS G12C突变的局部晚期或转移性胰腺癌患者,取得了不错的疗效。
患者38例,接受Sotorasib治疗的整体缓解率为21.1%,疾病控制率为84.2%,也就是说有84.2%的患者达到了临床疾病稳定。治疗的中位缓解持续时间为5.7个月,中位无进展生存期为4.0个月,中位总生存期为6.9个月。
Sotorasib对于一部分存在多发转移的患者,同样有非常好的疗效。举例来说,一位64岁的女性患者,基线时存在肝脏、淋巴结、肺以及腹膜多个部位的转移,之前曾经接受过FOLFIRINOX方案的治疗。在接受Sotorasib治疗之前,她的肝脏上有一个直径2.2厘米的病灶;治疗18周后,病灶缩小到了0.8厘米。
在非小细胞肺癌适应症上,Sotorasib是首款获批上市的KRAS抑制剂,Adgrasib是第二款获批上市的KRAS抑制剂。而从疗效数据来看,两者当中,“后来者”Adgrasib非常有“后来居上”的势头,数据上有一定的优势。
在结直肠癌、胰腺癌以及其它各类消化道肿瘤、实体瘤的适应症上,两款药物也在暗中“较劲”,试验进度飞快推进。就目前的小型试验数据来看,两者当中Adgrasib稍有优势。但我们仍然期待更大型试验的数据,更有说服力地验证两款药物的疗效。
新药已经登陆世界多国,中国患者不用等
对于美国的患者们来说,KRAS抑制剂已经上市,新适应症的研究也已经加快步伐,用上新药的机会触手可及。但对于我国的患者们,这两款药物仍有一些遥远。
不过好在,为了进入包括中国在内的全球市场,KRAS抑制剂的临床试验项目已经在各国稳步推进。由我国自主研发的同靶点药物也已经进入了临床试验的阶段,我国患者已经有机会用上国产创新药。希望尝试新药的患者,可以联系基因药物汇获取帮助。








































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城