2022年已经获批上市的EGFR抑制剂有哪些,EGFR临床试验正在招募的有哪些
“超级响应者”,在癌症治疗当中的定义,指的是少于10%的完全缓解者,或少于10%的、持续超过6个月的部分缓解者,或缓解持续时间超过临床试验中相应药物中位缓解持续时间的3倍的患者。
每位患者都希望成为治疗当中的“超级响应者”。但在对于超级响应者的定位当中,我们的想象力还是有些拘束了——通常情况下我们期待的是完全无癌的1年,病灶缩小、不再进展的2年或者3年、5年。
一篇今年发布的,来自日本的论文当中提出了一个更大的目标——72个月之后,“生存期长尾”。
72个月之后,到长期生存
由于人种与我国相似,基于日本人群的分析数据对于我国患者是具有比较高的参考价值的。这篇文章当中着重提出了一个概念:“tail plateau”,也就是生存期图像上的“长尾”。
文章提出,图像在72个月之后趋于平稳,也就是说,能够度过72个月的受访患者,几乎都能够开启一个非常长期的、无癌的生活。
在EGFR和ALK两种驱动基因型的患者当中都能观察到这种“长尾”。EGFR突变的患者中位总生存期是36.9个月,ALK重排阳性患者的中位总生存期是55.4个月;不论是那类患者,生存期的曲线在72个月之后都趋于平稳,“大多数在5年后仍然或者的患者,都在继续接受治疗”。
其中的EGFR,是非小细胞肺癌最常见的驱动基因之一。
为什么我们要关注EGFR
我们先来看几组数据
2020年,世界癌症死亡患者数量995.8万,新发癌症数量1929.3万,这两个数字之间的比值(死亡率与发病率比值,能够反应疾病的临床预后)是0.516;
2020年,中国癌症死亡患者数量300.3万,新发癌症数量456.9万,这两个数字之间的比值是0.657;
2020年,世界肺癌死亡患者数量179.6万,新发患者数量220.7万,这两个数字之间的比值是0.814;
2020年,中国肺癌死亡患者数量71.5万,新发患者数量81.6万,这两个数字之间的比值是0.876。
死亡率与发病率比值,计算时采用新发癌症病例总数与死亡人数计算比值,这个数值能够反应疾病的临床预后情况。整体来说,我国的癌症患者预后稍微低于世界平均水平;但是在肺癌这个单项上,我国患者的预后竟然已经基本与世界平均水平持平了!
这是为什么呢
大约85%~90%的肺癌分型属于非小细胞肺癌,其中肺腺癌的占比又有约60%~70%,可以说是肺癌当中占比最大的一个群体。
我们常说不同国家、不同地区、不同人种的群体,罹患的癌症也有一定的差别,有独特的流行病学特征。举例来说,美国肺腺癌患者的EGFR突变率稍高于10%,而中国肺腺癌患者的EGFR突变率超过60%!
恰好EGFR抑制剂的研究成果也是非常丰富的,药物众多,疗效出色。这也不意外,很多专家将针对EGFR这个突变和对应的靶向治疗药物EGFR抑制剂,称作是“上帝送给东方人的礼物”。
别的不说,对于EGFR突变患者们,当年力排众议、坚持将易瑞沙(吉非替尼)引入中国并进行临床试验、后续推动其进入医保的吴一龙教授,肯定是一位当之无愧的“救命恩人”。
从2005年吉非替尼在中国获批至今,EGFR突变非小细胞肺癌的一线治疗已经迎来了不止一次的更新。这一次,我们以EGFR突变非小细胞肺癌的治疗为主题,为这部分患者们提供一些有价值的“解决方案”。
目前已经获批的EGFR抑制剂
目前临床上已经上市的EGFR抑制剂(EGFR-TKI)可以分为四类:以吉非替尼为代表的第一代EGFR抑制剂,以阿法替尼为代表的第二代EGFR抑制剂,以奥希替尼为代表的第三代EGFR抑制剂,和以阿米万他单抗为代表的EGFR/MET双靶点抑制剂(根据适应症可分入第四代EGFR抑制剂)。
1、第一代TKI
关键词:可逆性结合,有一定的入脑性,耐药风险高
获批药物:厄洛替尼,吉非替尼,埃克替尼
最初,科学家发现部分非小细胞肺癌的癌细胞中EGFR蛋白表达水平远高于正常细胞,并以此为突破口研发了第一代EGFR抑制剂。从首款EGFR-TKI吉非替尼于2003年获得FDA批准上市至今,已获得FDA批准上市的一代EGFR抑制剂包括厄洛替尼、吉非替尼和埃克替尼。
这类药物的共同点在于,化学结构上有相同的喹唑啉母环,主要通过与ATP竞争性结合的方式,抑制发生了细胞的EGFR蛋白功能,主要针对19号外显子缺失和21号外显子点突变。
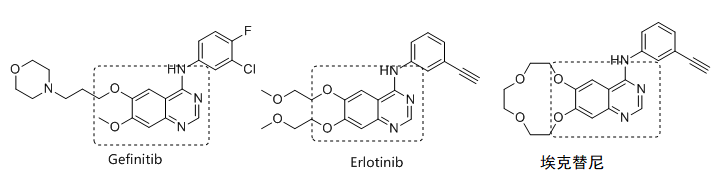
除了发生突变的细胞,一代EGFR抑制剂也同样会抑制正常细胞的EGFR蛋白功能,从而导致皮疹、腹泻等不良反应。此类药物入脑性较差,对于脑转移患者的疗效整体不佳。由于药物与靶点的结合方式为可逆性结合,一代EGFR抑制剂发生耐药的风险较大,通常发生在在连续用药1年左右。最常见的耐药突变为T790M突变型。
2、第二代TKI
关键词:不可逆结合,更好的疗效,更低的耐药风险
获批药物:阿法替尼,达克替尼
与一代药物不同,二代EGFR抑制剂对于药物化学结构做出了改进,除竞争性地与EGFR上ATP结合位点可逆地结合外,还能与EGFR特有的氨基酸残基发生烷基化作用或共价键结合,即不可逆的结合。目前,获得FDA批准上市的二代EGFR抑制剂包括阿法替尼和达克替尼两款。
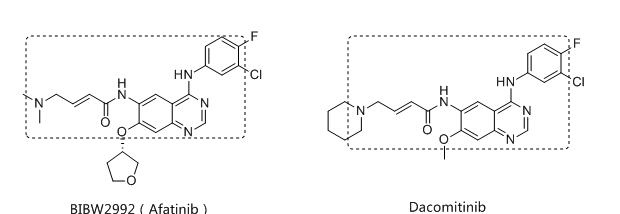
2016年ESMO大会上,全球首次一代与二代EGFR抑制剂吉非替尼和阿法替尼的头对头对比试验LUX-Lung 7公布了初步研究的数据。这是一二代EGFR抑制剂的首次正面“交锋”,显然,二代药物阿法替尼先下一局。
LUX-Lung 7的初步结果显示,接受二代EGFR抑制剂阿法替尼治疗的患者中位总生存期为27.9个月,接受一代EGFR抑制剂吉非替尼治疗的患者中位总生存期为24.5个月;阿法替尼治疗患者中位治疗失败时间为13.7个月,而吉非替尼治疗患者的中位治疗失败时间为11.5个月,显然接受阿法替尼治疗的患者治疗有效、疾病控制良好的时间整体更久。
除此以外,阿法替尼在部分非敏感突变、也就是EGFR外显子19缺失(ex19del)和L858R突变以外的各类突变亚型当中的疗效,是要强于第一代药物的。一些研究认为,阿法替尼能够降低患者的TMB,尤其在TMB较高的EGFR突变(例如外显子20插入突变ex20ins)患者当中治疗潜力强于其它的EGFR抑制剂。
与一代药物相比,二代EGFR抑制剂在避免耐药方面做出了卓有成效的努力。二代EGFR抑制剂的开发逻辑是,如果药物的疗效更好,或许耐药性会出现得更晚、甚至不会发生耐药。因此,二代EGFR抑制剂采取的是不可逆的共价结合方式,临床中展现出了更强的抑制作用,但仍然不能用于治疗一代EGFR抑制剂后发生耐药突变的患者,如T790M突变型患者等。
在这样的迫切需求之下,三代EGFR抑制剂应运而生。
3、第三代TKI
关键词:一二代耐药,更好的疗效,更少的不良反应
获批药物:奥希替尼,阿美替尼(国产),伏美替尼(国产)
2015年,FDA批准了首款三代EGFR抑制剂奥希替尼,填补了长期以来一二代EGFR抑制剂耐药后的治疗困境。除了靶向最常见的耐药突变T790M,奥希替尼对于常见的EGFR突变类型,如外显子18、19、21的突变型,均有很好的治疗效果。此外,奥希替尼具有良好的选择性,对于未发生突变的野生型EGFR蛋白作用效果弱,脱靶毒性更小,造成的不良反应更轻微。当然,比起一代EGFR抑制剂,奥希替尼还有非常重要的一点优势,即奥希替尼的入脑性更强,对于发生了脑转移的患者同样具有较好的疗效。
除奥希替尼以外,几款国产的第三代EGFR抑制剂,如已经获批的伏美替尼和阿美替尼等,疗效都与奥希替尼相仿。
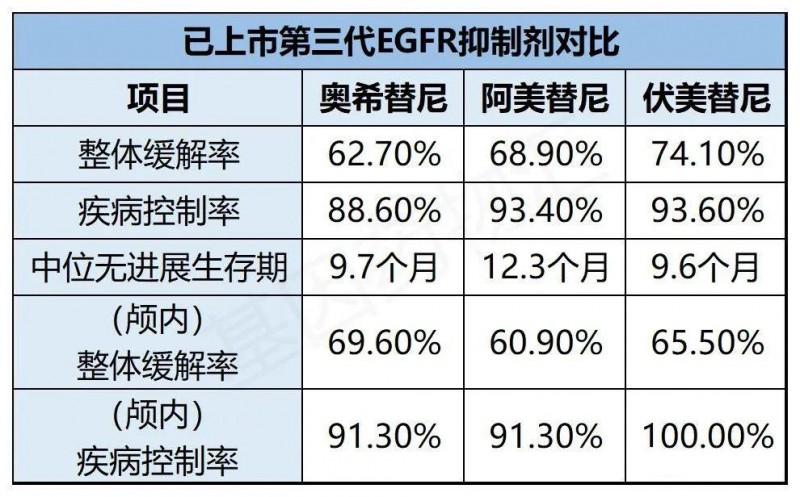
用于治疗第一、二代EGFR抑制剂耐药的T790M突变疾病时,这三款药物的缓解率都能够达到60%~70%以上,疾病控制率在90%左右,且颅内病灶的缓解率都在60%以上。
此外,这三款药物都完成了在一线治疗环境下与吉非替尼的“头对头”对比试验,疗效上有非常明显的优势。再加上同样完成了对比试验的阿法替尼,疗效总结如下:
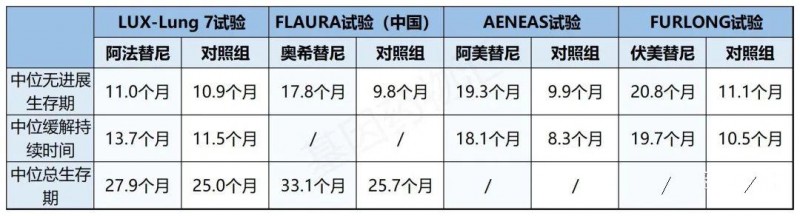
当然,由于试验的患者人群可能存在一定的差距,最终的疗效也可能存在一定的偏差(例如经常有外国专家提出,当中国[亚洲]患者占比较高的时候,EGFR抑制剂的疗效可能会较好等)。所以几款药物的疗效仅能作为参考,不能进行横向对比。
但从这两组数据当中我们也可以看出,国产的EGFR抑制剂、尤其是国产的新一代EGFR抑制剂已经有了不输奥希替尼的出色潜力。获批上市以及走入临床试验阶段的第三代EGFR抑制剂越来越多,尽管仍有很多不可替代之处,但奥希替尼终于不再是“一枝独秀”了。
4、EGFR/MET双靶点抑制剂
关键词:罕见突变亚型,奥希替尼耐药,共突变
获批药物:阿米万他单抗
阿米万他单抗,也就是我们熟知的JNJ-6372,为EGFR抑制剂的发展打开了一个全新的思路。这款药物首先获批的适应症是罕见突变EGFR ex20ins,随后又在奥希替尼耐药的患者当中展现出了卓越的疗效,拓宽了第四代EGFR抑制剂的新思路。当然,还有一点非常值得关注:作为一款双靶点抑制剂,阿米万他单抗在双突变的患者当中,同样有望展现出一定的治疗效果。这款药物的另一个靶点,MET,是很多EGFR抑制剂的耐药突变之一。因此,同时存在EGFR与MET异常的患者,完全有可能使用它作为新的治疗手段。
正在研究当中的EGFR抑制剂
正在进行研究或临床试验的EGFR抑制剂,主要分为3个类型:效仿或试图超越奥希替尼的第三代EGFR抑制剂,治疗奥希替尼耐药患者的第四代EGFR抑制剂,以及针对罕见靶点的EGFR抑制剂。
第三代EGFR抑制剂暂不表。第四代EGFR抑制剂当中,部分药物发展较快,如BBT-176(当前小型试验当中,接受治疗的患者病灶缩小30%~51%)等;还有一些国产药物也在进行临床试验。
能够用于罕见或难治EGFR突变亚型(包括ex20ins)的药物,又分为至少3类:
以阿米万他单抗(Amivantamab,JNJ-6372)为代表的EGFR/MET双特异性抗体,与几款经典的EGFR抑制剂有很大不同。目前的机理还需要进一步研究,但从疗效上来说,阿米万他单抗对于ex20ins突变的非小细胞肺癌有更好的治疗效果。
另一类以莫博替尼(Mobocertinib,TAK-788)为代表,在结构上与奥希替尼有相似之处,但增强了针对EGFR ex20ins以及其它非敏感突变的抑制效果,同时对HER2外显子20插入突变的肺癌也有一些抑制效果(因为这两类插入突变的结构有相似之处)。
还有一类是经过了优化,与现有的EGFR抑制剂都有结构上的不同的新药。由于其结构上的特点,这类药物与现有的第一至第三代EGFR抑制剂不存在交叉耐药,有潜力用于多类EGFR耐药突变、难治突变的患者,适应症范围更加广泛。
小汇有话说
上文中提到的3类在研EGFR抑制剂,均有新药在进行临床试验。有需求尝试新药的患者,可以咨询基因药物汇了解项目详细招募标准,或提交病历资料,申请接受入组评估。
文首的日本研究当中,同样还指出了一件事:大部分患者,并不是依靠某一款药物获得长生存期的。他们中多数都是依靠多款药物的配合,联合用药或序贯用药,才最终得到了如此长的生存期。
在EGFR突变患者中,37位患者从首次接受治疗以来存活了5年以上。其中仅有5名患者,只使用了一种EGFR抑制剂方案;2位患者使用了2种EGFR方案;其他患者都是用了多种药物的方案,不仅有EGFR抑制剂,还有化疗药物或免疫治疗方案。当然,发挥最主要疗效的还是EGFR抑制剂。







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城