2022年10月28日中国首个M-CTL细胞疗法KACM001自体淋巴细胞注射液新适应症申报被受理
2022年10月28日,据国家药监局药品审评中心(CDE)官网显示,北京康爱瑞浩生物科技股份有限公司(以下简称:康爱生物)自主研发的KACM001自体淋巴细胞注射液产品新适应症申报获得受理(受理号:CXSL2200546)。

截图源自NMPA官网
此次KACM001细胞注射液申报新适应症是康爱生物细胞治疗创新药研发路上的重要里程碑,意味着其在细胞治疗领域取得了突破性进展,开启了未来的高速发展之路。
早在今年5月份,KACM001自体淋巴细胞注射液产品(受理号:CXSL2200052)已正式获得国家药品监督管理局(NMPA)的临床试验默示许可,拟联合替吉奥/奥沙利铂或顺铂治疗局部晚期不可切除或转移性胃癌。
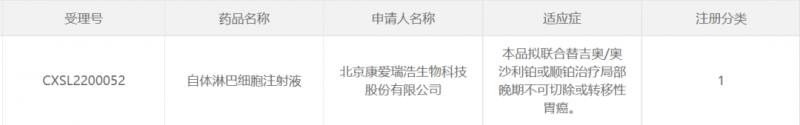
截图源自NMPA官网
KACM001是康爱生物自主研发,具有独立知识产权的自体淋巴细胞注射液,同时也是目前国内首个联合一线治疗方案,针对实体肿瘤治疗的1类新药,针对晚期不可切除/转移性胃癌。
KACM001注射液实际上就是该公司的MTCA-CTL(多靶点复合抗原细胞毒性T细胞)产品。CTL(cytotoxic T lymphocytes)技术,即细胞毒性T淋巴细胞。该技术主要是利用癌细胞特有的、正常细胞上没有或者含量很低的蛋白质做诱饵,把外周血中那“万里挑一”的真正能抗癌的淋巴细胞,挑选出来,然后在体外进一步改良和扩增,然后回输给患者。
MTCA-CTL免疫疗法是国内推出的新一代生物免疫治疗模式。在保证非MHC限制性杀伤性NK-T细胞扩增的同时,定向扩增MHC限制性的CD8+特异性CTL细胞,使其在细胞产品中的比率可达到60%~70%。这种杀伤细胞的共同作用,使杀伤肿瘤细胞的效率更高。
目前正在中国医学科学院肿瘤医院进行二期临床试验的多靶点复合抗原肽生物免疫治疗技术,是第五代也是全新一代细胞免疫治疗技术,可优化DC(树突细胞)活化方法,以增强免疫细胞对肿瘤细胞的杀伤作用,目前已取得很好的临床效果,相信将真正的让癌症患者受益。
【主要适用于实体肿瘤】头颈部肿瘤、食道癌、肺癌、胃癌、乳腺癌、肝癌、膜腺癌、结亘肠癌、卵巢癌、子宫癌、彗癌、前列腺癌、恶性黑色素瘤、肉瘤、部分恶性淋巴瘤。
若经济条件允许且想咨询MTCA-CTL疗法可联系无癌家园医学部,详细评估病情。








































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城