基于独立终点审核委员会(IRC)评价的无进展生存期(PFS),评估ARX788相较于拉帕替尼联合卡培他滨治疗 HER2 阳性局部晚期或转移性乳腺癌的有效性。

确诊的晚期肝细胞癌受试者,既往至少接受过一种PD-1/PD-L1单克隆抗体免疫治疗以及分子靶向药物治疗(索拉非尼,瑞戈非尼,仑伐替尼等)和/或一种抗血管生成药物(如贝伐珠单抗)治疗后进展或不耐受。
评估 D-1553 在 KRASG12C 突变的晚期或转移性实体瘤受试者中的安全性和耐受性。
评价HA121-28片在晚期胆道恶性肿瘤受试者中的临床疗效。

本研究旨在评估 tepotinib 联合奥希替尼以及 tepotinib 单药治疗在具有EGFR活化突变且经一线奥希替尼治疗后由于 MET 扩增而复发的晚期或转移性非小细胞肺癌患者中的抗肿瘤活性、安全性、耐受性和药代动力学特征。
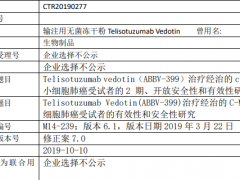
本项研究的主要目的是确定 telisotuzumab vedotin 在 c-Met+ NSCLC 受试者中的总缓解率(ORR)。
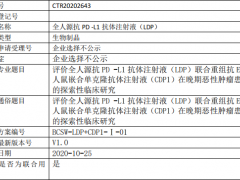
评估 LDP 联合 CDP1 治疗晚期恶性肿瘤患者的安全性,确定临床试验推荐剂量。
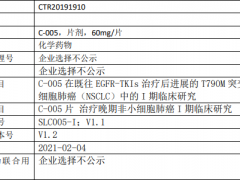
评价 C-005 在既往使用一代或二代 EGFR-TKI 耐药后产生 T790M 突变的晚期 NSCLC 患者的安全性和耐受性;确定 C-005 在携带 EGFR 突变的局部晚期或转移性 NSCLC 患者的 MTD(剂量递增阶段),及在确定的推荐剂量水平上的疗效(扩大入组阶段),为后续的临床试验给药剂量提供依据。
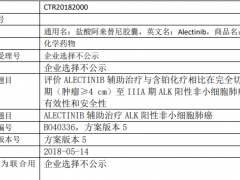
评价 alectinib 与含铂化疗相比,在完全切除的 IB 期(肿瘤≥4 cm)至 IIIA期间变性淋巴瘤激酶阳性非小细胞肺癌(NSCLC)患者中的有效性和安全性。
在肿瘤携带 EGFR 20 号外显子插入突变的局部晚期或转移性 NSCLC患者中比较 TAK-788 作为一线治疗与含铂化疗的疗效,由设盲的独立审查委员会(IRC)根据实体瘤疗效评价标准(RECIST)1.1 版评估的无进展生存期(PFS)证实。