时间:2018-12-18 10:59 编辑:全球肿瘤医生网
KEYTRUDA是一种抗PD-1疗法,通过增强身体免疫系统帮助检测和对抗肿瘤细胞的能力起作用。KEYTRUDA是一种人源化单克隆抗体,可阻断PD-1与其配体PD-L1和PD-L2之间的相互作用,从而激活可能影响肿瘤细胞和健康细胞的T淋巴细胞。
制药巨头默沙东(MSD)昨日宣布欧盟委员会(EC)批准KEYTRUDA(pembrolizumab,派姆单抗,K药),该公司的抗PD-1疗法,用于辅助治疗患有III期黑色素瘤和淋巴结转移且已经完全切除的成人患者。该批准基于与欧洲癌症研究和治疗组织(EORTC)合作进行的关键性III期EORTC1325 / KEYNOTE-054试验的数据。数据分析表明,KEYTRUDA显着延长了RFS。在III期高危黑色素瘤切除人群中,对比安慰剂组,降低疾病复发和死亡风险44%。
研究实验室临床研究副总裁Scot Ebbinghaus博士说: 默克公司对黑色素瘤患者的长期承诺包括特别关注在治疗范例早期为这些患者提供新的治疗选择。这项批准是KEYTRUDA在欧盟辅助治疗中的首次批准,建立在KEYTRUDA在晚期和转移性黑色素瘤环境中建立的基础之上。
该批准更新了KEYTRUDA在所有28个欧盟成员国以及冰岛,列支敦士登和挪威的用药新指导,以每三周200mg的批准剂量,直至疾病复发,不可接受的毒性或持续长达一年。KEYTRUDA在欧洲也被批准用于治疗成人晚期(不可切除或转移性)黑色素瘤的单一疗法。
黑色素瘤患者,特别是那些患有III期疾病的患者,往往具有高复发风险,EORTC和Merck的合作研究表明,手术后癌症复发的风险显着降低,研究主席Alexander Eggermont博士说,他是巴黎-萨克莱大学肿瘤学教授。 这种辅助治疗方案的批准标志着治疗黑色素瘤的另一个重要里程碑。
支持批准的数据
该批准基于EORTC1325 / KEYNOTE-054试验的数据,这是一项由Merck赞助并与EORTC合作进行的第III阶段,多中心,随机,双盲,安慰剂对照研究。根据美国癌症联合委员会(AJCC)第 7期,该研究正在评估使用KEYTRUDA与安慰剂治疗完全切除的黑色素瘤患者(IIIA期[ 1 mm淋巴结转移],IIIB或IIIC)的辅助治疗版)。总共,该研究招募了1,019名成年患者,他们被随机分配(1:1),每三周静脉输注KEYTRUDA 200 mg(n = 514)或安慰剂(n = 505),持续长达一年,直至疾病复发或不可接受的毒性。共同主要终点是所有患者的RFS和肿瘤表达PD-L1的患者的RFS。无复发生存率定义为从随机治疗开始到首次复发日期(局部,区域或远处转移)或死亡的时间。
在的数据分析中,与EORTC1325 / KEYNOTE-054试验中断的初始数据相比,另外7个月的随访,KEYTRUDA显着延长了RFS,将疾病复发或死亡的风险降低了44%。在整体意向治疗人群中,KEYTRUDA组的12个月RFS率为76%,安慰剂组为61%。在18个月时,RFS率分别为72%和54%。
基于先前报道的最终RFS分析,对于PD-L1阳性肿瘤患者(n = 853)的RFS共同主要终点,KEYTRUDA证实RFS显着延长,导致复发或死亡风险降低46%。KEYTRUDA组的6个月RFS率为84%,安慰剂组为75%。除了对肿瘤表达PD-L1的患者进行分析外,还对肿瘤为PD-L1阴性,BRAF突变阳性或BRAF突变阴性的患者进行了预定义的亚组分析,并根据分期进行。无论BRAF突变状态,PD-L1状态如何,都证明了RFS的益处。
在BRAF阳性肿瘤患者(n = 507)中,KEYTRUDA组的6个月RFS率为83%,安慰剂组为73%,RFS显着更长,复发或死亡的风险降低51%。使用KEYTRUDA单一疗法证实这种RFS益处在BRAF阴性肿瘤患者中是一致的。
KEYTRUDA作为单药治疗的安全性已在4,948例患者中进行了评估,包括晚期黑色素瘤,已切除III期黑色素瘤(辅助治疗),非小细胞肺癌,经典霍奇金淋巴瘤,尿路上皮癌或头颈部鳞状细胞癌(研究四种剂量:每3周2 mg / kg,每3周200 mg,或每2或3周10 mg / kg)。在该患者人群中,中位观察时间为7.3个月,KEYTRUDA最常见的不良反应为疲劳(34.1%),皮疹(22.7%),恶心(21.7%)和腹泻( 21.5%)和瘙痒症(20.2%)。单药治疗报告的大多数不良反应均为1级或2级严重程度。
派姆单抗获批适应症大盘点
①黑色素瘤
a) 用于治疗患有不可切除或转移性黑素瘤的患者
b) 用于辅助治疗患有III期黑色素瘤和淋巴结转移且已经完全切除的成人患者(新增)
②肺癌
a) 接受一线TKI治疗失败后/一线化疗后的PD-L1阳性的转移的非小细胞肺癌患者
b) 一线治疗PD-L1表达50%且EGFR、ALK阴性的非小细胞肺癌患者
c) 联合培美曲塞、卡铂一线治疗非鳞非小细胞肺癌患者
d) 联合卡铂、紫杉醇/白蛋白紫杉醇一线治疗鳞状非小细胞肺癌
③头颈癌
适用于治疗铂类耐药复发性或转移性头颈部鳞状细胞癌(HNSCC)的患者。
④经典霍奇金淋巴瘤
适用于治疗患有难治性经典霍奇金淋巴瘤(cHL)的成人和儿童患者,或者在3线或更多治疗后复发的患者。
⑤原发性纵隔大B细胞淋巴瘤
适用于治疗患有难治性原发性纵隔大B细胞淋巴瘤(PMBCL)的成人和儿童患者,或者在2线或更多线治疗后复发的患者。KEYTRUDA不建议用于需要紧急细胞减灭治疗的PMBCL患者。
⑥尿路上皮癌
a)用于治疗局部晚期或转移性尿路上皮癌(mUC)患者,不符合顺铂化疗的条件,其肿瘤表达PD-L1 [综合阳性评分(CPS)10],由FDA确定批准的测试,或不符合PD-L1状态也不适用铂类化疗的患者。
b)适用于治疗患有局部晚期或转移性尿路上皮癌(mUC)的患者,这些患者在含铂化疗期间或之后或在含有铂的化学疗法的新辅助或辅助治疗的12个月内疾病进展。
⑦微卫星不稳定性-高(MSI-H)实体瘤
适用于治疗无法切除或转移性微卫星不稳定性(MSI-H)或错配修复缺陷(dMMR)的成人和儿童患者:
a)经前线治疗失败且无有效替代疗法的实体瘤,包括结直肠癌、小肠肿瘤、肉瘤、子宫内膜癌、乳腺癌、甲状腺癌、腹膜后腺癌、胃癌、食管癌、小细胞肺癌、胰腺癌、前列腺癌、肾细胞癌。
b)或用氟嘧啶,奥沙利铂和伊立替康治疗后进展的结直肠癌。
c)在患有MSI-H中枢神经系统癌症的儿科患者中的安全性和有效性尚未确定。
⑧胃癌
用于治疗复发性局部晚期或转移性胃或胃食管连接(GEJ)腺癌的患者,其肿瘤表达PD-L1 [综合阳性评分(CPS)1],由FDA批准的测试确定。在包括含氟嘧啶和铂的化学疗法,或者HER2 / neu靶向疗法两线或多线治疗后进展。
⑨宫颈癌
适用于治疗复发或转移性宫颈癌患者,化疗期间或之后疾病进展,其肿瘤表达PD-L1(CPS1),由FDA批准的测试确定。
⑩肝细胞癌
适用于治疗曾接受过索拉非尼治疗的肝细胞癌(HCC)患者。
中国购买信息
7月25日,派姆单抗在中国上市!成为了继百时美施贵宝的Opdivo(O药,也叫纳武单抗)(6月上市)之后第2个正式在中国上市的PD-1/PD-L1单抗类药物。此次在中国上市的K药,仅仅是针对晚期恶性黑色素瘤,它也是目前中国唯一获批的针对这个患者群体的免疫治疗药物,国内的患者不用再到境外买药了。
那么派姆单抗在中国售价为多少呢?据了解,售价显着低于海外,仅为美国一半。
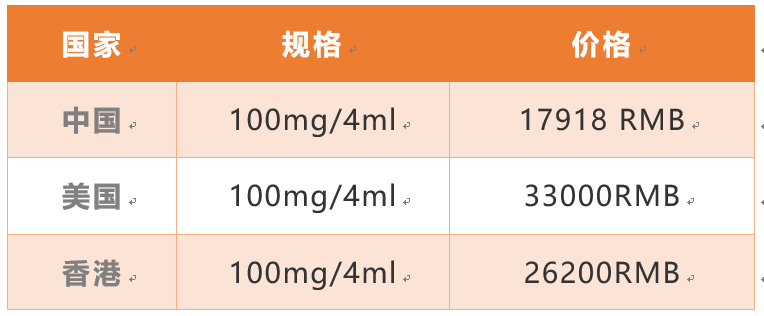
所以,派姆单抗在国内的售价只有美国的54%,香港的68%,应该算是全球比较低的价格了。全球肿瘤医生网抗癌咨询电话.
本网站新闻资讯、文章、研究数据、治疗案例均来自于国内外医学论文,所涉及到的新药、新技术有可能还处于临床研究阶段,患者不能作为治疗疾病的依据。癌症治疗目前尚无治愈手段,患者需要在医生的指导下,在医院接受正规治疗或参加新药新技术临床试验。