全球肿瘤医生网提醒患者:国内细胞免疫治疗技术,包括cart细胞,树突细胞疫苗,NK细胞,TILs细胞,TCR t细胞治疗,癌症疫苗等技术均处于临床试验阶段,未获准在医院正式使用。国内患者可以参加正规临床试验,在医生的监管下使用,全球肿瘤医生网不推荐患者贸然尝试任何医疗机构和研发机构的收费治疗。
17年8月30日,杨森公司宣布 CFDA 批准依鲁替尼胶囊,用于单药治疗既往至少接受过一种治疗的慢性淋巴细胞白血病(CLL)/ 小淋巴细胞淋巴瘤(SLL)、套细胞淋巴瘤患者。
依鲁替尼是全球第一个上市的 BTK 抑制剂,由强生和 Pharmacyclics 合作开发,最早是于 2013/11/13 获得 FDA 批准上市,上市之后销售额突飞猛进,由此也引起了 AbbVie 的巨大兴趣。AbbVie 于 2015 年 3 月斥资 210 亿美元重金收购了 Pharmacyclics,获得了依鲁替尼的美国市场商业权利。强生则拥有依鲁替尼在全球其他国家的商业权利。2016 年强生和 AbbVie 合计销售收入 30.83 亿元,2017 上半年,强生和 AbbVie 合计销售收入 20.36 亿美元。
强生最早于 2013/9/6(CDE 承办时间)在中国提交了依鲁替尼的注册申请,2016/11/ 7 提交了生产申请,2016/12/ 2 获得以与现有治疗手段相比具有明显治疗优势的理由被 CDE 纳入优先审评,2017/8/28 获得 CFDA 颁发的生产批件。依鲁替尼在中国上市申请的整个审评周期大约 10 个月,最终上市时间比美国晚了大约 4 年。
ASH2016 大会上曾公布过依鲁替尼的两项 5 年随访研究结果,均显示 CLL/SLL 患者越早使用依鲁替尼,生存获益越大(见:依鲁替尼 5 年随访数据公布:越早使用,生存获益越大),依鲁替尼在中国获批上市是中国患者的福音。
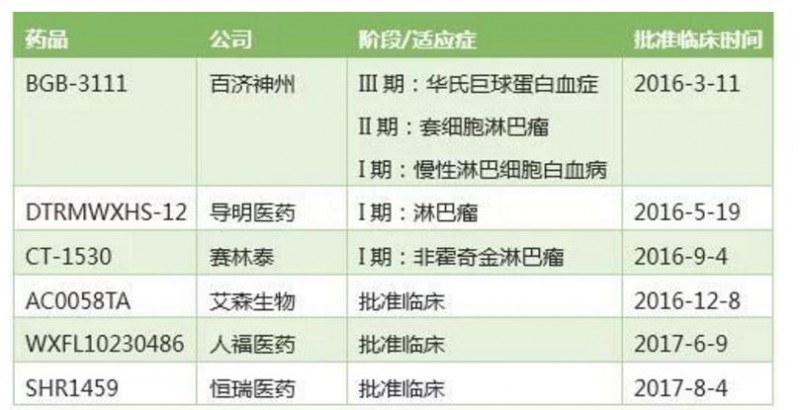
强生之外,国内目前共有其他 6 家公司的 BTK 产品向 CDE 注册申报,且均已获批临床。特别是百济神州的 BGB-3111,已经推进到了 III 期阶段。国内外在研的 BTK 抑制剂信息如下:
国内申报注册的 BTK 抑制剂
本网站新闻资讯、文章、研究数据、治疗案例均来自于国内外医学论文,所涉及到的新药、新技术有可能还处于临床研究阶段,患者不能作为治疗疾病的依据。癌症治疗目前尚无治愈手段,患者需要在医生的指导下,在医院接受正规治疗或参加新药新技术临床试验。
帮助广大患者在抗癌之路上少走/不走弯路
最终成功战胜病魔!
靶向治疗|最新资讯|临床试验|靶向药物|
基因检测|免疫治疗资讯|定期专家科普讲座