ICP-723是我国自主研发的新一代NTRK抑制剂,可以治疗携带NTRK融合基因的晚期或转移性实体瘤,包括乳腺癌、结直肠癌、肺癌、甲状腺癌等,以及对第一代NTRK抑制剂拉罗替尼和恩曲替尼耐药的患者。临床前研究表明,ICP-723具有良好的安全性和对多种实体瘤的高活性,有可能为NTRK基因融合的实体瘤患者提供广谱抗癌治疗。2021年8 月 31 日InnoCare Pharma公司宣布其第二代泛 TRK 抑制剂 ICP-723 获得美国食品药品监督管理局(FDA)的研究性新药批准在美国开始 I 期临床试验。

在这项 I 期剂量递增研究中,截止到2022年2月11日,共有17 名处于 I 期剂量递增的患者接受 ICP-723 治疗,其中6名为NTRK融合阳性的患者。 结果显示:6例NTRK融合患者中,这意味着6例NTRK融合阳性的患者在接受ICP-723治疗后,病情都得到了有效控制,病灶稳定或显著缩小。 值得一提的是,1名脑转移的患者也达到了部分缓解,脑部靶病灶从 并且所有达到部分缓解的患者在数据截止时仍持续响应。
根据上述初步研究数据表明,ICP-723在晚期实体瘤患者中安全且耐受性良好。各种癌症类型的NTRK基因融合的患者出现了得到了令人鼓舞的临床疗效,包括入脑活性。 值得振奋的是,目前在中国,ICP-723的临床试验目前正在招募患者,已经有大量NTRK阳性的患者通过全球肿瘤医生网成功入组。好消息是,目前针对青少年(12-18岁)患者也开启招募了,这款不限癌种的国研好药将为更多国内患者带来生存获益。 InnoCare 联合创始人、董事长兼首席执行官 Jasmine 博士说,“作为一种新型小分子第二代泛 TRK抑制剂,ICP-723在临床前实验中具有强活性和高选择性,有望克服对第一代TRK抑制剂的耐药性,更好地造福患者。”



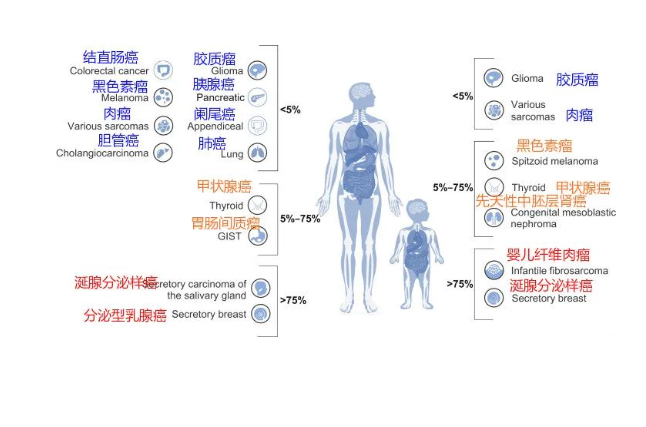
NTRK基因融合并不常见,有趣的是,亚洲患者NTRK融合的频率较高,在中国常见的肺癌,乳腺癌,结直肠癌中,只有1%~5%的患者存在这种突变,而一些罕见的癌症,比如婴儿纤维肉瘤和分泌型乳腺癌,存在NTRK融合的频率却高达90%~100%。 目前已发现NTRK融合存在于超过45类癌症中,包括非小细胞肺癌,乳腺癌、结直肠癌、甲状腺癌等。其中,NTRK在成人唾液腺癌,软组织肉瘤和甲状腺癌,儿童纤维肉瘤,唾液腺癌的突变频率最高,强烈建议这几类癌症患者确诊后及时检测NTRK基因。 申请方舟基因检测援助