
肿瘤免疫疗法,包括PD1、CTLA4、CAR-T细胞、TCR-T细胞、癌症疫苗、树突细胞、NK细胞、CTL细胞等,是目前全世界攻克癌症的研究热点。部分技术(PD1、CAR-T、CTLA)已经取得突破,被美国FDA批准作为药物临床治疗癌症,但大部分细胞治疗技术因为疗效问题,仍在临床试验研究过程中,或者被某些国家批准用于再生治疗(日本再生医疗法批准细胞技术辅助治疗癌症)。

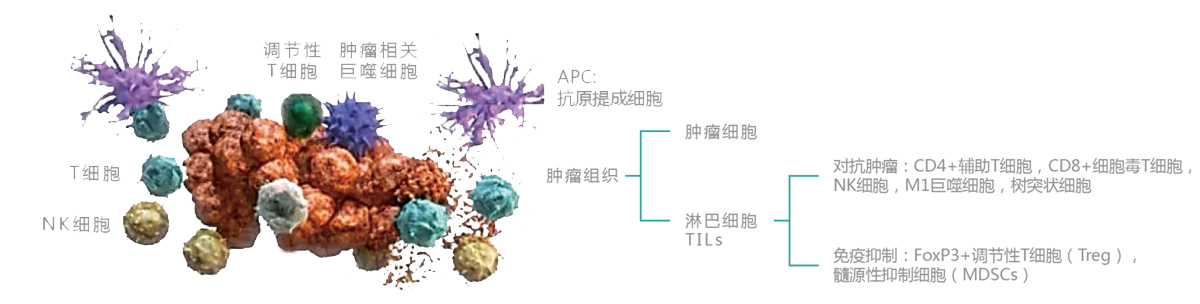 TIL(Tumorinfiltrating lymphocytes)指肿瘤浸润的淋巴细胞。在手术切除的肿瘤组织中,大部分是肿瘤细胞,也有少部分淋巴细胞。这些淋巴细胞中有部分是针对肿瘤特异性突变抗原的T细胞,是深入到敌军内部打击能力最强的免疫细胞,但是由于一些原因(比如肿瘤微环境和PD-1),他们的功能受到了抑制,不能在肿瘤组织中有效的杀伤肿瘤细胞。但是,科学家通过一些体外培养方法把这些肿瘤组织中的某类型的淋巴细胞富集起来,再回输给患者,就能够发挥抗肿瘤作用,而且联合PD-1效果会更好。
TIL(Tumorinfiltrating lymphocytes)指肿瘤浸润的淋巴细胞。在手术切除的肿瘤组织中,大部分是肿瘤细胞,也有少部分淋巴细胞。这些淋巴细胞中有部分是针对肿瘤特异性突变抗原的T细胞,是深入到敌军内部打击能力最强的免疫细胞,但是由于一些原因(比如肿瘤微环境和PD-1),他们的功能受到了抑制,不能在肿瘤组织中有效的杀伤肿瘤细胞。但是,科学家通过一些体外培养方法把这些肿瘤组织中的某类型的淋巴细胞富集起来,再回输给患者,就能够发挥抗肿瘤作用,而且联合PD-1效果会更好。
过继性T细胞疗法--TIL细胞疗法是由免疫界泰斗Rosenberg及其团队开创的新方法。 Rosenberg认为,癌细胞入侵时,自身的免疫系统会试图打败体内蔓延的肿瘤。 过去三十年间,他和他的团队一直在致力做一件事情:如何发现并放大“打败”工作做得最好的那部分免疫系统细胞。
TIL的免疫细胞来自于肿瘤组织,而其他细胞免疫疗法大部分来取自血液,这直接决定了免疫细胞识别肿瘤的能力。据估计,肿瘤里分离出的免疫细胞,有60%以上能识别肿瘤,而血液里面分离的免疫细胞,不到0.5%。
这种新型的疗法不是像传统的简单的扩增回输,而是要确定患者病例中特定的突变。之后利用突变信息找到能够最有效瞄准这些突变的T细胞,最后提取出专门患者肿瘤中细胞突变的T细胞,这些细胞具有精准识别癌细胞的能力。
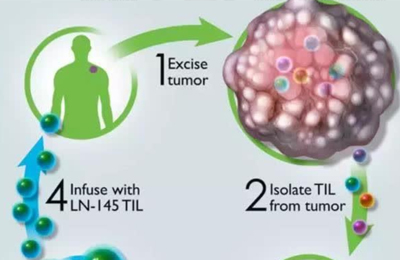
这些免疫细胞经过体外培养后,重新注入到患者体内。同时,研究团队联合使用了免疫增强药物白细胞介素2和另一种“明星抗癌药”PD-1抑制剂Keytruda,Keytruda即属于另一种免疫疗法免疫检查点阻断,在某些癌症中有显著的效果。
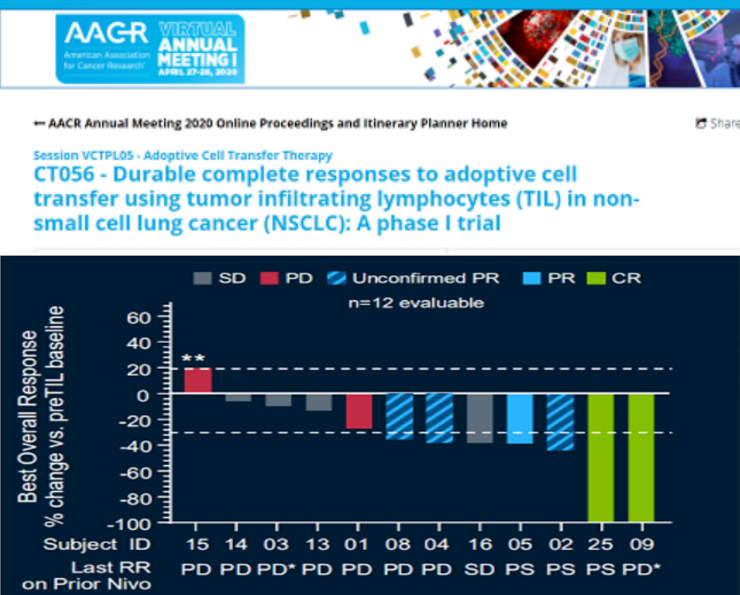
今年的AACR会议上,一项由美国知名癌症中心莫菲特癌症研究中心(H. Lee Moffitt )开展的基于TIL细胞治疗的Ⅰ期临床结果公布:
在12名可评估的非小细胞肺癌患者中,TIL疗法可达到,其中两名患者达到持久的完全缓解。大部分患者在首次TIL治疗后进行 CT扫描就开始出现明显的肿瘤消退。
3名患者病情缓解,其中两名完全患者,并且已超过一年。
另一名患者的缓解即将得到确认。
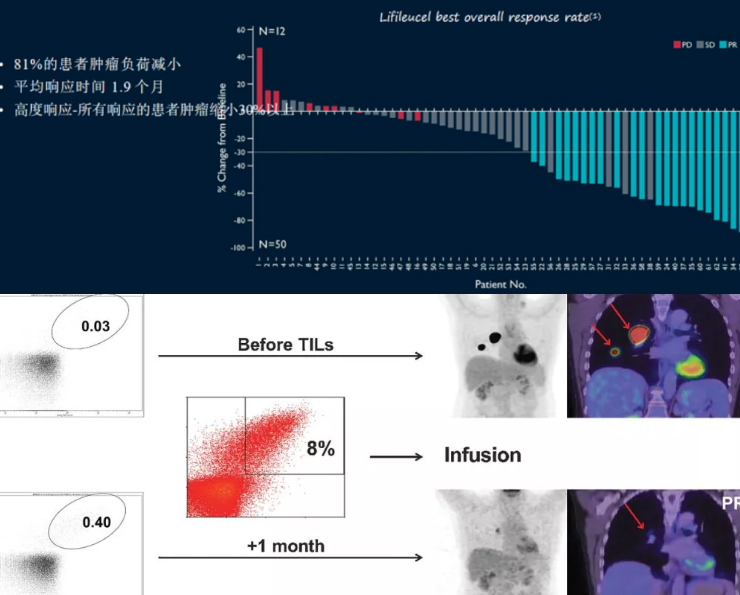
2024年2月16日,美国食品药品监督管理局(FDA)加速批准lifileucel(Amtagvi,Iovance Biotherapeutics,Inc.)用于PD-1/PD-L1治疗后进展的晚期黑色素瘤。
本次获批主要是基于全球性的多中心2期研究C-144-01的临床试验数据。C-144-01是一项开放标签、多队列、多中心的2期临床试验,旨在检视单次注射lifileucel在晚期黑色素瘤患者身上的疗效与安全性,这些患者患有不可切除或转移性黑色素瘤,之前接受过至少一种全身治疗,包括PD-1阻断抗体,如果BRAF V600突变阳性,则接受BRAF抑制剂联合或不联合MEK抑制剂。在153例患者中,独立评审委员会(IRC)根据RECIST v1.1标准评估的客观缓解率(ORR)为31.4%,其中包含8位患者达完全缓解(CR)与40位患者达部分缓解(PR)。在中位27.6个月的研究随访中,41.7%的反应维持≥18个月。中位总生存期和无进展生存期分别为13.9个月和4.1个月。
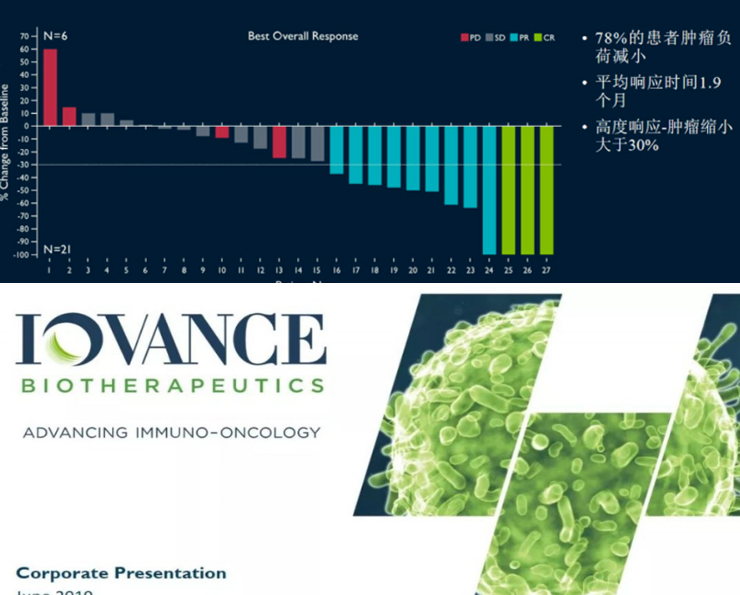
LN-145就是由Iovance公司研发的基于自体肿瘤浸润淋巴细胞(TIL)的疗法,第二阶段innovaTIL-04(C-145-04)积极的试验的数据显示,晚期宫颈癌患者的TIL治疗。
结果显示:
客观缓解率(ORR),完全缓解率(CR),疾病控制率(DCR)。即12名的患者有效果,包括1名完全应答,9名部分应答和2个未确认的部分应答;
中位随访时间为3.5个月,12例患者中有11例持续应答;
没有任何严重的副作用发生。
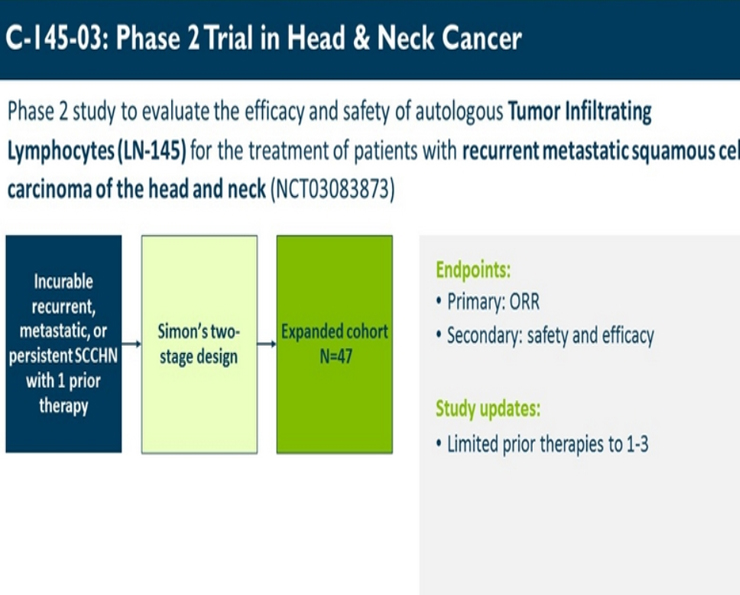
C-145-03是2期临床试验,招募患有复发性和/或转移性HNSCC的患者,其已接受至少一种先前的全身免疫疗法和/或化学治疗的治疗。
初步数据显示,试验中的8名患者中有3名患者的肿瘤大小减少了。
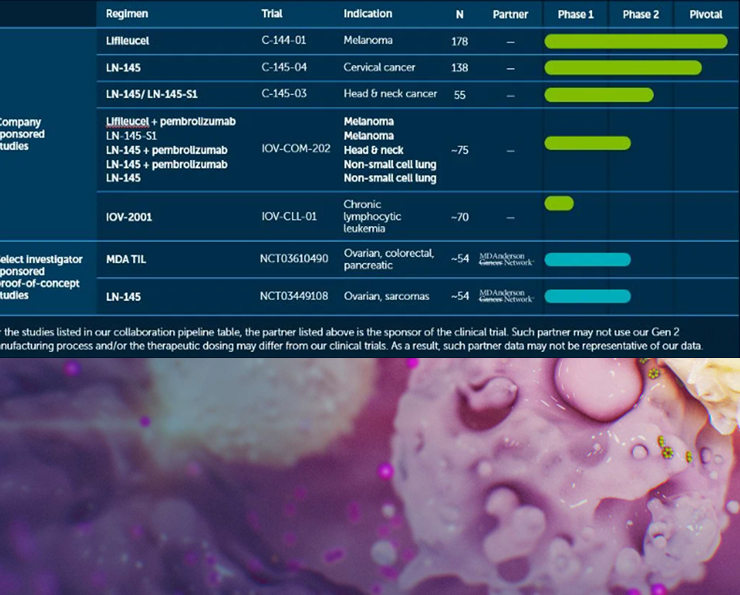
IOV-COM-202是一项2期临床试验,招募已被诊断为组织学证实的不可切除或转移性黑色素瘤(队列1),头颈部复发或转移性鳞状细胞癌(队列2),或复发或转移的患者非小细胞肺癌(队列3)。
临床试验旨在确定Iovance研究性TIL治疗(LN-144 / LN-145)是否安全有效地治疗不可切除/转移性黑色素瘤,复发/转移性HNSCC和NSCLC(帮助患者活得更长和/或更慢降低癌症进展),暂未公布临床结果。
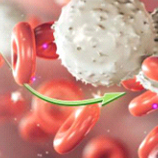
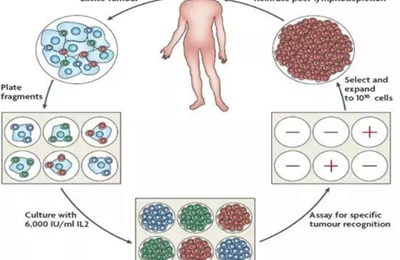
我们得到病人的肿瘤组织块,其中混杂着体积较大的肿瘤细胞(浅蓝色)以及体积小而圆的T淋巴细胞(红色,绿色,深蓝色)
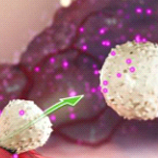
肿瘤样本被运送到专有的GMP设施,在那里TIL被分离并繁殖,将不同种类的T淋巴细胞在细胞板上克隆化,并加入高浓度的IL-2来选择培养,在三周内产生数十亿TIL。

在IL-2的刺激下不同种类的T淋巴细胞都得到了克隆扩增,形成了细胞群;
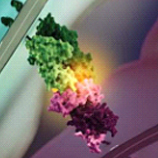
用病人的肿瘤细胞和扩增后的T淋巴细胞反应,凡是能够发生杀瘤效应的T淋巴细胞群作为阳性TIL群留下(红色),其余的丢弃(绿色,深蓝色);
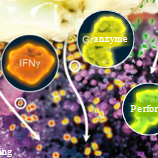
用负载了肿瘤特异性抗原的树突状细胞(DC)进一步扩增培养肿瘤特异性的TIL;
患者开始一周的预处理治疗(清髓)以准备接受TIL.TIL产品作为一次性疗法施用,在TIL输注后立即接受多达6剂白细胞介素2(IL-2),来支持患者体内TIL的生长和激活。
| 癌种 | 研究数据 |
|---|---|
| 非小细胞肺癌 | 今年的AACR会议上,一项由美国知名癌症中心莫菲特癌症研究中心(H. Lee Moffitt )开展的基于TIL细胞治疗的Ⅰ期临床结果公布: 在12名可评估的非小细胞肺癌患者中,TIL疗法可达到25%的总缓解率,其中两名患者达到持久的完全缓解。大部分患者在首次TIL治疗后进行 CT扫描就开始出现明显的肿瘤消退。
3名患者病情缓解,其中两名完全患者,并且已超过一年。
另一名患者的缓解即将得到确认。 来源:AACR会议,莫菲特癌症研究中心(H. Lee Moffitt )开展的基于TIL细胞治疗的Ⅰ期临床结果 |
| 黑色素瘤 | 莫菲特癌症中心对60例晚期黑色素瘤(MEL)患者(中位年龄为49岁),进行了TIL疗法的汇总疗效分析,试验对象为仅接受TIL治疗、TIL与纳武单抗(nivo)联合治疗、TIL与伊匹单抗(ipi)联合治疗、TIL与维莫非尼(vem)联合治疗。结果显示: TIL疗法在晚期黑色素瘤患者中的客观缓解率(ORR)达到36%,完全缓解率(CR)达14%,中位总生存期(OS)长达52个月(95%CI:24-未达到),中位无进展生存期(PFS)达到10个月(95%CI:7-71)。 |
| 宫颈癌 | 段innovaTIL-04(C-145-04)积极的试验的数据显示,晚期宫颈癌患者的TIL治疗总体反应率(ORR)为44%。 结果显示: 客观缓解率(ORR)44%,完全缓解率(CR)11%,疾病控制率(DCR)达85%。即12名的患者有效果,包括1名完全应答,9名部分应答和2个未确认的部分应答; 中位随访时间为3.5个月,12例患者中有11例持续应答; 没有任何严重的副作用发生。 来源:Iovance公司研发的基于自体肿瘤浸润淋巴细胞(TIL)的疗法 |
| 头颈鳞状细胞癌 | C-145-03是2期临床试验,招募患有复发性和/或转移性HNSCC的患者,其已接受至少一种先前的全身免疫疗法和/或化学治疗的治疗。 初步数据显示,试验中的8名患者中有3名患者的肿瘤大小减少了30%。 来源:2期临床试验 |
| 实体肿瘤 | IOV-COM-202是一项2期临床试验,招募已被诊断为组织学证实的不可切除或转移性黑色素瘤(队列1),头颈部复发或转移性鳞状细胞癌(队列2),或复发或转移的患者非小细胞肺癌(队列3)。 临床试验旨在确定Iovance研究性TIL治疗(LN-144 / LN-145)是否安全有效地治疗不可切除/转移性黑色素瘤,复发/转移性HNSCC和NSCLC(帮助患者活得更长和/或更慢降低癌症进展),暂未公布临床结果。 来源:IOV-COM-202的2期临床试验 |