2019年肺癌靶向药靶向治疗和肺癌免疫治疗及免疫治疗药物盘点
肺癌是世界第一大癌,发病率和死亡率均排在首位。肺癌分为非小细胞肺癌(NSCLC)和小细胞肺癌(SCLC),前者占比80%以上,后者占约15%。
虽然肺癌已经有多种靶向药问世,例如靶向EGFR、ALK、ROS1和BRAF的多种肺癌靶向药已经获批,基于驱动肺癌患者的致癌基因变异开发的靶向疗法已经是肺癌治疗的重要手段。但是,仍然没有满足肺癌患者想要获得长期生存的愿望!
在2019年,肺癌在免疫治疗药物和靶向治疗药物中取得了重大的突破,难治靶点也有新的靶向药来对付,也取得了非常好的临床数据,多种免疫治疗药物扩大了新适应症,肺癌治疗的选择越来越多!
肺癌靶向治疗——难治靶点也有重大突破
肺癌是靶向治疗研究进展最快的领域,目前,已经被纳入临床指南的标准检测靶点有EGFR、ALK、ROS1和NTRK,这些靶点是有确切的获批药物的。而有些在研的其他靶点也能为肺癌患者的生存期带来获益。
非小细胞肺癌常用靶向药国内上市及医保情况
EGFR——肺癌
| 药品名 | 中文名 | 生产商 | 中国上市 |
| Gefitinib(Iressa) | 吉非替尼(易瑞沙、伊瑞可) | 阿斯利康(外) | 是,纳入医保 |
| Icotinib(Conmana) | 埃克替尼(凯美纳) | 贝达药业(国) | 是,纳入医保 |
| Erlotinib(Tarceva) | 厄洛替尼(特罗凯) | OSI/Genentech(外) | 是,纳入医保 |
| Osimertinib(Tagrisso) | 奥希替尼(泰瑞莎) | 阿斯利康(外) | 是,纳入医保 |
| Dacomitinib(Vizimpro) | 达克替尼 | 辉瑞(外) | 否 |
| Afatinib(Gilotrif) | 阿法替尼(吉泰瑞) | 勃林格殷格翰(外) | 是,纳入医保 |
| Necitumumab(Portrazza) | 耐昔妥珠单抗 | 礼来(外) | 否 |
ALK——肺癌
| 药品名 | 中文名 | 生产商 | 中国上市 |
| Crizotinib(Xalkori) | 克唑替尼(赛可瑞) | 辉瑞(外) | 是,纳入医保 |
| Alectinib(Alecensa) | 阿来替尼(安圣莎) | 罗氏(外) | 是,未进医保 |
| Ceritinib(Zykadia) | 色瑞替尼(赞可达) | 诺华(外) | 是,未进医保 |
| Brigatinib(Alunbrig) | 布加替尼 | 武田(外) | 否 |
| Lorlatinib(Lorbrena) | 劳拉替尼 | 辉瑞(外) | 否 |
ROS1——肺癌
| 药品名 | 中文名 | 生产商 | 中国上市 |
| Crizotinib(Xalkori) | 克唑替尼(赛可瑞) | 辉瑞(外) | 是,纳入医保 |
| Ceritinib(Zykadia) | 色瑞替尼(赞可达) | 诺华(外) | 研究中(ROS1) |
| Brigatinib(Alunbrig) | 布加替尼 | 武田(外) | 研究中(ROS1) |
| Lorlatinib(Lorbrena) | 劳拉替尼 | 辉瑞(外) | 研究中(ROS1) |
| Cabozantinib(Cabometyx) | 卡博替尼 | Exelixis(美) | 研究中(ROS1) |
| Entrectinib(RXDX-101) | 恩曲替尼 | 罗氏(外) | 否 |
NTRK——实体瘤
| 药品名 | 中文名 | 生产商 | 适应症 | 中国上市 |
| Larotrectinib(Vitrakvi) | 拉罗替尼 | 拜耳(外) | NTRK融合实体瘤 | 否 |
| Entrectinib(RXDX-101) | 恩曲替尼 | 罗氏(外) | NTRK融合实体瘤 | 否 |
靶向MET两款药物崭露头角
大约3%的肺癌患者中观察到MET外显子14突变,并且MET靶点目前在NCCN指南中被列为克唑替尼的潜在靶标。在2019年ASCO大会上,我们看到了另外两个靶向药超乎意料的研究结果。
首先,MET抑制剂capmatinib,每天口服两次400mg剂量,用于初治和先前治疗过的MET外显子14突变的晚期非小细胞肺癌(NSCLC)患者。
结果显示,先前接受治疗的患者(n = 69)78%的疾病控制率。在未接受过治疗的患者中(n = 28),96%病情得以控制。先前治疗和未治疗患者的中位无进展生存期分别为4.8个月和11.1个月。
另外,MET酪氨酸激酶抑制剂tepotinib,MET外显子14突变阳性晚期NSCLC 患者,每日口服500mg 。无论是通过组织切片(n = 57)或者血液(n = 58)检测到MET外显子14突变,治疗结果没有任何明显的疗效差异。无进展生存期分别是组织切片检测组9.5个月,血浆检测组为10.8个月。
这两种药物副作用很相似,以周围水肿和恶心为主要症状,没有更严重的。
RET融合两款新药进展迅速
在大约1%-2%的晚期NSCLC患者中观察到RET融合,目前还没有靶向药获批,但RET是另一种前景较好的生物标志物。有两个靶向药,在今年获得了突破性进展。
01、LOXO-292临床试验已入驻中国
一个RET融合靶向药LOXO-292( selpercatinib)则在今年的世界肺癌大会(WCLC)上出尽风头。LOXO-292在一个105位 NSCLC患者组成的队列中,客观无进展生存率高达60%,既往未接受过其他治疗的患者客观无进展生存率可以达到80%!
LOXO-292产生的无进展生存期可达到20个月,总生存期则超过20个月。患者对LOXO-292的耐受性很好,很少出现2级以上的不良反应(AE)。
总的来说,药物LOXO-292已经在这个RET突变的患者亚组中显示出非常好的活性。
目前,LIBRETTO-431临床试验正在评估针对未接受过RET融合阳性的非小细胞肺癌(NSCLC)患者selpercatinib(也称为LOXO-292)的治疗效果。
02、BLU-667获FDA突破疗法认定
在2019 ASCO大会上,我们看到了RET抑制剂BLU-667在起始剂量下进行1/2阶段试验的结果,每日口服400毫克剂量,48例患者的疾病控制率为96%,其中许多患者的反应持续时间较长。
该试验还证明BLU-667具有良好的活性,无论先前经铂化疗或免疫治疗过,或者脑转移的患者,都有良好的治疗效果。
既往做过铂类化疗患者(n=35)的无进展生存率为60%,疾病控制率高达为100%。
另外,重点是对于未接受过其他治疗晚期癌症患者,采用BLU-667初始治疗,在7名患者中的5名患者中缩小了肿瘤,无进展生存率为71%。
在可评估疗效的脑转移患者中,CT扫描或MRI上检查发现9名中有7名患者缩小了脑肿瘤,缓解率为78%。2个脑转案例展示中,1例患者脑病灶缩小了70%,另一例缩小了67%。
截止至数据公布时,还有82%患者仍在接受BLU-667治疗,也就是说获益还在继续。
对于RET突变,迄今仍然没有靶向药获批。而本次BLU-667所展现的亮眼数据,也支持这款新药在明年第一季度递交申请。但是,目前BLU-667已经获得了美国FDA授予的突破性疗法认定。我们共同期待它早日获批造福大众!
KRAS突变新药打破十年失败魔咒
KRAS是肺癌中最常见的突变,存在于20%-25%的病例中,但是有关KRAS突变阳性的NSCLC 临床试验在十多年来一直没有取得进展,几乎所有KRAS相关的临床试验都已失败告终。
01、靶向药AMG 510给肺癌KRAS人群带来新生机
2019年ASCO年会上,一个非常早期的研究报告将一种新药带进我们的视野。AMG 510是一种新型小分子抑制剂,靶向KRAS G12C突变,晚期NSCLC中有13%的KRAS G12C突变。
该药物在一项多中心1期试验中进行了研究,按照不同AMG 510剂量递增模式分别给予:180mg,360mg,720mg和960mg。
数据截止时,入组的10名非小细胞肺癌患者,对抗KRAS G12C阳性晚期非小细胞肺癌患者的无进展生存率达到50%,在这10名可评估的NSCLC患者中,5名患者发生部分应答,疾病控制率更是高达为100%。
- 分享两个治疗成功的案例 -
一名61岁的女性,于2010年8月被诊断患有KRAS G12C阳性转移性非小细胞肺癌。接受过化疗、放疗和nivolumab(纳武单抗,Opdivo)。在2018年9月,开始用180mg的AMG 510治疗。肿瘤减少了34%,截至数据截止时还在接受治疗,已经治疗27.4周。
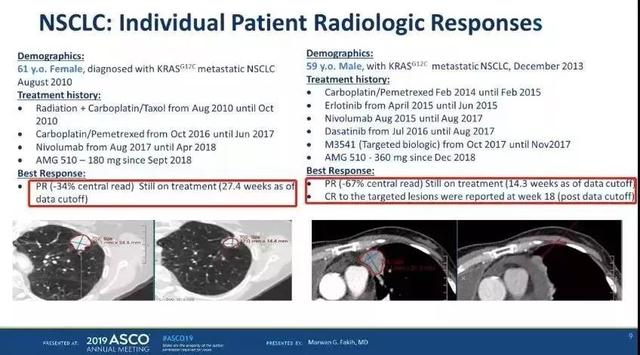
另一例是59岁男性患者,2013年12月被诊断患有KRAS G12C阳性非小细胞肺癌。接受了化疗、厄洛替尼(特罗凯)、纳武单抗、达沙替尼和M3541。2018年12月开始用360 mg的AMG 510治疗。在数据截止时继续接受治疗,肿瘤大小减少了67%,已经治疗了14.3周。
02、派姆单抗(K药)也能应对KRAS靶点毫不含糊
2019年12月12日,在内瓦举行的欧洲医学肿瘤学会(ESMO)免疫肿瘤大会上发表的论文论文摘要,III期KEYNOTE-042研究结果,无论是KRAS突变与否,抗PD-1疗法pembrolizumab(KEYTRUDA,派姆单抗,可瑞达,帕博利珠单抗,K药)单药一线治疗肿瘤表达PD-L1(肿瘤比例评分[TPS]≥1%)的转移性非鳞状非小细胞肺癌(NSCLC)患者,改善了总生存期(OS)、无进展生存期(PFS)、总缓解率(ORR)。
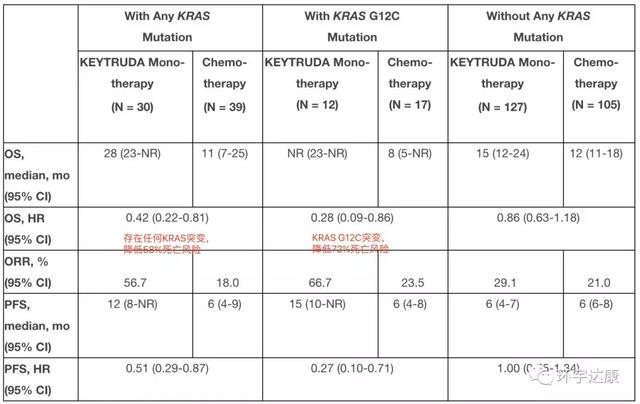
在KEYNOTE-042中登记的1,274例未经治疗的转移性非鳞状NSCLC患者的肿瘤表达PD-L1(TPS≥1%),其中301例患者具有可评估的KRAS数据(n = 232,无任何KRAS突变;n = 69,有任何KRAS突变,包括n = 29(具有KRAS G12C突变)。
患者按1:1的比例随机分配,每三周(Q3W)静脉注射KEYTRUDA 单药200 mg(n = 637)或研究者选择的化疗方案(培美曲塞或紫杉醇)(n = 637)。持续治疗直至疾病进展或出现不可接受的毒性。主要终点是OS,按顺序评估TPS≥50%、≥20%和≥1%的数据,次要终点是PFS和ORR。
该探索性分析的结果表明,无论KRAS突变状态如何,KEYTRUDA单药治疗均能改善临床疗效。与化学疗法相比,单药KEYTRUDA将存在任何KRAS突变的患者的死亡风险降低了58%,具有KRAS G12C突变的患者死亡风险降低了72%。KEYTRUDA的安全性与先前报道的转移性NSCLC患者的研究一致。
肺癌免疫治疗——全面覆盖肺癌多种类型
说完了靶向药的进展,我们再来看看免疫治疗药物,也就是常说的PD-1和PD-L1。癌症免疫疗法自从问世以来,除了在黑色素瘤和尿路上皮癌取得了重大突破,在肺癌方面进展更加迅速。
01、派姆单抗在中国接连获批3个肺癌适应症
今年,默沙东(MSD)的重磅PD-1抑制剂Keytruda(pembrolizumab,派姆单抗)又获得两项FDA批准。Keytruda在4月获批作为单药疗法,一线治疗PD-L1阳性(TPS>1%)的非鳞状NSCLC患者,随后在6月获批作为单药疗法,治疗SCLC患者。
不仅在FDA大显身手,截至目前,派姆单抗而且在国内已经获得3个一线治疗非小细胞肺癌的适应症和1个二线治疗黑色素瘤的适应症。11月25日,中国国家药监局(NMPA)批准该默沙东的重磅PD-1抑制剂Keytruda,与卡铂或紫杉醇联用,一线治疗转移性鳞状非小细胞肺癌(NSCLC)患者。
派姆单抗(K药)在中国获批的适应症
| 时间 | 适应症 |
| 2018-7-26 | 单药,黑色素瘤,二线治疗 |
| 2019-3-28 | 联合培美曲塞和铂类,非鳞状非小细胞肺癌,一线治疗 |
| 2019-10-2 | 单药,TPS≥1%非小细胞肺癌,一线治疗 |
| 2019-11-25 | 联合卡铂和紫杉醇,鳞状非小细胞肺癌,一线治疗 |
02、阿特珠单抗FDA获批肺癌2个新适应症
2019年3月19日,美国食品和药物管理局(FDA)宣布,批准对PD-L1抑制剂atezolizumab(阿特朱单抗,Tecentriq)与卡铂和依托泊苷联合用于广泛期小细胞肺癌(ES-SCLC)患者的一线治疗。阿特珠单抗成为20多年来首款获批治疗广泛期小细胞肺癌的一线新疗法。
又在今年9月,欧盟批准Tecentriq(atezolizumab,阿特珠单抗),与化疗(卡铂和白蛋白紫杉醇)联用,一线治疗转移性非鳞状非小细胞肺癌(NSCLC)患者,这些患者不携带EGFR基因突变或ALK变异。
另外,阿特珠单抗作为一线单药疗法,在治疗PD-L1高表达非小细胞肺癌患者的3期临床试验中,表现也优于化疗效果,我们期待后续的临床数据。
03、nivolumab / ipilimumab组合有望进军肺癌一线
2018年8月,纳武单抗(Nivolumab,opdivo)成为第一个被批准用于特定小细胞肺癌患者的免疫检查点抑制剂。早在2015年,纳武单抗就已经获批用于肺癌的治疗。
2019年,百时美施贵宝(BMS)的Opdivo(nivolumab,纳武单抗)/Yervoy(ipilimumab,伊匹单抗)组合作为肺癌一线疗法,在3期试验中表现优于化疗,它可能为肺癌患者提供一款不含化疗药的癌症免疫组合疗法,我们拭目以待。
04、德鲁单抗入驻中国,Ⅲ期肺癌再添“免死金牌”
2019年11月末,阿斯利康(AstraZeneca)公司的PD-L1抑制剂Imfinzi(durvalumab,德鲁单抗)刚刚获得FDA的优先审评资格,有望成为一线治疗小细胞肺癌患者的第二款PD-L1抑制剂。
此次优先审评资格基于III期CASPIAN试验的阳性数据。结果显示,与标准护理(SoC)含铂化疗相比,固定剂量的德鲁单抗联合SoC含铂化疗显著改善了总生存期(13.0个月 vs 10.3个月),18个月存活率大幅提高(33.9% vs 24.7%)。
另外,2018 年 2 月,美国 FDA 正式批准德鲁单抗用于治疗Ⅲ期不可手术切除,接受初始放化疗的治疗后无进展的局部晚期非小细胞肺癌(NSCLC)患者。不到两年时间,2019年12月9日,中国国家药品监督管理局官网显示德鲁单抗注射液的上市申请获得批准,这意味着,德瓦鲁单抗成为中国内地首个获批上市的PD-L1单抗药物,用于治疗同步放化疗后未进展的不可切除Ⅲ期非小细胞肺癌(NSCLC)。
文章小结
肺癌是全球第一大癌,也是用药选择最多的癌症,但是该如何制定治疗方案,选择哪种药物更能延长生存期,只凭基因检测报告,只靠病理报告,恐怕是很难做出正确判断的。21世纪,癌症治疗更加关注的是个性化方案,即根据不同的病情选择不同的药物及剂量,针对每个个体做出最合适的治疗方案。
全球肿瘤医生网对接国内、外的肿瘤医院及经验丰富的肺癌专家,为全国肺癌患者代挂号、代问诊,或者预约专家进行一对一专家咨询(面诊或远程视频咨询均可,),的专家会紧随国际治疗前沿,带来的治疗指导建议,可以更精准地解读基因检测报告,解决当地医生经验不足,不合理给药或者是盲目告知“回家坐以待毙”的情况。







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城