2020年2月抗癌新药,五大抗癌药物,癌症新药,抗肿瘤新药获FDA优先审批,上市在即
新年刚过,虽然国内还笼罩在肺炎疫情的阴霾下,但是国际上对于抗癌药物的审批和上市丝毫没有慢下脚步,好消息不断。1月份已有3款抗癌药物获批上市,分别是用于治疗膀胱癌的pembrolizumab,胃肠间质瘤的AYVAKIT和上皮肉瘤的tazemetostat。而2月份,已有多款药物获得优先审批称号,如全球首个MET靶向药capmatinib,胃肠间质瘤新药Avapritinib,乳腺癌新药图卡替尼,小细胞肺癌新药lurbinectin。昨天,FDA又传来好消息,授予阿特珠单抗(Tecentriq)一线治疗非小细胞肺癌优先审批。
FDA将于今年6-8月左右公布对这些药物的最终审批结果。这意味着,如果一切顺利,2020年的中下旬将有多款抗癌新药呈井喷式获批上市,将给癌友们带来更多治疗的选择和希望!
五大抗癌药物获FDA优先审批,上市在即
全球肿瘤医生网医学部将2月份获得优先审批的五大抗癌药物的信息做了盘点,便于病友们参考。
注释*优先审查:FDA对确定有可能在严重疾病的治疗,预防或诊断方面提供重大改进的药物给予优先审查
01、全球首款METex14抑制剂-Capmatinib
药物名称:Capmatinib(卡马替尼 INC280)
生产厂家:诺华
优先审批时间:2020年2月11日
FDA预计裁定时间:6个月内
适应症:治疗携带MET外显子14跳跃突变的转移性非小细胞肺癌(NSCLC)患者,包括一线治疗(初治)患者和先前接受过治疗(经治)的患者
NSCLC约占肺癌诊断的85%。METex14突变发生在3-4%的新诊断晚期NSCLC病例中,这是一种预后特别差的肺癌,目前尚无批准的针对METex14突变的晚期NSCLC的疗法。
2020年2月11日,FDA已受理MET抑制剂capmatinib(INC280)的新药申请(NDA)并授予了优先审查,正被评估用于治疗携带MET外显子14跳跃突变的转移性非小细胞肺癌(NSCLC)患者,包括一线治疗(初治)患者和先前接受过治疗(经治)的患者。
此次优先审批是基于II期临床研究GEOMETRY mono-1的阳性结果,共97例患者入组:
(1)在初治患者(28例,先前没有接受过治疗)中,总缓解率(ORR)为67.9%,疾病控制率(DCR)为96.4%,中位缓解持续时间(DOR)为11.14个月,中位无进展生存期为9.69个月。
(2)在经治患者(69例,先前已接受过治疗,88.4%含铂化疗)中,总缓解率ORR为40.6%,疾病控制率(DCR)为78.3%,中位缓解持续时间DOR为9.72个月,中位无进展生存期为5.42个月。
(3)约有一半的脑转移患者对capmatinib应答(13人中有7人;54%)。在这些患者中,有4例完全消除了脑部病变(31%),颅内疾病控制率DCR为92.3%(12/13)。
如果获得批准,卡马替尼将是第一个专门针对METex14突变的晚期肺癌的治疗方法。
02、死亡风险降低85%,胃肠间质瘤迎来新药-Ripretinib
药物名称:ripretinib(瑞普替尼 DCC-2618)
生产厂家:Deciphera Pharmaceuticals
优先审批时间:2020年2月13日
FDA预计裁定时间:2020年8月13日
适应症:晚期胃肠道间质瘤(GIST)患者
目前,高达85%的GIST肿瘤在PDGFRA和KIT这两个基因突变之一。这些突变导致异常KIT和PDGFRA蛋白的产生,从而驱动癌症。瑞普替尼是一种KIT和PDGFRα激酶开关控制抑制剂。
FDA授予优先审批是基于INVICTUS 3期研究的积极结果,在该研究中,瑞普替尼与安慰剂相比,疾病进展或死亡的风险降低了85%(HR,0.15, P <.0001)。中位无进展生存期(PFS)为6.3个月,而安慰剂组仅为1.0个月,瑞普替尼组的总缓解率(ORR)为9.4%,而安慰剂组为0%( P = .0504)。
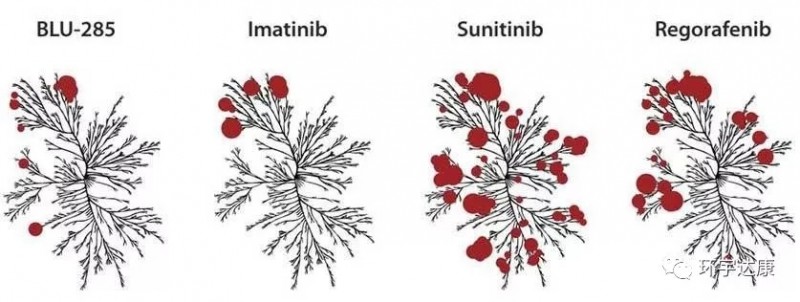
除了即将获批的瑞普替尼,目前,胃肠间质瘤目前已获批了四款药物:Avapritinib,伊马替尼,舒尼替尼,瑞格菲尼。
03、乳腺癌新药-图卡替尼
药物名称:tucatinib(图卡替尼)
生产厂家:Genetics
优先审批时间:2020年2月13日
FDA预计裁定时间:2020年8月20日
适应症:联合曲妥珠单抗和卡培他滨用于治疗局部晚期无法切除或转移性HER2阳性乳腺癌的患者,包括脑转移瘤患者,这些患者已分别或联合接受至少三种先前的HER2指导药物
与拉帕替尼和neratinib一样,tucatinib是一种口服TKI。然而,tucatinib仅阻断HER2,与其他针对多种受体的药物相比,导致皮疹和腹泻等脱靶效应更少。
此次优先审批是基于一项名为HER2CLIMB II期试验的数据,结果表明,在未经手术切除的局部晚期或转移性HER2阳性乳腺癌患者中,经严格预处理的患者与单独使用曲妥珠单抗和卡培他滨相比,曲妥替尼三联体可使死亡风险降低34%。
曲妥替尼三联药物组合的中位总生存期(OS)为21.9个月而曲妥珠单抗和卡培他滨单独治疗的中位总生存期(OS)为17.4个月。图卡替尼组和对照组的1年和2年OS发生率分别为76%和62%,45%和27%。
值得注意的是,图卡替尼还具有很好的入脑活性,三联药物将脑转移患者的疾病进展或死亡的风险降低了52%。
04、小细胞肺癌新药-Lurbinectin
药物名称:Lurbinectin(卢比卡丁)
生产厂家:PharmaMar
优先审批时间:2020年2月18日
FDA预计裁定时间:2020年8月16日前
适应症:治疗含铂治疗后进展的小细胞肺癌(SCLC)患者
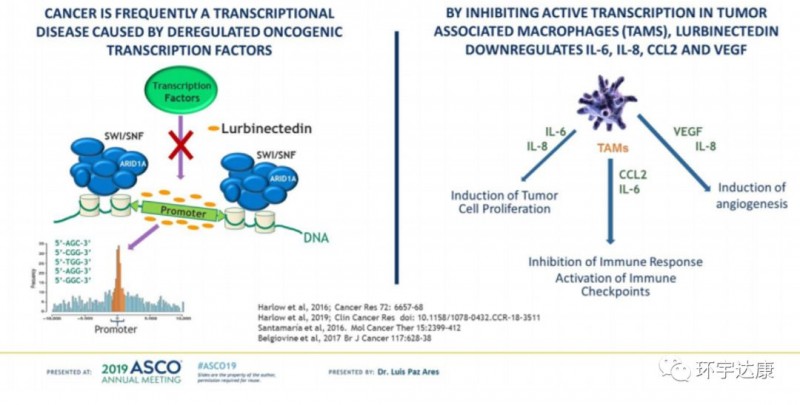
Lurbinectedin是PharmaMar自主研发的海鞘素衍生物,它是RNA聚合酶II的抑制剂,能够与DNA双螺旋结构上的小沟共价结合。RNA聚合酶II在肿瘤细胞转录过程中往往过度活化, lubrinectedin 可使得肿瘤细胞在有丝分裂过程中畸变、凋亡、最终减少细胞增殖。
此次优先审批基于II期篮子试验(NCT02454972)的结果,其中lurbinectin在铂类化疗进展的患者中达到35.2%的总缓解率(ORR),其中105例患者中的37例部分响应,另外35名患者病情稳定,疾病控制率达到了68.6%(95%CI,58.8%-77.3%)。
如果Lurbinectedin获得批准,这将成为30年来小细胞肺癌的首个新化疗方案。
05、非小细胞肺癌一线治疗新方案-阿特珠单抗
药物名称:Tecentriq(阿特珠单抗)
生产厂家:罗氏
优先审批时间:2020年2月19日
FDA预计裁定时间:2020年6月19日前
适应症:治疗含铂治疗后进展的小细胞肺癌(SCLC)患者
昨日,罗氏(Roche)宣布,美国FDA授予其重磅PD-L1抑制剂Tecentriq(Atezolizumab)优先审评资格,作为一线单药疗法,治疗PD-L1高表达,且无EGFR或ALK基因突变的晚期非鳞状和鳞状非小细胞肺癌(NSCLC)患者。FDA将在今年6月19日之前做出批准决定。
此次优先审批是基于3期临床研究IMpower110的结果,该研究显示,在PD-L1高表达患者中,与化疗相比,Tecentriq单药治疗使中位总生存期(OS)延长了7.1个月(20.2个月VS13.1个月;HR=0.595,95% CI:0.398-0.890;p=0.0106)。
阿特珠单抗(Atezolizumab)是一种单克隆抗体,可靶向PD-L1蛋白。阿特朱单抗与肿瘤细胞和肿瘤浸润性免疫细胞上表达的PD-L1结合,阻断其与PD-1和B7.1受体的相互作用。通过抑制PD-L1,可以激活T细胞消灭肿瘤细胞。
上周,Tecentriq刚在中国获批上市(阿替利珠单抗,商品名泰圣奇),联合化疗用于一线治疗广泛期的小细胞肺癌。
获批癌种:转移性非小细胞肺癌、广泛期小细胞肺癌、转移性三阴乳腺癌、晚期膀胱癌
以上是2020年2月纷纷获得优先审批的药物盘点,我们期待这五款重磅药物能顺利通过FDA的审批,早日上市造福患者。
我们处在一个充满奇迹的时代,快速发展的医疗科技给人类带来了新的希望。
曾经,癌症是不治之症。但随着抗癌手段的不断更新,尤其是分子靶向药物等新一代治疗方法的出现,人类全面战胜癌症的那天不再遥不可及,让我们一起见证这一天的来临!

































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城