实体瘤CAR-T细胞治疗,CAR-T细胞疗法国内临床试验招募中
在英语中,汽车被称为CAR,在T细胞中也有一种被称为CAR,这就是大名鼎鼎的嵌合抗原受体T细胞,简称为CAR-T细胞。而近两年兴起的CAR-T细胞疗法可谓是肿瘤免疫治疗中的一匹黑马,它的出现代表了个性化癌症治疗的重大进步,特别是给血液系统恶性肿瘤患者带来重生的希望。
2017年更是被称为CAR-T疗法的元年。这是由于FDA在2017年先后批准了全球首先的两个,也是目前仅有的两个CAR-T细胞疗法商业产品:诺华的Kymriah(淋巴瘤)与吉利德的Yescarta(白血病),由此癌症免疫治疗进入了一个新时代。
绝处逢生,患者迎来新的希望CAR-T免疫疗法
谈到CAR-T免疫疗法,我们不得不提到一个小女孩的名字,Emily Whitehead,美国最著名的白血病女孩。在2010年5岁,年仅5岁的Emily被诊断出患有B细胞急性淋巴性白血病,由于病情复发且十分凶猛,医生表示无能为力,后来她的父母放手一搏,决定试试CAR-T细胞免疫疗法。令人难以置信的是,CAR-T疗法奏效了。迄今为止,Emily已被成功无进展生存8年,她也成为这一史诗级疗法的代言人而载入史册。
2019年的Emily(无癌7年)
CAR-T疗法开发者Carl June博士同Emily参加活动

01、何谓CAR-T疗法
CAR-T(Chimeric antigen receptor T-cell,嵌合抗原受体T细胞)疗法属于过继性T细胞转移(adoptive T-cell transfer,ACT)的一种,是输血医学的一个新领域,涉及淋巴细胞回输以实现抗肿瘤,抗病毒或抗炎作用。
1989年美国的Zelig Eshhar教授首次提出CAR-T疗法的概念,他提出将抗体的轻重链连接到T细胞表面TCR的恒定区上,随后又将scFv(T细胞表达的抗体单链的的可变区)替换轻重链,避免了多次重复的转基因,这就是第一代CAR-T疗法。
其实质是将嵌合抗原受体(CAR)导入T细胞中从而产生肿瘤特异性识别的T细胞。一旦T细胞表达这种受体,便可用单个融合分子与抗原进行特异性结合并激活T细胞。这项技术的重点在于能够在相对较短的时间内产生大量有肿瘤杀伤效力的T细胞。
在早期临床试验中,CAR-T细胞疗法并没有表现出惊人的疗效,然而随着抗CD19 CAR-T细胞疗法在B细胞恶性肿瘤中显示出的巨大潜力,CAR-T产品一时间成了抗肿瘤领域的新星。目前,CAR-T已经发展至第三代,且在急性粒细胞性白血病、慢性粒细胞性白血病、非霍奇金淋巴瘤、多发性骨髓瘤中取得了显著的疗效。
02、CAR-T细胞疗法的工作原理
与其他免疫治疗技术一样,CAR-T细胞疗法旨在加强免疫系统内在的抗癌能力,这种疗法是从患者的血液中提取T细胞,并在体外对这些细胞进行基因改造,给它们装上识别癌细胞表面抗原的“嵌合抗原受体”(CAR)。
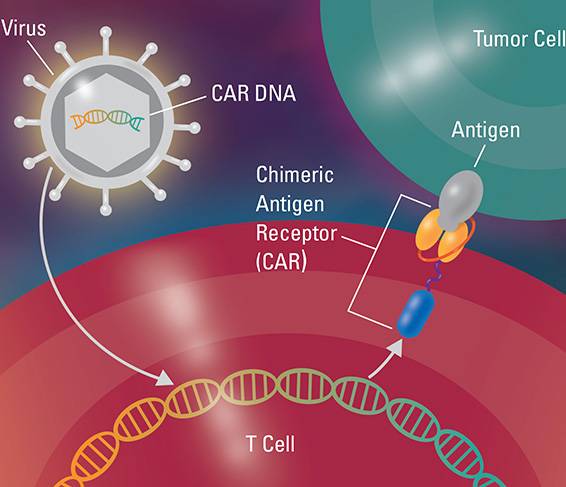
随后,这些改造之后的细胞在实验室中经过大量扩增,再被输注回患者体内,从而增大CAR T细胞在体内的存活几率。一旦存活,CAR T细胞将继续在患者体内繁殖,就像是一支装备了武器,训练有素的军队,随时会对癌细胞展开无情的攻击。
CAR-T细胞疗法的临床试验目前涉及到了部分儿童和成年人的血液癌症,如白血病、淋巴瘤和多发性骨髓瘤等。
03、FDA批准上市的2款CAR-T疗法
目前,已被FDA批准的两种CAR T细胞疗法Yescarta和Kymriah分别用于治疗白血病和淋巴瘤。

04、CAR-T疗法适合哪些人群
目前,FDA批准的CAR-T细胞治疗产品仅用于经过两次标准治疗失败的成人B细胞非霍奇金淋巴瘤或儿童急性淋巴细胞白血病患者。但现在临床试验开始评估CAR-T细胞治疗作为成人淋巴瘤和儿童急性淋巴细胞白血病的第一线或第二线治疗。由于临床试验,每一种癌症患者都有不同的FDA批准的细胞疗法产品。
经过两次治疗失败的小儿急性淋巴细胞白血病或成人侵袭性B细胞淋巴瘤患者,是接受CAR-T细胞治疗的理想选择。直到2017年年底,对于已经通过两次治疗而未达到缓解的患者,没有标准治疗方法,CAR-T细胞疗法是FDA批准的唯一一种疗法,目前对这些患者显示出显著的益处。
近年来,CAR-T细胞疗法经改进后,也被用来治疗实体瘤、自身免疫疾病、HIV感染和移植排斥等疾病,具有更广阔的应用空间。
05、CAR-T疗法的治疗流程
评估:患者需要进行很多检测和筛查,以确定CAR-T疗法是否适用。
采集:通过分离术采集患者身上的T细胞,在这个过程中,血液通过一个机器分离出T细胞,并且将剩下的血液回输患者体内。
改造:T细胞会被送到实验室进行基因改造,以在其表面产生嵌合抗原受体(CARs)。CAR使得T细胞可以识别肿瘤细胞表面的抗原。
增殖:在实验室里,经过基因改造的T细胞不断生长,直到成千上万,这一般需要几周时间。当CAR T细胞足够多时,就会被冷冻起来,送到患者所在的医院。
调节疗法:在接受CAR T细胞输注之前,患者可能会先接受针对其癌症的化疗。这有助于为注入的CAR T细胞创造更多的空间,使其可以在人体内扩大和增殖。
输注:化疗后不久,患者住进医院,医生将CAR T细胞像输血那样重新输注到体内。这是一个一次性的过程,尽管患者可能需要在医院住上几周,以监测他们的整体状况,以及对治疗和副作用的反应。
恢复:CAR T疗法的恢复期大概要持续2~3个月。在接受了CAR T细胞输注后,患者要在医院里住1到3周,这期间医生要监测他们对于治疗的反应,并且管理出现的副作用。
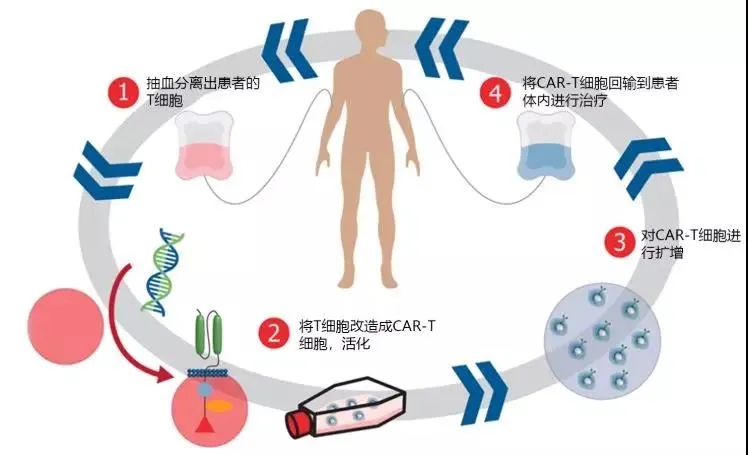
图为CAR-T的生产制备过程简单示意图
注:患者出现的副作用类型和严重程度因人而异,在治疗后的几周内会有严重的并发症的风险。通常来说,这些并发症是暂时的,会自己消退或者得到治疗。可能的副作用包括细胞因子释放综合征,是一种有着像流感那样症状(发高烧/打冷颤)的炎症,但也可能包括低血压和呼吸困难以及其他器官功能障碍,还有神经系统方面的问题,比如意识糊涂,难以理解语言讲话,或者昏迷。因为每一个患者的情况都不同,患者需要和医生提前进行沟通,并在出院后按时定期随访,以监测患者的疾病复发情况。
06、CAR-T技术在实体瘤中的瓶颈
CAR-T细胞疗法之所以在血液瘤中的疗效显著,全都得意于血液瘤的肿瘤细胞有着祖传的靶点——CD19(只存于肿瘤细胞中而不存在于正常细胞),在治疗中可以依靠此靶点带领CAR-T细胞找到并消灭癌细胞。PBCAR269A是Precision公司的第三种同种异体嵌合抗原受体CAR-T细胞疗法的候选药物,用于治疗靶向BCMA靶点的多发性骨髓瘤(蓝鸟公司)。该疗法计划在今年展开I期临床试验。
然而,实体瘤中并没有那么明显的只存在于癌细胞中而不存在于正常细胞中的靶点。因此一直以来,CAR-T细胞在治疗实体瘤中的临床疗效不佳。医学界一直希望CAR T细胞可以为更多的实体肿瘤开发出新的特异性靶点!

CAR-T疗法突破实体瘤治疗瓶颈,抗癌效果翻倍
目前,随着CAR-T代数的更迭,CAR-T在增殖、细胞因子释放等方面有了明显改进,这一技术终于破冰,越来越多的临床试验开始尝试将CAR-T细胞疗法用于实体瘤,晚期实体肿瘤患者受益于CAR-T疗法不再是梦!
具有代表性的抗原靶点:
间皮素(mesothelin):用于治疗间皮瘤、胰腺癌、卵巢癌、肺癌;
CEA:用于治疗肺癌、结肠癌、胃癌、乳腺癌和胰腺癌;
MUC-1:用于治疗肝癌、肺癌、胰腺癌、结肠癌、胃癌;
GPC3:用于治疗肝癌;
EGFRvIII:用于治疗神经胶质瘤、头颈部肿瘤;
B7-H3:用于治疗尤文肉瘤、横纹肌肉瘤、肾母细胞瘤、神经母细胞瘤和髓母细胞瘤以及特别难以治疗的脑干肿瘤(DIPG);
PSMA:用于前列腺癌等;
Claudin18.2:用于胃癌,胰腺癌等。
01、80%小鼠肿瘤完全消失!EGFRvIII CAR-T细胞"咬死"致命脑瘤
《自然》子刊Nature Biotechnology发表的一篇论文中,来自哈佛医学院麻省总医院的科学家们展示了一项抗击大脑恶性肿瘤的研究结果。他们结合两种抗癌新技术,对胶质母细胞瘤展开有效攻击。利用可产生双特异性抗体的新型CAR-T细胞进行治疗,在80%的小鼠中,脑内的肿瘤完全消失!

这项研究负责人Marcela Maus教授曾经尝试过让CAR-T细胞去识别EGFRvIII,对胶质母细胞瘤发起攻击。可实体瘤之所以难治,很棘手的原因在于“异质性”,这些癌细胞的分子特征不尽相同。在胶质母细胞瘤中,还有很多细胞不表达突变形式的EGFR,却大量表达正常的EGFR,它们同样会放大生长信号,造成肿瘤疯长。这时候,光靠识别EGFRvIII的CAR-T细胞还不能击退肿瘤。
怎么能再补上一拳、提高治疗效果?这时新型免疫疗法——双特异性T细胞接合器(BiTE)上场。所谓的“双特异性”,就是可以同时靶向两个分子,它就像两个分子挂钩,一个“咬住”肿瘤细胞EGFR,另一个“咬住”效应T细胞上的表面抗原,把T细胞激活,使之产生能杀伤肿瘤的蛋白质。
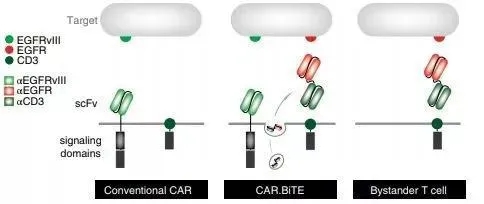
图示表达双特异性抗体的CAR-T细胞
接下来,研究团队在胶质母细胞瘤小鼠模型中检验了这种新CAR-T细胞的治疗潜力。他们在免疫缺陷型小鼠脑中植入了人脑胶质瘤细胞,然后把分泌BiTE的CAR-T细胞注入小鼠体内,同时靶向表达EGFRvIII和EGFR的肿瘤细胞予以打击。经过3周时间,80%的小鼠表现出了“完全缓解”,体内已经看不到肿瘤!
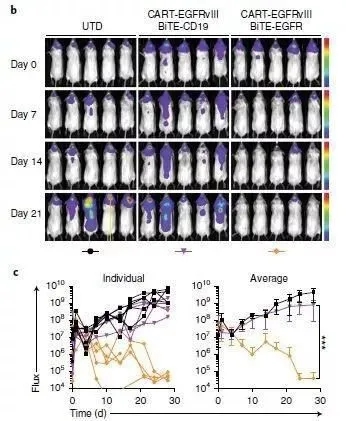
图示分泌BiTE靶向EGFR的CART-EGFRvIII细胞,让小鼠脑内的肿瘤在3周之内显著缩小甚至完全消失
此外,由于针对EGFR的BiTE会局部地在CAR-T细胞到达的部位起作用,并不影响其他表达EGFR的正常组织,这一点研究者也在小鼠身上通过移植的人体皮肤进行了检验,为这种疗法的安全性提供了数据。同时,研究者为这种CART.BiTE细胞申请了专利,并希望开展进一步的临床试验。
02、中国研发出国际首个靶向Claudin18.2的实体瘤CAR-T疗法
近两年,我们国家的实体肿瘤取得了备受世界瞩目的成绩,研发出了国际上首个靶向Claudin18.2的实体瘤CAR-T疗法。
Claudin18.2(CLDN18.2)是一种胃特异性膜蛋白,被认为是胃癌和其他癌症类型的潜在治疗靶点。基于此,中国研究人员开发了国际上首个针对 Claudin18.2 的 CAR-T 细胞。
2019 ASCO年会上,CAR-Claudin18.2 T 细胞治疗胃癌/胰腺癌的临床数据更新显示,靶向claudin18.2 CAR T细胞治疗12例转移性腺癌(胃癌7例,胰腺癌5例),未发生严重不良事件、治疗相关死亡或严重神经毒性。11例评估对象中:1例(胃腺癌)完全缓解;3例(胃腺癌2例胰腺腺癌1例)部分缓解;5例病情稳定;2例病情进展;总客观缓解率为33.3%。
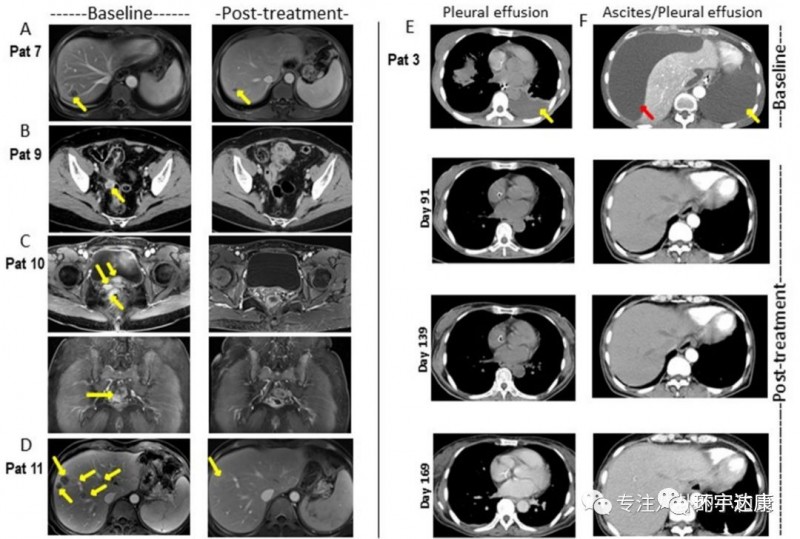
并且,CAR-Claudin18.2 T 细胞治疗胃癌的临床前研究成果显示,靶向Claudin18.2的CAR-T细胞在小鼠模型中可以完全清除胃肿瘤,且没有发生脱靶毒性。
好消息是,这项试验已经率先由国内胃肠道肿瘤享负盛名的北京大学肿瘤医院胃肠肿瘤科开展,评估自体人源化抗claudin18.2嵌合抗原受体T细胞在晚期实体瘤中的安全性及功效。
入组标准(部分)
1.年龄18~75岁,男性或女性;
2.患有病理证实的实体瘤(即晚期胃癌,食管胃交界癌和胰腺癌)并且经标准治疗失败的受试者;
3.Claudin 18.2 IHC染色阳性;
4.预计寿命>12周;
03、MUC1 CAR-T疗法显著抑制乳腺癌的生长
1.MUC28z CAR-T细胞疗法:三阴性乳腺癌
2019年5月24日,北卡罗来纳大学夏洛特分校研究人员在《Immunol》杂志上公布了在异种移植模型中,单剂量的MUC28z CAR-T细胞可显著抑制三阴性乳腺癌(TNBC)肿瘤的生长的临床研究。
超过90%的乳腺癌患者中,MUC1过表达且糖基化异常。所以与肿瘤相关的MUC1是侵袭性表型的标志物,并用作靶向免疫治疗的肿瘤新抗原。因此,研究人员采用TAB004(一种高度特异性地针对tMUC1的单克隆抗体)工程MUC28z(一种嵌合抗原受体)融合分子来生成CAR T细胞,并对这些T细胞进行了表型和功能分析,结果发现MUC28z CAR-T细胞不管是在小鼠体内还是体外均能够有效抑制TNBC肿瘤的生长,具有针对tMUC1阳性TNBC肿瘤的高治疗潜力,并且对正常乳腺上皮细胞的损害较小。
由于tMUC1在包括胰腺导管腺癌和多种乳腺癌亚型在内的大多数上皮来源的实体瘤中广泛表达,因此MUC28z CAR-T细胞可能会在靶向实体瘤方面广泛应用。
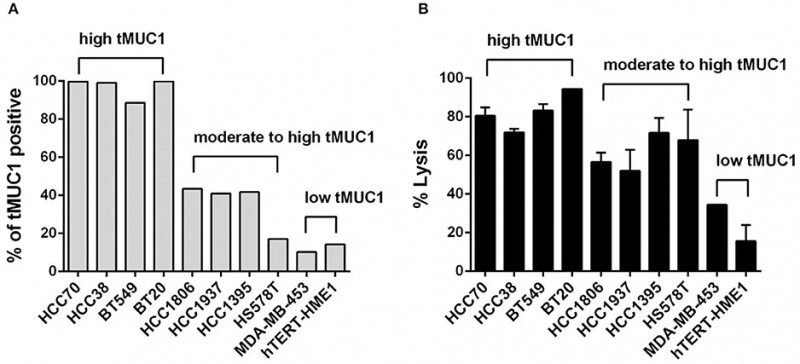
图示MUC28z CAR T细胞以抗原依赖性方式在体外裂解TNBC肿瘤细胞
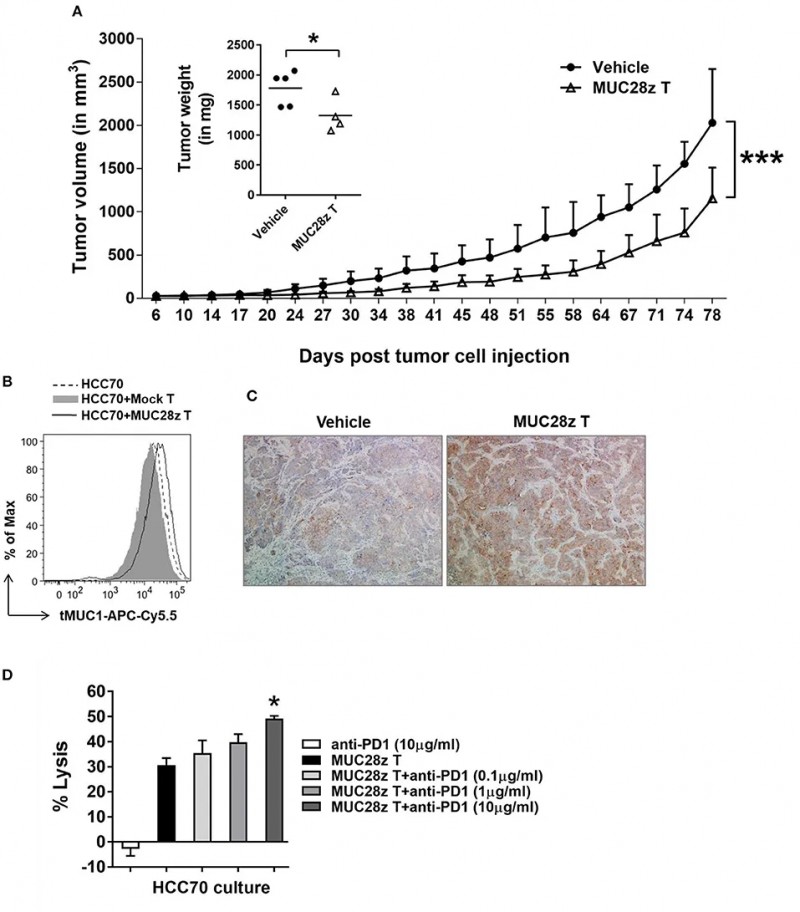
图示MUC28z CAR T细胞具有体内缩小HCC70肿瘤的长期疗效
2.huMNC2-CAR44 T细胞疗法:转移性乳腺癌
2019年6月24日,Minerva Biotechnologies(一家生物制药公司,专注于开发癌症免疫疗法)宣布,美国FDA已批准huMNC2-CAR44 T细胞疗法的研究性新药申请(IND),将对huMNC2-CAR44用于转移性乳腺癌进行临床试验,其靶向乳腺癌中MUC1(存在于超过75%的实体瘤癌细胞中)裂解产物MUC1 *生长因子受体。
之前针对MUC1的癌症疗法的尝试都失败了,因为它们是以全长的MUC1中在肿瘤细胞上被切割然后脱落并从癌细胞表面释放的那一部分为靶点。Minerva对仍然存在于癌细胞的部分MUC1(MUC1 *)、其活化配体和下一代CAR-T技术方面展开广泛专利布局。
MUC1靶点的发现推动了CAR-T细胞疗法在实体瘤中应用的进展,国内博生吉、荣泽生物等专注于细胞、免疫疗法的公司在针对MUC1靶点的CAR-T细胞疗法中也取得了不错的成果。
Minerva打算在2019年底之前开始乳腺癌的临床试验。“我们很高兴我们很快就能开始转移性乳腺癌的人体临床试验,”Minerva首席执行官Cynthia Bamdad博士说。“超过95%的乳腺癌呈MUC1 *呈阳性,这种癌症免疫疗法有可能为数千名与这种可怕疾病作斗争的患者带来希望。”
04、生存期翻倍,间皮素CAR-T细胞疗法具有潜在抗肿瘤作用
在宾夕法尼亚大学,Beatty的实验室开发了一种特异性针对间皮素的CAR。研究发现,几乎所有的胰腺癌组织都过量产生一种叫做间皮素(mesothelin)的蛋白,针对该蛋白设计的Car-T细胞,能很好地识别并攻击胰腺癌细胞。
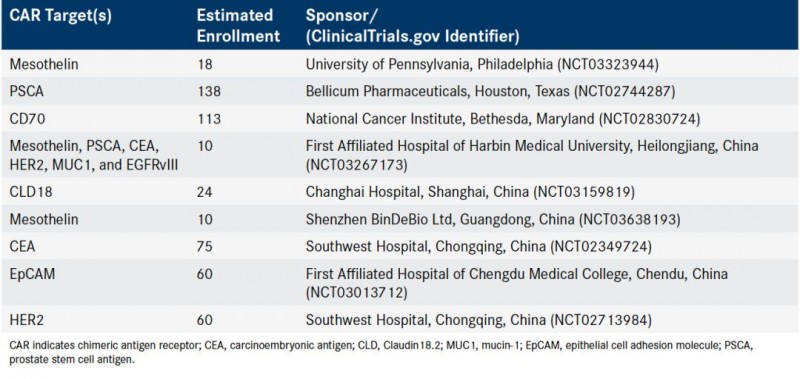
这种理论已经在小鼠试验中得到了完美的证实,接受普通T细胞治疗的胰腺癌小鼠平均生存54天。而接受间皮素引导T细胞治疗的动物平均生存96天,提高了78%!
间皮素为细胞表面糖蛋白,在多种肿瘤中高表达,如恶性胸膜间皮瘤、胰腺癌、卵巢癌及部分肺癌,在正常的胸膜、腹膜以及心包膜表面低表达,临床前研究表明针对间皮素的CAR-T细胞具有潜在抗肿瘤作用。
宾夕法尼亚大学在2019年美国临床肿瘤学会上公布的间皮素CAR-T疗法结果显示,共有6名难治性转移性胰腺导管腺癌患者成功入组,并且所有患者都接受过2次或更多次治疗。这些患者每周输注间皮素 CAR T细胞3次,总共9次剂量。结果显示有2名患者的稳定疾病,其无进展生存时间为3.8个月和5.4个月。
因此,这种新型疗法在胰腺癌患者中是具有生物学活性,这项研究仍在临床试验进行中(NCT03323944)。
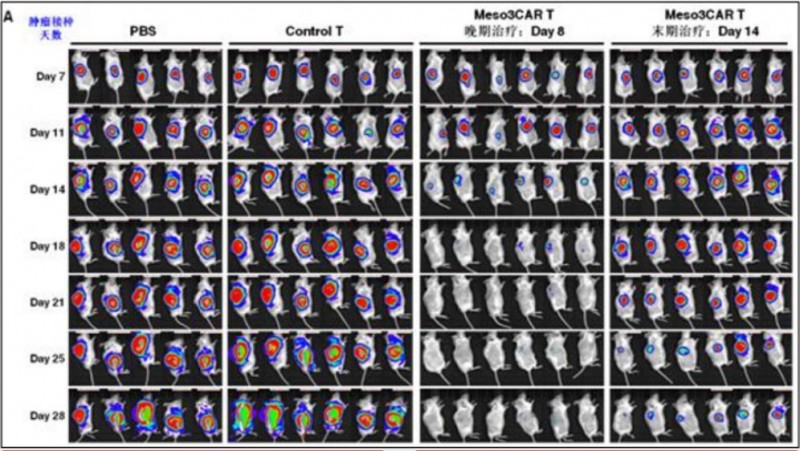
目前,国内也进行了大量的间皮素CAR-T临床研究,取得了初步成果,在小鼠实验中,接受新型间皮素CAR-T疗法的晚期卵巢癌小鼠的肿瘤出现快速消退。
05、B7-H3 CAR-T 疗法明显抑制肿瘤细胞生长,大大延长生存期
近日来自斯坦福医学院的Majzner教授团队研发了全新一代针对实体肿瘤的CAR-T疗法,这种特殊的CAR T细胞疗法之所以被誉为最有希望的疗法之一,是因为它靶向一种在很多实体肿瘤中高水平存在的抗原——B7-H3,包括一些儿童癌症。
通过研究筛选了388例儿童肿瘤的标本进行检测。结果显示,84%的样本(肿瘤细胞)中都存在B7-H3。其中70%的样本中B7-H3的含量都非常高。包括骨尤文肉瘤、横纹肌肉瘤、肾母细胞瘤、神经母细胞瘤和髓母细胞瘤及脑干肿瘤(DIPG)等癌症中,肿瘤细胞表面都存在非常多的B7-H3。
通过基因编辑技术形成新一代CAR-T细胞——B7-H3 CAR-T在小鼠身上展开了试验。他们将人体的肿瘤细胞移植到小鼠体内,形成多个儿童癌症的小鼠模型。并对这些小鼠模型进行B7-H3 CAR-T细胞治疗。与对照组相比,B7-H3 CAR-T 明显抑制了小鼠肿瘤细胞的生长,大大延长了小鼠的生存期。经过治疗,实验组小鼠的存活率几乎达到了100%。
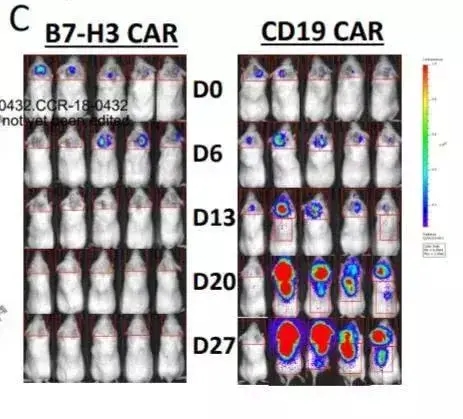
左边为接受B7-H3 CAR-T治疗小鼠;右边为CD-19 CAR-T治疗小鼠;图中红蓝色为小鼠肿瘤
迄今为止,关于B7-H3 CAR T细胞疗法的数据令人鼓舞,并且没有报告治疗相关的严重副作用。目前这项试验正在进行Ⅰ期人体临床试验,招募神经系统肿瘤及髓母细胞瘤等儿童肿瘤,若想了解详情请咨询全球肿瘤医生网。
机不可失,众多CAR-T疗法临床招募进行中
除了上述突破性的临床研究进展,目前国内各大医院正在积极进行各类肿瘤的CAR-T临床研究。
| 试验药物 | 实验名称 | 招募条件 | 实验地点 |
| CAR-T细胞 | 难治性/复发性B细胞恶性肿瘤中脐带血衍生的CAR-T细胞 | B细胞淋巴瘤 | 河南省肿瘤医院 |
| BCMA CAR-T细胞 | 难治性和复发性多发性骨髓瘤患者的BCMA纳米抗体CAR-T细胞 | 复发和难治性多发性骨髓瘤 | 广东深圳 |
| 靶向HER2、间皮素、PSCA、MUC1、Lewis-Y或CD80/86的CAR-T细胞 | HER2/间皮素/Lewis-Y/PSCA/MUC1/PD-L1/CD80/86-CAR-T细胞免疫疗法 | 肺癌 | 中山大学附属第一医院 |
| 靶向EpCAM的CAR-T细胞 | 腹膜内输注EpCAM CAR-T细胞在晚期胃癌腹膜转移中(WCH-GC-CART) | 胃癌 | 四川大学华西医院 |
| CD19/CD20双特异性CAR-T细胞 | B细胞淋巴瘤中CD19/CD20双特异性纳米抗体衍生的CAR-T细胞 | ||
| 靶向PC-T细胞的GPC3和/或TGF β | 靶向PC-T细胞的GPC3和/或TGF | 肝细胞癌 | 中山大学附属第一医院 |
| CAR-T/TCR-T细胞免疫疗法 | 自体CAR-T/TCR-T细胞免疫疗法治疗实体恶性肿瘤 | 食管癌、肝癌、胃癌 | |
| CAR-T细胞免疫疗法 | CAR-T细胞免疫疗法 | 肝细胞癌 | 南京大学医学院附属南京鼓楼医院 |
| 肉瘤特异性CAR-T细胞 | 针对肉瘤的第四代安全工程CAR | 肉瘤 | 广东深圳 |
| 间皮素导向的CAR-T细胞 | PC调节间皮素阳性多发实体瘤 | 成人实体瘤 | 中国人民解放军总医院 |
| MUC-1 CAR-T细胞免疫疗法 | MUC-1 CAR-T治疗肝内胆管癌 | 肝内胆管癌 | 浙江大学附属第二医院 |
| EGFR806特异性嵌合抗原受体(CAR)T细胞 | EGFR阳性的复发性或难治性小儿中枢神经系统肿瘤的EGFR806 | 小儿中枢神经系统肿瘤 | 西雅图儿童医院 |
在细胞疗法出现之前,包括晚期胃腺癌、胰腺癌在内的实体瘤通常是采用手术、放化疗进行治疗,其中胃腺癌的发生率占胃恶性肿瘤的95%,胰腺癌更是常见肿瘤中恶性程度最高的肿瘤,中位生存期和5年生存率都远远低于其他肿瘤,号称“癌中之王”。但是大部分患者术后会出现局部复发或转移,另外,这类恶性肿瘤对放化疗的敏感性也不高。所以基于目前的标准疗法,治疗效果并不理想,而且预后极差。免疫疗法的出现,将给更多的晚期患者带来长期生存的希望和奇迹。
我们坚信,在完善的细胞免疫监管制度出台后,国家将放开细胞免疫治疗的大门造福更多的癌症患者,我们国家的细胞免疫疗法也将登上国际舞台!
目前这项技术正在国内招募各类晚期实体肿瘤患者,想参加的可以向全球肿瘤医生网医学部申请。
参考文献
https://www.healio.com/hematology-oncology/neuro-oncology/news/online/%7B6fafc1ef-3edc-4599-8159-230c1771164b%7D/car-t-cells-show-potential-for-treatment-of-pediatric-solid-tumors
https://www.frontiersin.org/articles/10.3389/fimmu.2019.01149/full#supplementary-material
https://clincancerres.aacrjournals.org/content/25/8/256
https://www.biospace.com/article/releases/minerva-biotechnologies-announces-fda-acceptance-of-ind-application-for-humnc2-car44-t-cells-to-treat-metastatic-breast-cancer/
https://www.firstwordpharma.com/node/1649108#axzz5rpYDX3hI

































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城