非小细胞肺癌新药,肺癌临床试验招募进行中
近年来,被誉为癌症治疗“第四支柱”的靶向治疗发展迅速,越来越多的新药面世,为患者争取到了更长的生存期与更好的生活质量。
除了靶向药物研发最多的EGFR靶点与疗效惊人的“钻石突变”ALK,ROS1也是肺癌患者、尤其是非小细胞肺癌患者应当关注的重要突变之一。这个突变的发生率较低,仅1%~2%,但整体疗效较好,且在研药物种类繁多,患者生存希望比较乐观。
认识ROS1融合突变
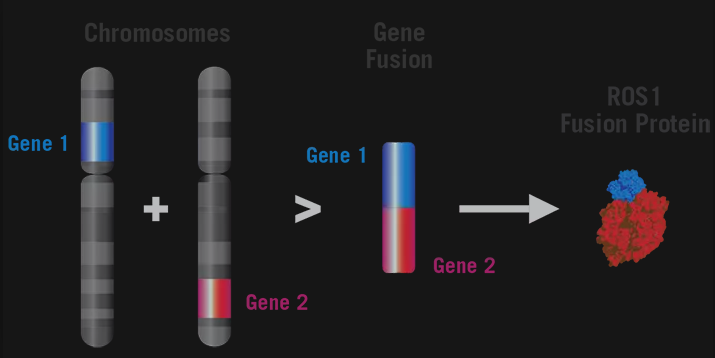
ROS1融合突变是一类泛癌种的致癌因素,在多癌种中表达,包括肺癌、卵巢癌、肉瘤、胆管癌等。在非小细胞肺癌中,ROS1突变的发生率约为2%,致病类型多为腺癌,通常发生于相对年轻的无吸烟史患者。
全称:c-ros肉瘤致癌因子-受体酪氨酸激酶(ROS proto-oncogene 1 , receptor tyrosine kinase)
占比:占非小细胞肺癌的1%~2%,亚洲患者中发生率较高
突变类型:融合突变
特点:
1. 更多地发现于无吸烟史患者及女性患者,平均年龄49.8岁,占所有肺癌患者的1%~2%,在亚洲患者和Ⅳ期患者中发生率较高;
2. 因ROS1突变而导致的非小细胞肺癌病理类型通常为腺癌,占肺腺癌患者的3.1%;
3. ROS1突变具有较强的排他性,极少与EGFR突变同时出现(0.5%),很少与KRAS突变同时出现(1.8%),基本不会与ALK突变同时出现;
4. 由于ROS1结构与ALK结构相似,因此部分靶向药物可同时用于ALK突变和ROS1突变患者。
ROS1靶点靶向药物疗效确切,屡获认可
由于ROS1为非小细胞肺癌患者重要的突变基因之一,临床上针对这一靶点的药物研究进展迅速。在美国,多种临床药物已经获得FDA批准或NCCN指南推荐。
克唑替尼(Crizotinib)
2016年3月11日,克唑替尼获得FDA批准用于治疗ROS1阳性的转移性非小细胞肺癌,客观缓解率达到72%,中位缓解持续时间17.6个月,中位无进展生存期19.2个月;针对东亚患者群体,克唑替尼治疗的客观缓解率为71.1%,中位缓解持续时间19.7个月,中位无进展生存期15.9个月。但克唑替尼无法通过血脑屏障,对于发生脑转移的患者效果较差。
目前,克唑替尼已经获批在国内上市。
恩曲替尼(Entrectinib)
2019年8月15日,恩曲替尼获得FDA批准用于治疗ROS1阳性的转移性非小细胞肺癌或NTRK融合的多种实体瘤患者,其治疗非小细胞肺癌患者客观缓解率达到77.4%,完全缓解率5.9%,中位缓解持续时间24.6个月;相比克唑替尼,恩曲替尼能够经过血脑屏障,对于发生脑转移的患者治疗总缓解率为55.0%。
劳拉替尼(Lorlatinib)
目前暂未获得FDA批准,但已经获得了NCCN指南推荐。劳拉替尼为三代TKI抑制剂,可针对ALK突变及ROS1突变的患者。治疗ROS1突变的非小细胞肺癌患者,客观缓解率为62%,疾病控制率90%,中位无进展生存期21个月,中位疾病控制时间25.3个月。同时,劳拉替尼也具有较好的通过血脑屏障的能力,可以应用于发生脑转移的患者。
色瑞替尼(Ceritinib)
目前暂未获得FDA批准,但已经获得了NCCN指南推荐。色瑞替尼治疗ROS1阳性非小细胞肺癌患者的客观缓解率为62%,中位缓解持续时间为21.9个月,中位总生存期为24个月;对于此前未接受过克唑替尼治疗的患者,中位无进展生存期为19.3个月;对于曾接受克唑替尼治疗、但疾病持续进展或耐药的患者,中位无进展生存期为9.3个月。同时,色瑞替尼也可以通过血脑屏障。但色瑞替尼的不良反应较严重,常见不良反应包括腹泻(78%)、恶心(59%)、厌食(56%)等。
根据版的NCCN指南(2020.v1),对于检测到ROS1重排阳性的患者,推荐的用药方案如下:
| 一线全身治疗前发现ROS1重排 | 一线治疗期间发现ROS1重排 | 初始治疗期间检测发现疾病进展 | |
| 用药推荐 | 首选克唑替尼或恩曲替尼,可选色瑞替尼 | 完成计划的治疗,或中断当前治疗方案;首选克唑替尼或恩曲替尼,可选色瑞替尼 | 换用劳拉替尼或全身治疗方案 |
国际:ROS1靶点药物研发快速进展
国际上对于ROS1靶点药物的研究持续进展,许多新药已经在Ⅰ期临床试验或临床前试验中被验证为有效,有望尽快投入后期临床试验之中。
TPX-0005
TPX-0005(repotrectinib)是一种靶向ALK、ROS1和TRK融合突变的抑制剂类药物,作为单药使用治疗ROS1阳性患者的Ⅰ/Ⅱ期试验结果显示,对于ROS1(+)患者,整体缓解率超过70%;患者对于药物治疗整体耐受性较好,与治疗最相关的不良事件为头晕、消化不良、感觉异常、便秘和疲劳等,2~3级不良反应在减药或停药后可消失或缓解。
DS-6051b
DS-6051b由日本公司研制,是一类靶向ROS1及NTRK的抑制剂类药物,在小鼠实验中显示出了良好的效果。通过口服给药,小鼠的肿瘤病灶明显缩小,并且疗效能够持续很长一段时间。
但对于国内患者来说,无论是已经经过FDA批准上市、却暂未进入国内市场的药物,还是获得NCCN指南推荐、国内却暂无获取途径的药物,或者正在进行临床试验的外国药物,都显得有些遥不可及。幸而,国内针对ROS1靶点的靶向药物进展也十分迅猛,相关实验正在有条不紊地开展之中。
国内:TQ-B3101临床招募进行中!
目前获批进入国内市场的ROS1靶点靶向药物仅有克唑替尼,幸而国内对ROS1靶点的靶向药物研发也在快速发展,由中国医学科学院肿瘤医院牵头,共28家临床机构参与的评价TQ-B3101胶囊治疗ROS1阳性非小细胞肺癌的疗效和安全性Ⅱ期试验正在招募患者!
TQ-B3101为正大天晴药业集团研制并申报的小分子靶向抑制剂类药物,针对ROS1靶点,目前已经获得国家药品监督管理总局的批准(批件号:2016L06653),并通过伦理审查。
这是一项多中心、单臂试验,所有参与试验的患者均可获得相同的药物治疗。目前,TQ-B3101的前期试验结果暂未公布,但单臂试验获批门槛较高,必须为疗效相当显著的药物,因此本次试验的结果将非常值得期待。
主要纳入标准
1、患者年龄≥18岁;
2、ECOG评分0~1分,预期生存期超过3个月;
4、通过组织学或细胞学证明诊断为局部晚期或转移性非小细胞肺癌;
5、提供ROS1阳性书面报告,或在入组前提供组织学标本、活检组织标本送中心实验室进行检测,并确认为ROS1阳性;
6、既往接受过不超过2个化疗方案(若接受超过2个化疗方案,则需再次进行检测,且检测结果确认为ROS1阳性);
7、距离首次研究用药前28天,经影像学证实,至少存在1处脑部病灶除外的可评价的靶病灶;
8、主要器官功能正常。
主要排除标准
1、EGFR(+);
2、既往接受过克唑替尼或任何其他已经上市的或正在进行临床研究的ROS1抑制剂治疗;
3、具有影响口服药物的多种因素;
4、其他严重伴随疾病等。
扫码申请入组



































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城