什么是免疫治疗法(PD-1/PD-L1),国内上市的免疫治疗药物有哪些,免疫治疗法(PD-1/PD-L1)副作用
免疫治疗被誉为继手术、化疗之后癌症治疗的第三大革命性突破,在2013年《科学》杂志评选出的年度十大科学突破排行当中,免疫治疗高居榜首。这种通过调动患者自身免疫能力抵抗并清除癌症的治疗方案,成为了癌症治疗的全新突破点。
免疫检查点抑制剂治疗是免疫治疗中重要的组成部分,尤其适用于实体肿瘤,受到了医疗界的重视。其中最具代表性、研究成果最丰富的,是针对PD-1/PD-L1靶点的免疫治疗药物。
在本期专家视点栏目中,全球肿瘤医生网邀请到了北京大学肿瘤医院消化肿瘤内科主任、医学博士、博士生导师张小田教授,从专家视角、用通俗的语言深入浅出地讲述,关于PD-1/PD-L1的那些事儿。
什么是免疫治疗法(PD-1/PD-L1)
相信许多患者都听说过,或者是使用过PD-1/PD-L1抑制剂药物。以PD-1/PD-L1抑制剂的发展速度与规模,即使是现在没有使用过的患者,未来也很有可能会接触到这类药物。
与常规的化疗、放疗等不同,免疫治疗并不依靠药物或射线对于癌细胞造成杀伤,而是通过调控患者自身的免疫免疫能力,借免疫细胞之手攻击癌细胞。其疗效有目共睹,与之相伴的通常都是“超级幸存者”的故事。
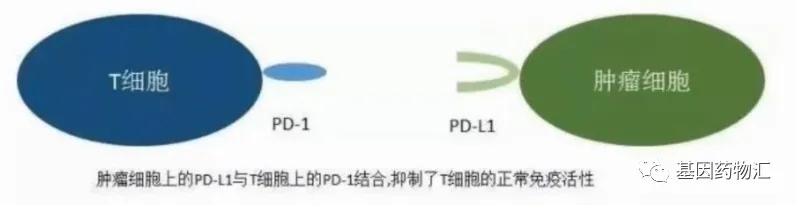
为了避免伤及正常的人体细胞,免疫T细胞上存在一个“刹车”——PD-1。凭借这一受体,T细胞能够将携带PD-L1受体的细胞识别为正常细胞。
但癌细胞同样也会通过大量表达PD-L1受体来关闭T细胞的“刹车”,将自己“伪装”成为正常细胞,进而逃避人体免疫系统的杀伤。

PD-1/PD-L1抑制剂能够分别特异性地与这两种受体结合,阻断这一“刹车”过程。通过恢复T细胞被肿瘤细胞关闭的“刹车”功能,人体免疫系统杀灭肿瘤细胞的途径恢复,T细胞能够正常行使免疫功能,消灭肿瘤细胞。
因此准确地说,通过免疫检查点抑制剂药物进行的免疫治疗并非“增强人体的免疫能力”,而是“使失常的免疫功能恢复正常”。
当然,T细胞想要正常地杀灭肿瘤细胞,其实是有很多关键前提的,包括T细胞的数量是否充足、T细胞能不能进入肿瘤病灶的内部、有没有必要的免疫因子或影响这一过程的抑制因子存在等等。每一个关键前提都可能引起一种免疫疗法,我们今天讨论的PD-1/PD-L1抑制剂关注的只是这一对抑制因子。
国内外已上市的PD-1/PD-L1抑制剂(单克隆抗体)药物有哪些
目前各种临床研究都证实了免疫治疗在实体瘤治疗中的效果,相关研究发展迅速,许多药物及适应症已经获批临床应用
国外上市的免疫治疗药物
PD-1:派姆单抗,纳武单抗
PD-L1:度伐利尤单抗,阿特珠单抗
国内上市的免疫治疗药物
PD-1:特瑞普利单抗、信迪利单抗、卡瑞丽珠单抗、替雷利珠单抗
目前,国内尚无PD-L1抑制剂获批。
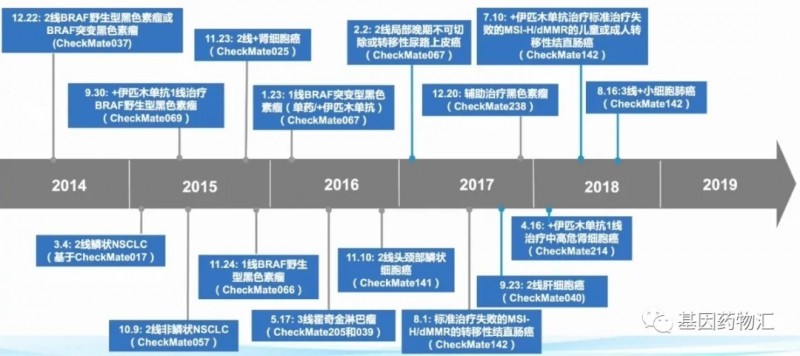
事实上,当前临床上各类免疫药物的适应症发展及获批速度都很快。以纳武单抗为例,自2014年获批首个适应症,到2018年,5年的时间内纳武单抗共有16个适应症获批,横跨八大癌种,包括常见的肺癌、结直肠癌、肝癌、肾癌、黑色素瘤等等。
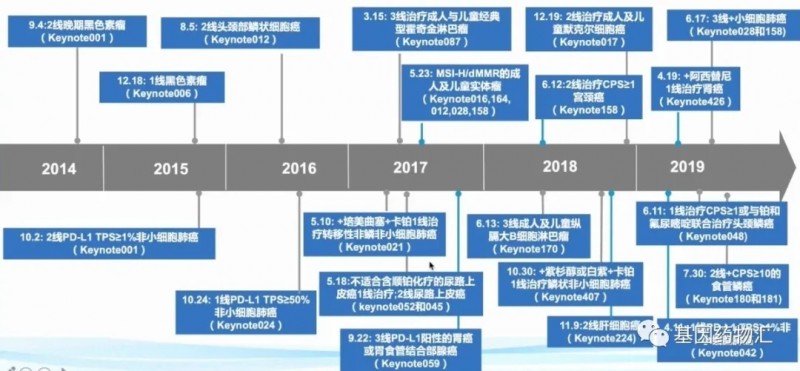
派姆单抗的适应症发展同样迅速。与纳武单抗相似,派姆单抗的首个获批适应症也是黑色素瘤。从2014年至2019年共20个适应症获批,横跨十三大癌种及实体瘤,包括常见的肺癌、胃癌、肝癌、肾癌、尿路上皮癌、宫颈癌、食道癌等。
在我国,免疫疗法的起步虽稍晚,但发展同样迅速。外国研发的药物在我国获批的适应症及临床试验较少,但仍然覆盖了许多癌种。
| 获批药物 | 公司 | 适应症 | 获批时间 | 基于研究 |
| 纳武单抗(Nivolumab) | 百时美施贵宝(BMS) | 2线非小细胞肺癌 | 2018-6-15 | CM078 |
| 纳武单抗(Nivolumab) | 百时美施贵宝(BMS) | 2线头颈部鳞癌 | 2019-10-8 | CM141 |
| 帕博利珠单抗(Pembrolizumab) | 默沙东(MSD) | 2线黑色素瘤 | 2018-7-25 | KN151 |
| 帕博利珠单抗(Pembrolizumab) | 默沙东(MSD) | 1线非鳞非小细胞肺癌 | 2019-3-29 | KN189 |
| 帕博利珠单抗(Pembrolizumab) | 默沙东(MSD) | 1线TPS≥1%非小细胞肺癌 | 2019-10-8 | KN042 |
| 帕博利珠单抗(Pembrolizumab) | 默沙东(MSD) | 1线鳞状非小细胞肺癌 | 2019-11-29 | KN407 |
| 德瓦鲁单抗(Durvalumab) | 阿斯利康(AZ) | 局部晚期非小细胞肺癌 | 2019-12-9 | Pacific |
| 阿替利珠单抗(Atezolizumab) | 罗氏(Roche) | 三期临床:一线/二线非小细胞癌,一线三阴性乳腺癌,尿路上皮或非上皮癌等 | 暂未获批 |
除进口药物以外,我国自主研发的四款PD-1单抗也展露出了不错的潜力,多在2018~2019年间获批上市。
| 获批药物 | 公司 | 适应症 | 获批时间 | 基于研究 |
| 特瑞普利单抗(Toripalimab) | 君实 | 既往接受全身系统治疗失败的不可切除或转移性黑色素瘤 | 2018-12-17 | CT4 |
| 信迪利单抗(Sintilimab) | 信达 | 至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤 | 2018-12-27 | ORIENT1 |
| 卡瑞丽珠单抗(Camrelizumab) | 恒瑞 | 至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤 | 2019-5-31 | NCT031554 |
| 替雷利珠单抗(Tislelizumab) | 百济 | 复发或难治性经典型霍奇金淋巴瘤 | 2019-12-27 | 多中心II期临床研究 |
除已经获批的适应症,多项其他适应症的药物临床试验已经获得了国家食品药品监督管理局的批准,开始招募患者。以阿特珠单抗为例,其临床试验的癌种包括肺癌、乳腺癌、肝癌、头颈鳞状细胞癌、尿路上皮癌等。
| 登记号 | 药物 | 适应症 | 分期 |
| CTR20170731 | 纳武单抗+伊匹木单抗 | 实体瘤 | I期 |
| CTR20180914 | 纳武单抗+伊匹木单抗 | 非小细胞肺癌 | II期 |
| CTR20180929 | 纳武单抗+伊匹木单抗 | 早期非小细胞肺癌 | II期 |
| CTR20170541 | 纳武单抗+伊匹木单抗 | EGFR突变阳性非小细胞肺癌 | II期 |
| CTR20170340 | 纳武单抗+伊匹木单抗 | 非小细胞肺癌 | II期 |
| CTR20170694 | 纳武单抗+伊匹木单抗 | 广泛期小细胞肺癌 | II期 |
| CTR20170913 | 纳武单抗+伊匹木单抗 | 胸膜间皮瘤 | II期 |
| CTR20180252 | 纳武单抗+伊匹木单抗 | 尿路上皮癌 | II期 |
| CTR20180072 | 纳武单抗+伊匹木单抗 | 局限性肾细胞癌 | II期 |
| CTR20171227 | 纳武单抗+伊匹木单抗 | 晚期食管鳞状细胞癌 | II期 |
| CTR20170371 | 纳武单抗+伊匹木单抗 | 胃癌或胃食管交界处癌 | II期 |
| CTR20160926 | 德瓦鲁单抗+曲美木单抗 | 实体瘤 | I期 |
| CTR20170485 | 德瓦鲁单抗+曲美木单抗 | 不可行手术切除的肝细胞癌 | II期 |
目前,免疫治疗的发展方向不止在于拓展更多的适应症,也在于寻找一种能够更加有效地利用免疫治疗优势的治疗方案。目前临床上已经获批的免疫疗法通常应用于后线及末线治疗,而当前临床研究的思路之一,就在于将免疫疗法的应用时机从后线推进至新辅助治疗,即术前的全身治疗方案;或在对于免疫治疗并不敏感的非优势治疗人群中,采用免疫治疗与其他治疗手段联合的方案,提升治疗效果等。
当然,除了针对已有药物的进一步研究,目前我国药企在新药研发方面同样走在国际前列。再加上外国研发药物拓展中国市场,已经进入临床或开始试验的免疫检查点抑制剂药物多达31种。
| BLA | III期 | II期 | I期 | |
| PD-1 | 替雷利珠单抗(Tislelizumab)(百济) |
1.Cemiplimab(赛诺菲) 2.HLX-10(复宏汉霖) 3.SCT-I10A(神州细胞) 4.AK-105(康方) |
1.GLS-010(誉衡药业) 2.GB226(嘉和生物) 3.HX008(翰中) 4.BAT-1306(百奥泰生物) 5.PDR-001(诺华) |
1.LZM-009(丽珠、翰思生物) 2.609A(三生国健) 3.QL1604(齐鲁) 4.HAB21(苏州斯坦维) 5.SG001(石药) 6.F520(山东新时代) 7.CS1003(基石) |
| PD-L1 | 阿替利珠单抗(Atezolizumab)(罗氏) |
1.CS1001(基石) 2.KN035(思路迪) 3.SHR-1316(恒瑞医药) 4.TQB2450(正大天晴) 5.Agelumab(默克) |
1.SHR-1316(恒瑞) 2.KLA-167(四川科伦) 3.GR-1405(智翔金泰) 4.LP002(厚德奥科) |
1.MSB-2311(迈博斯) 2.HS636(海正生物) 3.ZKAB001(兆科肿瘤) 4.P003(白帆生物) |
从Ⅰ期到Ⅱ期Ⅲ期,免疫检查点抑制剂药物的临床试验可以说是玲琅满目。但对于患者来说,这些免疫治疗的临床试验是否是值得尝试的呢?
对此,张小田教授指出,只要有机会、有适合的新药临床试验,除非存在病情进展迅速、时间不允许,或者就医困难、难以照料等特殊情况,否则患者都应当考虑参加。
临床研究很可能能够为患者提供新的治疗策略。即使是部分设置了对照组的临床试验,没能被选入接受新药治疗的试验组,对照组患者接受的也是当前临床上疗效最为确切的标准治疗方案。
张小田教授给广大患者们的建议是,要积极与自己的主管医生交流,积极了解临床研究,不要拒绝临床研究。
哪些患者适合使用PD-1/PD-L1抑制剂,什么时候应当使用PD-1/PD-L1抑制剂
从医生的角度来说,患者是否需要使用、或者什么时间使用PD-1/PD-L1抑制剂是需要结合实际情况作出判断的。即使是针对同一靶点的药物,治疗不同特征的患者的疗效也会存在一定的差异。但整体来说,适合应用PD-1/PD-L1抑制剂的患者应当具备一些基本的特征。
MSI-H/dMMR;
PD-L1高表达;
TMB高;
EBER阳性。
当然,也有一些癌种,并不需要关注MSI、PD-L1等的表达水平。如肾癌及黑色素瘤等,患者不需要存在MSI-H或PD-L1高表达,也可以从免疫治疗中获益。
而每一款PD-1/PD-L1抑制剂都有其独特的适应症,临床应用时,应当在完全了解患者疾病特点的情况下综合选择。
派姆单抗:MSI-H/dMMR晚期胃癌的一线或二线治疗及PD-L1 CPS≥1晚期胃癌病人的三线治疗;
纳武单抗:晚期胃癌病人的三线治疗,是首个也是目前唯一一个与化疗联合用于胃癌及食管癌一线且临床结果阳性的治疗药物;
信迪利单抗、卡瑞丽珠单抗、替雷利珠单抗、特瑞普利单抗:可在纳武单抗、派姆单抗不可及时考虑应用。
张小田教授指出,除了这些已经明确的适应症,在应用免疫治疗时也有一些跨适应症的尝试。比如某些适应症在国外已经获批,但国内尚未获批,保证安全性的前提下、在其他进口产品不可及的情况下,可以结合患者的实际情况酌情考虑应用。
同时,张小田教授也强调,在进行这种跨适应症的应用时,首先必须考虑我国人群与外国人群的差异,不能照搬。如纳武单抗治疗胃癌,在我国人群中的临床研究数据较好,但在高加索人种的研究数据并不理想,这就是人种差异带来的疗效差异。
国内外的PD-1/PD-L1抑制剂产品有哪些差别
目前并没有非常明确的两款免疫治疗药物之间疗效对比的研究。各国研发的PD-1/PD-L1抑制剂药物,都会根据本国患者群体的特点而存在一定的差异。由于国内外的肿瘤疾病的流行病学特点不同,因此许多临床试验在国内外人群中的结果并不完全相同。
从适应症来看,美国的PD-1单抗研究主要针对肺癌,而国内的适应症则主要从黑色素瘤和霍奇金淋巴瘤开始。受限于临床试验样本类型,目前许多进口药物对于中国患者的临床研究数据并不充分。对于某些特定的疾病或适应症,国产PD-1/PD-L1抑制剂药物的疗效甚至会优于进口药物。
总得来说,国内或国外药物的选择原则是:综合考虑药物获批的适应症、主治医生的临床经验、临床研究及其数据进行选择。
使用过进口PD-1/PD-L1抑制剂,可以再换用国产的同类药物吗
原则上来说,作用机制相同的药物,并不推荐在耐药后换用。比如同样作用于PD-1靶点的派姆单抗和纳武单抗,由于其作用机理相同,耐药后换用另一种的疗效可能并不会很好。
目前没有证据表明针对同一靶点的药物治疗同一疾病的疗效可能存在差异。没有国产药与国产药之间的对比试验,没有进口药与国产药之间的对比,也没有国产药与进口药之间的对比,因此疗效会更好或更差的结论都完全没有任何临床数据来支撑。可以说,任何追求使用进口药或国产药的做法都是缺乏理论依据的。
但作用于不同靶点的药物之间是有可能考虑换用的。针对PD-1和PD-L1抑制剂之间并不存在交叉耐药,对于其中一类发生耐药的话,可以结合临床实际与临床经验考虑换用另一类药物。
PD-1/PD-L1抑制剂治疗需要多长时间
接受PD-1/PD-L1治疗后存在两种情况,一种是用药后不久,影像学检查等结果发现疾病进展,一种是治疗持续有效。
用药后不久发现疾病进展,此时应当考虑这种影像学检查显示的“进展”是真性进展还是假性进展。发生假性进展时,患者继续接受免疫治疗,病灶会在进展一段时间之后开始缩小。如果因为假性进展而放弃使用免疫治疗,显然患者会错失治疗的机会。
PD-1/PD-L1抑制剂治疗持续有效,目前的研究证据支持在持续治疗2年后停药。
此外,PD-1/PD-L1抑制剂也可应用于围手术期的辅助治疗。对于不同的癌种、不同的分期,辅助治疗的推荐时间也不同。整体来说,大部分情况下推荐的治疗时间为1年。
PD-1/PD-L1抑制剂的常见副作用有哪些
大家可能都听过一句话,除了头发和牙齿,人身体的每个地方都有免疫细胞。有免疫细胞,自然就可能引起免疫相关的反应。因此,PD-1/PD-L1抑制剂的副作用种类非常多。
常见副作用:乏力、输注相关反应、腹泻、结肠炎、肝毒性、肺炎、自身免疫性甲状腺疾病(甲减、甲亢)垂体炎、肾上腺功能减退症、1型糖尿病、急性肾损伤、淀粉酶及脂肪酶升高等;
其他副作用:吉林巴利综合征等神经系统综合征、心脏毒性、红细胞再生障碍性贫血、中性粒细胞减少、血小板减少、获得性血友病、眼部炎症、风湿性疾病和肌肉骨骼受累等。
大多数患者自身免疫性疾病的发作是相对轻度的,只有少部分患者需要暂停药物治疗。对于患者来说,不论在治疗中发生怎样的副作用,都应当及时与主治医生沟通,避免造成不可挽回的后果。
一旦发生严重的副作用,首先自然应当考虑停药。但停药之后是否能够再次应用PD-1/PD-L1抑制剂,就必须结合患者的自身情况以及不良反应类型进行谨慎评估了。
PD-1/PD-L1抑制剂耐药后应当如何治疗
目前,临床上对于PD-1/PD-L1抑制剂耐药后的治疗方案主要有四种思路。
免疫联合化疗:一些研究认为,免疫治疗耐药后再次接受化疗,化疗的疗效可能会更加显著;
免疫联合放疗;
免疫联合抗血管生成治疗;
免疫联合免疫治疗:
1.PD-1耐药之后可换LAG-3抗体和CTLA-4抗体继续免疫治疗,先用PD-1无效并不影响CTLA-4抗体的使用;
2.PD-1联合CPI-444可以提高肿瘤中免疫细胞的活性;
3.PD-1耐药之后更换药物或继续使用原药物仍然可能延长生存期。
当然,目前免疫治疗尚属于比较新的研究领域,对于包括CTLA-4等在内的新兴靶点,以及免疫检查点抑制剂与其他治疗手段联合应用的疗效研究仍处于进行阶段。究竟哪种方案的效果更好、更能延长患者的生存期,还需要更多的临床研究数据。
使用PD-1/PD-L1抑制剂前的注意事项有哪些
采用免疫治疗,患者必须具备一定的免疫能力,基础状况太差、合并疾病严重等的患者可能无法从免疫治疗中获益。除此以外,接受过器官移植或患有自身免疫疾病的患者可能因为免疫治疗而产生严重的排斥反应,甚至导致死亡。
除此以外,患者不仅应当关注自身是否拥有免疫治疗可能获益的标志物(如MSI-H、PD-L1高表达等),也应当关注是否存在免疫治疗效果不佳的标志物,或可能因免疫治疗导致超进展的标志物。
目前比较明确的免疫治疗禁忌症包括:
进入终末期、卧床不起的患者;
有急性细菌感染,病情尚未控制的患者;
做过肝移植、肾移植的患者;
有系统性红斑狼疮、白塞病、干燥综合征、血管炎等自身免疫病,尚未控制的患者;
携带MDM2扩增、EGFR突变、JAK突变等可以首选靶向治疗的患者。
除此以外,接受免疫治疗前,患者还应当完善必备的检查项目,包括血常规、肝肾功、电解质、凝血、甲状腺功能,心电图、腹部B超、胸部X线等。
张小田教授对癌症患者的寄语
张小田教授说,目前国内最负盛名的几个大的肿瘤中心,都有许多新药临床研究。
教授指出,我们应当具备底线思维的能力,立足最低点,追寻最好的结果。目前临床上的治疗方案很多,新的治疗方案也很多。患者绝对不要轻易地说出放弃,而是要尽量追寻到可能有用的新药物。
我国免疫治疗领域发展迅速,与之相应的是大量的新药临床试验问世。不同的临床研究处于不同的阶段,研究的目的不同,患者能够接受到的治疗也不同。患者们应当在入组试验前与专家进行充分的沟通,透彻地了解自己即将接受的试验的设置情况、分组情况,了解这种药物在前期试验或临床前研究中的表现,再结合自身的病情,在综合考虑各种情况之后作出判断。
当然,在接受免疫治疗前必须明确的一件事是,免疫治疗不仅有完全缓解的可能,也存在一定的超进展风险。患者必须在进行充分的检查之后再开始接受治疗,并且在治疗过程中与医生保持沟通,将风险降低到最小。

张小田
医学博士,教授,博士生导师
北京大学肿瘤医院消化肿瘤内科主任医师
中国临床肿瘤学会 青年专家委员会 主任委员
中国抗癌协会胃癌专业委员会青年委员会 主任委员
中国抗癌协会肿瘤支持治疗委员会 秘书长
中国研究型医院学会精准医学与肿瘤MDT专业委员会 副主任委员
中国老年学会老年肿瘤专业委员会胃肠分委会 常务委员







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城