钻石突变NTRK基因融合突变,NTRK抑制剂,NTRK靶向药物有哪些,NTRK临床试验招募中
2018年11月,整个医疗界和癌友圈都为一款FDA新批准上市的抗癌药物沸腾,这就是全球首个不区分肿瘤来源用于初始治疗的靶向药--Vitrakvi ®(拉罗替尼,larotrectinib),用于成人和小儿具有神经营养受体酪氨酸激酶(NTRK)基因融合的实体瘤治疗。这款新型的抗癌药物每年可以帮助成千上万的人,它已经给世界各地的患者来了新的希望。各类NTRK融合癌症接受治疗后奇迹重生!
婴儿纤维肉瘤TPM3-NTRK1融合病灶全部消退
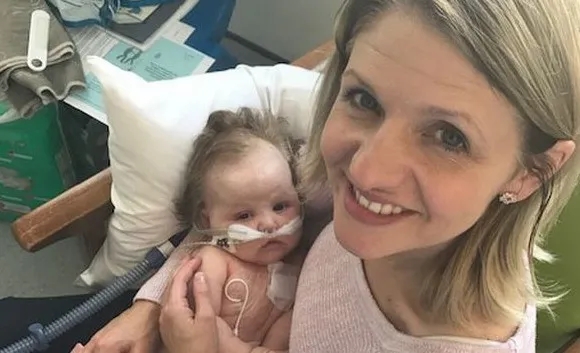
胶质母细胞瘤ETV6-NTRK3融合肿瘤快速消退
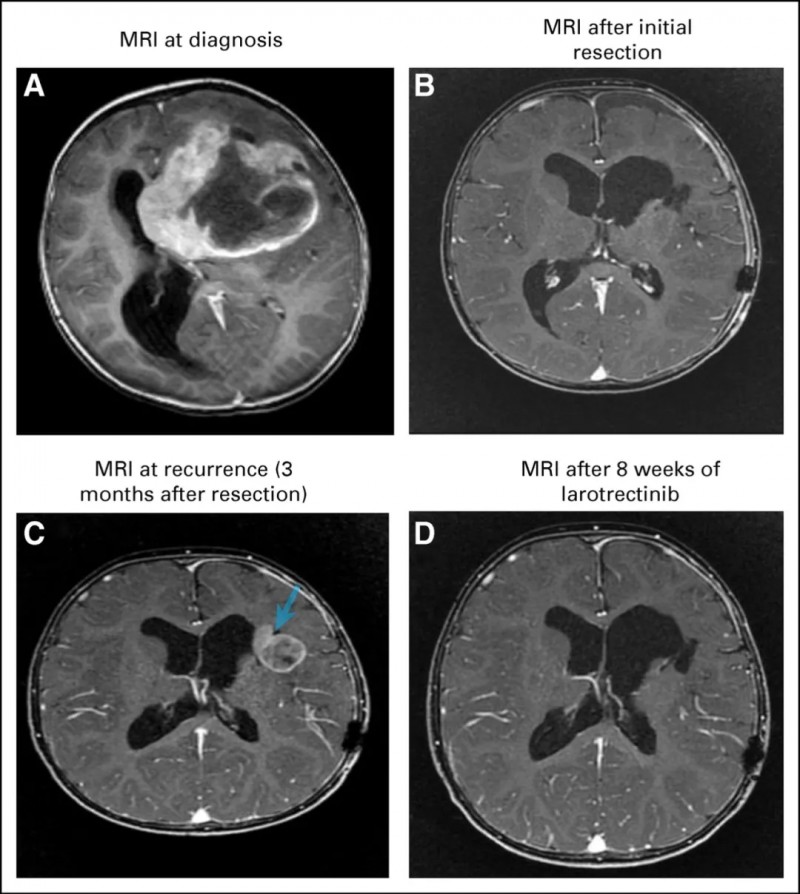
自此,又一个“钻石”靶点基因-NTRK迅速的火遍了癌友圈,开启了泛癌种治疗的新纪元!除了拉罗替尼,全球对于NTRK药物的研发正在如火如荼的进行中,今天全球肿瘤医生网医学部就为大家深度解析关于NTRK基因,以及其上市新药和最新进展。
初识"钻石"基因NTRK
NTRK之所以被称为“钻石”基因,首先是因为它非常罕见,在中国常见的肺癌,乳腺癌,结直肠癌中,只有1%~5%的患者存在这种突变,而一些罕见的癌症,比如婴儿纤维肉瘤和分泌型乳腺癌,存在NTRK融合的频率却高达90%~100%。其次,针对NTRK融合突变上市的药物及在研的药物临床效果显著,接受治疗的患者通常都能快速起效,很多晚期患者在使用NTRK抑制剂后得到了重生,像钻石一样罕见又珍贵。

NTRK在正常组织中的重要性
NTRK(NeuroTrophin Receptor Kinase)是神经营养因子受体络氨酸激酶。原肌球蛋白受体激酶(TRK)家族包括 TRKA、TRKB 和 TRKC 三种蛋白,它们分别由 NTRK1、NTRK2 和 NTRK3 基因编码,这些蛋白通常在神经组织中表达 。在健康组织中,NTRK通路参与神经系统的发育和功能以及细胞存活,在健康组织中起重要的作用。
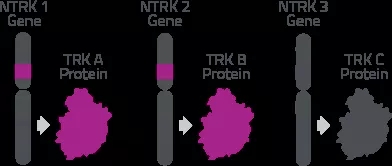
NTRK基因融合产生致癌蛋白
然而,当NTRK基因家族,包含NTRK1、NTRK2和NTRK3,任何一个基因如果和其他的基因发生了融合突变,那么就会导致异常活性,驱动肿瘤的发生。比如目前,婴儿纤维肉瘤,先天性中胚层肾病和分泌性乳腺癌都显示出ETV6-NTRK3融合,就是ETV6和NTRK3基因发生了融合,以及米歇尔的肿瘤中出现的TPM3-NTRK1,就是TPM3和NTRK1基因发生了融合。
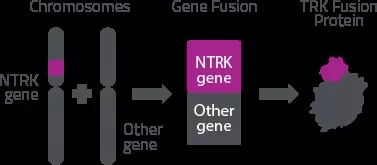
驱动癌症的致癌NTRK融合
至今,已经确定了25种不同的融合。致癌嵌合蛋白激活涉及癌细胞增殖,存活和血管生成的信号级联反应,导致肿瘤形成。

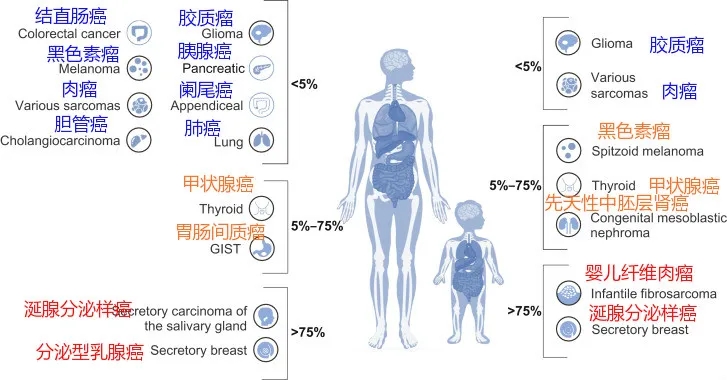
各类癌症出现NTRK融合的频率
目前已发现NTRK融合存在于超过25类癌症中,包括乳腺癌、结直肠癌、肺癌、甲状腺癌等,成人和儿童患者都可以使用。
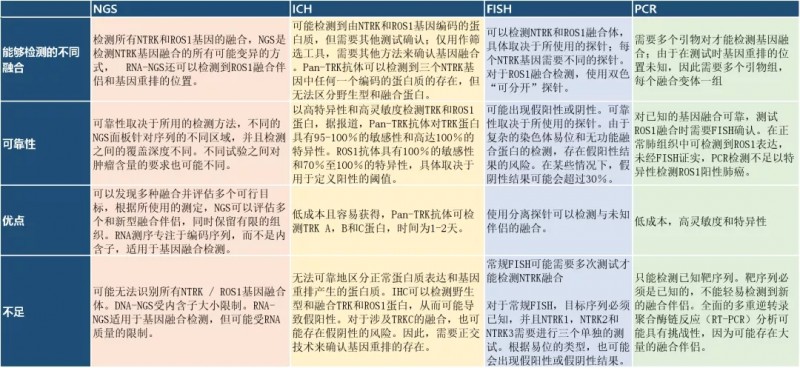
如何检测NTRK基因
目前,有多种方法可用于检测NTRK基因融合,包括FISH、IHC、NGS和PCR检测。我们将各类检测技术做了表格让大家能够直观的了解各类检测技术的利弊。
对于病友们来说,可能有些难以理解。我们来看下面的研究。
NCCN指南更新参考的《新英格兰医学杂志》对 NTRK 基因融合阳性患者(55例)的研究中(PMID:29466156),对NTRK基因融合的检测,使用的方法就是NGS(50例)和FISH(5例)。
所检测的实验室都是经过 CLIA 认证的。比如,其中有Foundation Medicine (Cambridge, MA, USA)、Memorial Sloan Kettering Cancer Center (New York, NY, USA) 和 University of Washington(Seattle, WA,USA)。
NTRK的融合虽与相关药物疗效有关,但是不容忽视的一点就是,此靶点的耐药机制已有研究,涉及到多个氨基酸位点的突变,这些突变的位点就只能用NGS方法来检测了。
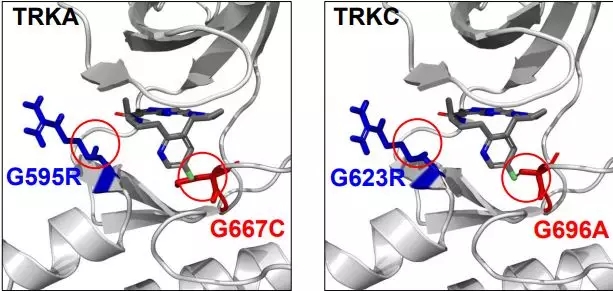
所以我们在检测NTRK融合的时候,还需要检测其耐药的位点,比如:TRKA出现G595R突变,TRKB出现 G639R 突变或者TRKC出现G623R突变等。针对其耐药位点的第二代TRK靶向药物LOXO-195已经出炉,专门来对抗耐药的新突变。因此,NGS二代测序最具优势。
FDA批准的NTRK靶向药有哪些
目前,全球上市的用于治疗NTRK融合基因实体瘤的药物有两个,分别是拜耳/LOXO的拉罗替尼(2018年11月被FDA批准上市)以及罗氏的恩曲替尼(2019年8月被FDA批准上市)。这两款药物成为癌症疗法从“基于癌症在体内的起源”转向“基于肿瘤的遗传特征”这一演变过程中的重要里程碑。
这两款不分癌症种类的广谱抗癌药开启了肿瘤治疗的新篇章,具有划时代的意义,那么这两款广谱抗癌药究竟有哪些不同,病友们究竟该如何选择呢?下面是这两款药物全面的用药信息对比,包括适应症,有效率,副作用,用法用量,价格全面对比,希望在抗癌的道路上能给大家提供更多的希望和帮助。
| 药品信息 | 拉罗替尼 | 恩曲替尼 |
| 通用名 | Vitrakvi | Rozlytrek |
| 英文名 | Larotrectinib | Entrectinib |
| 代号 | LOXO-101 | RXDX-101 |
| 生产厂家 | 拜耳 | 罗氏 |
| 作用靶点 | NTRK | NTRK/ROS1/ALK |
| 上市时间 | 2018年11月26日 | 2019年8月16日 |
| 适应症 | 治疗患有NTRK基因融合的局部晚期或转移性实体瘤的成人和儿童患者(12岁以上) |
1.治疗NTRK基因融合阳性的晚期复发实体瘤的成人和儿童患者; 2.ROS1阳性非小细胞肺癌患者 |
| 临床效果 |
NTRK融合阳性实体瘤成人患者:75% NTRK融合阳性实体瘤儿童患者:93% NTRK融合阳性非小细胞肺癌患者:4例接受拉罗替尼治疗的NTRK基因融合的非小细胞肺癌患者中3例都出现持续反应(从8.21到>20.27个月) |
NTRK融合阳性实体瘤成人患者:57.4% NTRK融合阳性实体瘤儿童患者:100% 局部晚期或转移性ROS1阳性非小细胞肺癌患者:总缓解率达到78%,完全缓解率达到5.9% |
| 剂型规格及价格 |
成人口服胶囊25mg和100mg,每月32800美元(30天100mg); 儿童患者为口服液体制剂,每月1.1万美元 |
口服胶囊100/200mg,每月17050美元 |
| 使用剂量成人 | 对成年人的剂量是每天口服100mg,每天两次,直至疾病进展或出现不可接受毒性 | 在成人中的推荐剂量是每天口服600毫克,与或不与食物同服,直到疾病进展或不可接受的毒性 |
| 使用剂量儿童 |
儿童按年龄和体重是用剂量:体表面积小于1.0米的儿科患者,推荐剂量是100mg/m2,每日口服两次,与或不与食物同服 |
12岁以上儿童: 体表面积大于1.50m2,推荐剂量600mg 体表面积大于1.11~1.50m2,推荐剂量500mg 体表面积大于0.91~1.10m2,推荐剂量400mg |
| 副作用 |
疲劳、恶心、头晕、呕吐、AST升高、咳嗽、ALT升高、便秘和腹泻 警告神经毒性,肝毒性和胚胎、胎儿毒性 |
疲劳、恶心、头晕、呕吐、咳嗽、便秘和腹泻、味觉障碍、水肿、感觉迟钝、呼吸困难、肌痛、认知障碍、体重增加、发热、关节痛和视力障碍。 警告肝毒性和胚胎-胎儿毒性-以及充血性心力衰竭、中枢神经系统效应、骨骼骨折、高尿酸血症、QT间期延长和势力障碍 |
拉罗替尼&恩曲替尼最新免费用药招募信息
拉罗替尼(Larotrectinib)和恩曲替尼已经正式在国内开展临床试验并引起了广泛的关注,这意味着,国内的患者也终于有机会免费用上这些美国上市的天价抗癌“特药”!
1.验证拉罗替尼对不同类型的肿瘤疗效。这些肿瘤必须存在一种特定的基因变化(NTRK1, NTRK2或NTRK3)。
适合患者:
通过分⼦学⽅法检测出NTRK1、NTRK2或NTRK3融合基因的局部晚期或转移性恶性肿瘤,必须接受过 适合其肿瘤类型和疾病分期的既往标准疗法失败后的患者。(即将招满,想申请的火速联系医学部)
2.Entrectinib治疗携带 NTRK1/2/3、ROS1或 ALK基因重排的局部晚期或转移性实体瘤患者的开放性、多中心、全球性 II期篮式研究,来确定携带NTRK1/2/3、ROS1或ALK基因重排的每类实体瘤患者人群(篮子)接受Entrectinib治疗后的客观缓解率(ORR)
适合患者:
经组织学或细胞学确诊为局部晚期或转移性实体瘤,携带NTRK1/2/3基因融合/重排,且不同时存在第⼆ 种致癌因素(例如EGFR、KRAS)
入组标准(部分):
1. 经组织学或细胞学确诊为局部晚期或转移性实体瘤,而且根据Foundation Medicine, Inc.或CLIA认证或同等机构认可的当地诊断实验室采用任何核酸类诊断检测方法进行的检测,该肿瘤携带一种预计分别转化成具有一个功能性TrkA/B/C、ROS1 或ALK激酶结构域的融合蛋白的NTRK1/2/3、ROS1或ALK基因重排,且不同时存在第二种致癌因素(例如EGFR、KRAS);
2. 对于通过当地实验室分子检测入组的患者,要求提交存档或新鲜的肿瘤组织(除非存在医学禁忌),在Foundation Medicine, Inc.或该地区其他认可的中心实验室进行独立中心分子检测;
3. 根据当地采用RECIST v1.1进行的评估,疾病可测量。
申请方式:做过基因检测的病友,请将基因检测报告,诊断报告电子版或拍照发送至doctor.huang@globecancer.com,邮件中留下联系方式,医学部将为您全面分析检测报告,匹配能够入组的临床试验,以及有无新药可以使用。
NTRK最新药物研究进展盘点
和所有的靶向药一样,总会出现的一个问题是耐药。TRK基因突变的癌症患者会对TRK抑制剂(如Loxo Oncology的larotrectinib药物)产生抗性,因此目前有多款药物被研发用于治疗这类TRK基因突变的癌症患者。
一,TPX-0005(Repotrectinib)
Repotrectinib(代号为TPX-0005,中文译音:瑞波替尼)是新一代的ROS1,pan-TRK和ALK多靶点抑制剂,能够克服几乎所有的ROS1,NTRK1-3和ALK抑制剂产生的耐药问题,因此,对于ROS1,NTRK1–3或ALK重排的患者已经接受过靶向治疗产生耐药后,Repotrectinib将是一种有效的治疗新选择。
Repotrectinib(瑞波替尼,代号TPX-0005)是美国TP Therapeutics公司研发的第二代ALK/ROS1/TRK抑制剂,也是新一代的广谱抗癌药,临床证实其效力比克唑替尼高90倍。
截至2020年7月10日第二阶段最新的中期数据,结果表明:
初治ROS1阳性非小细胞肺癌患者,客观缓解率达到86%;
经过TKI及化疗的非小细胞肺癌患者,客观缓解率达到40%;
经过TKI但未接受化疗的ROS1阳性非小细胞肺癌患者,客观缓解率达到67%;
NTRK阳性TKI经治的晚期实体肿瘤患者,客观缓解率达到50%。
这项数据非常振奋人心,也使Repotrectinib有潜力成为ROS1或NTRK阳性肿瘤患者的同类最佳治疗方案,包括TKI初治和TKI经治患者。
TPX-0005最新招募信息
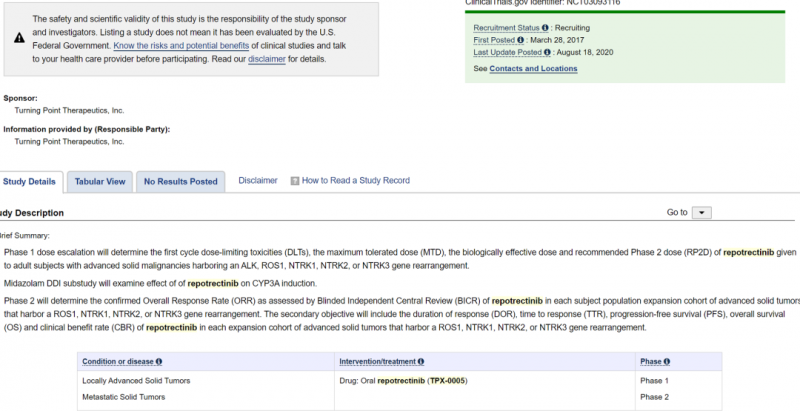
目前这款药物在全球范围内进行临床研究,美国,意大利,韩国,中国香港等地知名的癌症中心正在招募患者,想了解详情的患者可以咨询全球肿瘤医生网医学部。
二,LOXO-195
科学家经过研究,发现LOXO-101耐药机理和EGFR情况很像,主要是靶点本身(TRK基因)产生了新的突变,比如TRKA出现G595R突变,或者TRKC出现G623R突变。
根据这个发现,第二代TRK靶向药物LOXO-195已经出炉,专门来对抗耐药新突变。
结果十分乐观!
在美国亚特兰大AACR会议上公布的最新研究显示:在使用一代TRK抑制剂治疗耐药后,LOXO-195最终可能是一种有意义的治疗方法。”
这是一项一期试验,所以入组的患者不多,一共有31名之前曾接受过至少一种第一代TRK靶向治疗的患者入组,包括7名儿童和24名成人。包括15种类型的肿瘤,最常见的是肉瘤(16%),胃肠道间质瘤(13%),胰腺癌(12%)和乳腺癌(各20%)。其中21例接受过拉罗替尼larotrectinib,9例接受过恩曲替尼entrectinib,1例接受过PLX7486。平均接受治疗的时间为11个月。
截至2018年12月3日,29名患者的治疗效果可以评估,10名患者(34%)出现完全缓解或部分响应。 另外9名患者病情稳定。
“LOXO-195在剂量小于或等于100 mg BID时耐受良好; 最佳剂量和时间表仍在探索中。
三,ICP-723
ICP-723是一种国内研发的第二代泛酪氨酸受体激酶(泛TRK)小分子抑制剂,用于治疗不同肿瘤类型的神经营养性酪氨酸激酶(NTRK)阳性的肿瘤患者以及由于抗性TRK基因突变而对第一代酪氨酸激酶(TRK)抑制剂产生耐药性的患者。2019年3月17日,ICP-723片申报临床试验申请,即将开始临床试验并招募患者。
四,AB-106
AB-106是一款口服、高选择性的ROS1/NTRK双靶点小分子抑制剂。这款抗癌新药是2018年底从日本第一三共株式会社独家引进,早期临床试验结果显示,AB-106具有以下特点:
1.对ROS1及NTRK1-3具有高效抑制作用,对克唑替尼的主要耐药位点ROS1 G2032R同样具有高效抑制作用。
2.安全性好,应答率高,有效持续时间长,带给病人更长的无疾病进展生存期。
3.对克唑替尼治疗失败的ROS1阳性非小细胞肺癌患者及脑转移患者也有疗效。
4.跨癌种,有ROS1或NTRK融合突变就可适用。
根据中国国家药监局药品审评中心公示,目前小分子酪氨酸激酶抑制剂在研药物AB-106胶囊已于近日获得2项临床试验默示许可。一项拟开展的适应症为携带NTRK1、NTRK2、NTRK3融合基因的不分瘤种的实体瘤;另一项拟开展适应症为携带ROS1融合基因的非小细胞肺癌(NSCLC)。
五,TL118
TL118胶囊是一款国产“不限癌种”NTRK融合基因突变靶向药,目前国内已开展TL118治疗晚期NTRK融合实体肿瘤的临床试验。
TL118最新招募信息
适合患者:
经病理组织学和/或细胞学确诊的局部晚期或转移性恶性实体瘤,既往检测存在NTRK基因融合突变, ECOG体⼒评分0-2分,⾄少有⼀个可评估的肿瘤病灶。
试验题目:TL118胶囊在NTRK基因融合的晚期恶性实体瘤患者中的安全性、耐受性、药代动力学特征的剂量递增、开放的I期临床试验
NTRK基因开启泛癌种治疗的宝藏之"钥"
总结一下,目前多款针对NTRK的药物临床证实效果显著,并且都是广谱抗癌药物,对很多不同肿瘤都有效,因此需要提醒大家的是,即使是标准治疗方案失败,也可以尝试进行基因检测,一旦存在ALK,ROS1,NTRK1、NTRK2或者NTRK3基因融合,就可以尝试这些特效的广谱抗癌药。做过基因检测的病友,可以将报告发送至全球肿瘤医生网医学部申请,我们的专家将为您全面分析检测报告,匹配能够入组的临床试验,以及有无新药可以使用。
1.请将基因检测报告,诊断报告电子版或拍照发送至doctor.huang@globecancer.com,邮件中留下联系方式,医学部收到报告分析完毕后一个工作日内电话联系。
目前已经上市的多款广谱抗癌药:拉罗替尼,恩曲替尼,LOXO-292等仍在国内的招募仍在进行,由国内肿瘤领域权威的几家医院率先开展。以前这些美国研发上市的抗癌新药对于国内的患者来说遥不可及,近两年随着国家的重视,加快了各类抗癌药物研发上市的审批速度,让更多国外的新药好药,也能造福国内的癌症患者。希望这款药物能尽快在国内完成临床试验,顺利上市,造福患者。


































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城