肺癌脑转移治疗,肺癌脑转移怎么办,肺癌脑转移不等于死亡通知书,选对方案或许连放疗都不用做
越来越多的研究已经证实,不同类型基因突变驱动的同类癌症,仍然存在许多的不同之处。比方说,因EGFR突变导致的非小细胞肺癌,发生脑转移的风险高达44%~63%,远远超过非EGFR突变患者的10%。
而脑转移正是有统计学分析指出,发生了脑转移的EGFR突变非小细胞肺癌患者,接受同样的一线治疗的无进展生存期是明显比不存在脑转移的患者更短的(8.67个月 vs 10.9个月),总生存期的差异更大(11.6个月 vs 18.7个月)[1]。
基于这样的疾病特点,入脑活性、也就是治疗脑内病灶的能力,成为了EGFR抑制剂疗效的重要组成部分。哪些方案能够取得更好的疗效呢?让我们通过几项重要临床试验及典型患者病例,简单分析一下几类常用EGFR抑制剂治疗脑转移的效果。
第一、二代EGFR抑制剂:颅内病灶缓解率60%~70%
根据一项来自韩国研究者2020年发布的大样本量统计分析结果[2],多类第一代及第二代EGFR抑制剂,一线治疗发生了脑转移的EGFR突变非小细胞肺癌患者,颅内病灶的缓解率均在60%~70%左右。
吉非替尼、厄洛替尼、阿法替尼治疗的颅内缓解率分别为64.7%、68.2%和72.9%,中位颅内无进展生存期分别为17.3个月、12.4个月、23.3个月。其中,第二代EGFR抑制剂阿法替尼的疗效要更好一些。
另一项早期的日本研究[3]的结果也比较类似,患者的缓解率为42.9%。这两项临床试验都来自亚洲机构,主要以亚洲人种的患者为主,得到的疗效可能也更贴近国内患者的实际。
来自欧美的研究[4]得到的疗效有一些差距,但整体数据也非常不错,使用厄洛替尼治疗发生了脑转移的EGFR敏感性突变患者,缓解率为26.4%,颅内无进展生存期11.7个月。
当然,除了缓解率比较高以外,第一二代EGFR抑制剂治疗得到的临床完全缓解率数据也很不错。就比如我们接下来看到的这个病例。
案例一
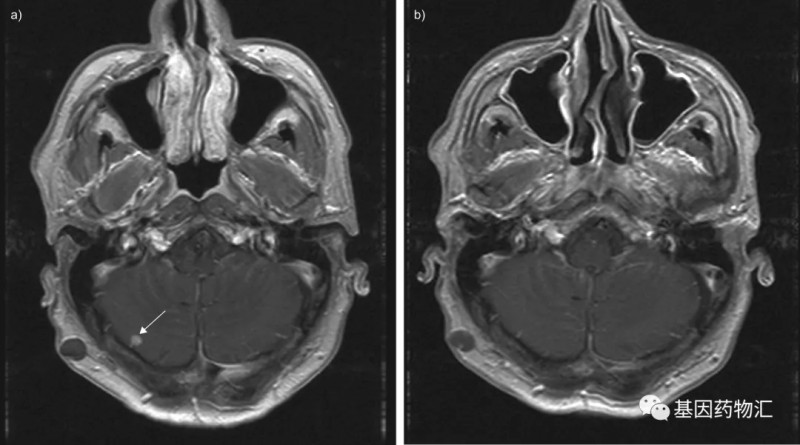
这位患者是一名罹患了肺腺癌的男性,EGFR外显子19缺失(EGFR ex19del)突变,属于对EGFR抑制剂比较敏感的亚型。图左是他接受厄洛替尼治疗前的影像,白色箭头标记了位于小脑右半球的一个非常明显的颅内转移病灶。而图右是他接受了厄洛替尼4个月治疗之后的图像,同位置,颅内转移病灶已经完全消失!
当然,能够通过第一二代EGFR抑制剂治疗让病灶完全消失、并且维持很长的时间自然是非常理想的,但是也有很多患者,在治疗的过程中发生了耐药突变,不再对第一二代EGFR抑制剂响应。对于这些耐药患者来说,还有什么可以选择的方案呢?
第三代EGFR抑制剂:一线耐药患者缓解率,超过60%
第一二代EGFR抑制剂耐药,最常见的突变亚型就是EGFR T790M。第三代EGFR抑制剂在继承第一二代药物出色的一线疗效的基础上,增加了对于这类突变型癌症的治疗作用。
基因药物汇为大家整理了目前已经在国内获批的三款第三代EGFR抑制剂,以及众多在研(国产)第三代EGFR抑制剂中比较有代表性的D-0316,制成了清晰的数据对比表格。

从中我们可以看出,几款第三代EGFR抑制剂治疗颅内病灶的入脑性都非常出色,颅内病灶缓解率都在60%左右或更高,疾病控制率更是接近100%。这意味着,不仅一线治疗的患者能够从第三代EGFR抑制剂的治疗中获益,即使是发生了T790M突变、对于第一二代EGFR抑制剂耐药的患者,也同样有非常高的概率能够通过治疗缓解,甚至是完全消除脑内的肿瘤病灶!
案例二[4]
这名患者是一位74岁的老太太,毕生从未吸烟,在一次检查中发现血液癌胚抗原水平升高,因此接受了胸部CT检测,并最终确诊为T4N1M1c,即ⅣB期肺腺癌。
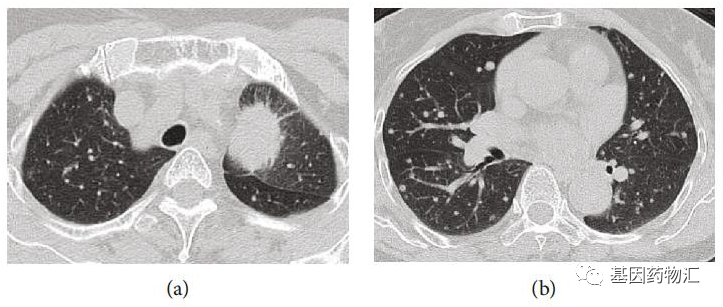
患者的胸部CT扫描图像,肺部巨大的阴影以及周围的小结节十分明显。
除了肺部的病灶,患者颅内的转移病灶也数量惊人,根据增强MRI的检查结果,病灶总共超过20个!属于非常典型的多发脑转移。
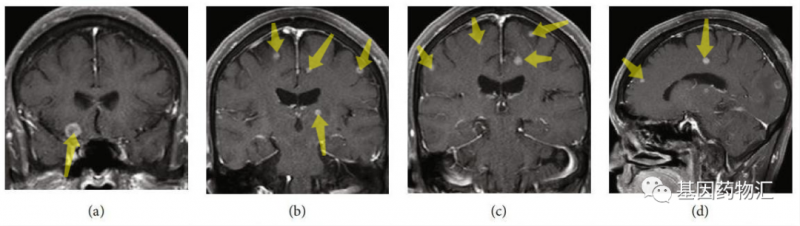
高龄、晚期、多发转移,这样的患者还有希望通过药物治疗达到缓解吗?事实上,在接受了仅仅5周的奥希替尼治疗之后,患者颅内的病灶,竟然完全消失了!
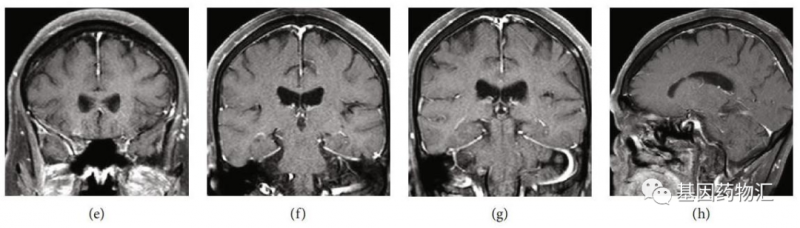
研究者据此指出,对于部分患者,尤其是将奥希替尼作为一线治疗方案的患者,脑部放疗完全可以推迟,甚至部分响应良好的患者根本不需要脑部放疗。
这说明,在某些特殊的情况下(比如患者可能很难耐受放疗,或颅内转移病灶数量过多等),可以考虑先使用奥希替尼治疗。如果患者对于药物的响应良好,很可能奥希替尼的治疗能够为脑部放疗提供条件,或者直接凭借药物治疗完全消除病灶。
当然,奥希替尼的应用也有一定的适应症限制,许多突变亚型的患者存在一些耐药突变型,对于第三代EGFR抑制剂的治疗不敏感,那么这些患者可以选择哪些治疗方案呢?
"后奥希替尼时代",新药引领个性化治疗格局
越是多线耐药的患者,可能存在的基因突变型就越是多样,治疗也更加复杂甚至困难。对第三代EGFR抑制剂耐药的患者,最常见的突变类型包括MET(约占25%)、EGFR Del19/T790M/C797S及L858R/T790M/C797S三突变(约占20%~40%左右)和HER2/3等。
目前,MET突变和C797S突变是“后奥希替尼”新药研发的最主要方向。
01、EGFR C797S抑制剂:第四代EGFR抑制剂,"国研"走上世界前列
目前,首款走入临床试验阶段的第四代EGFR抑制剂是由我国药企研发的新药TQB3804。这款药物不以EGFR Del19等突变类型为主要靶标,而是专门针对第三代EGFR抑制剂耐药后常见的C797S突变,因此对于第三代药物耐药后患者的治疗效果更加出色。
目前,TQB3804在临床前试验中已经展现出了良好的效果,进一步的人体试验项目正在进行,我们会密切关注试验结果。
除此以外,由外国药企研发的BLU-945在临床前研究中也展现出了出色的潜力,目前正在进行进一步的临床试验。
02、MET抑制剂:多款新药问世,耐药、脑转移患者均可获益
MET突变可能作为一种导致原发肿瘤的原因存在,同时也是导致EGFR抑制剂耐药的“元凶”之一。
目前已经获批上市的MET抑制剂有两款,分别是在日本获批上市的特普替尼和经FDA批准在美国上市的卡马替尼。这两款药物在耐药患者的治疗中均展现出了比较理想的效果。
其中瑞普替尼治疗的整体缓解率达到42.4%,卡马替尼治疗的整体缓解率达到了67.9%,两款药物的疾病控制率均超过了90%,且缓解持续时间分别达到了12.39个月和9.72~11.14个月。
而特普替尼在发生了脑转移的患者的治疗中也展现出了良好的潜力,患者的全身客观缓解率为52.4%,疾病控制率76.2%;中位缓解持续时间9.5个月,中位无进展生存期9.5个月。
目前,MET抑制剂的研发项目非常丰富,针对各类MET突变亚型均有临床试验正在招募。各类MET异常的非小细胞肺癌患者,以及接受过一线EGFR抑制剂治疗、后续发生了MET扩增而耐药的患者,都可以联系全球肿瘤医生网医学部详细咨询,匹配适合的临床试验项目。
03、EGFR-MET双抗:"双管齐下"、突破耐药困境
既然MET突变是EGFR耐药最重要的原因之一,那么使用双靶点抑制剂、即“双抗”药物,是否能够将治疗的效果再次提升一个台阶?
这样的治疗思路也受到了重视。使用EGFR-MET双靶点抑制剂JNJ6372治疗第三代EGFR抑制剂耐药患者的Ⅰ期临床试验初步结果,曾经在ASCO大会上公开,引起了广泛的重视。
该结果显示,在47例曾经接受第三代EGFR抑制剂治疗的患者中,整体缓解率达到了21%;在C797S、c-MET扩增及其它突变类型的患者中均观察到了缓解。
04、HER3抑制剂:ADC"家族"又出"救命药",疾病控制率超高
HER2/3突变同样是奥希替尼耐药最主要的原因之一。来自日本的U3-1402是一款HER3抗体偶联药物,在往届ESMO大会上,研究者曾经公开了这款药物用于EGFR抑制剂耐药患者的疗效数据,疾病控制率达到了惊人的70%!
研究中,86%的患者曾经接受过奥希替尼治疗,90%的患者使用过化疗;患者的中位治疗线数为4线,其中包括2线EGFR抑制剂治疗。
当然,U3-1402最具突破性的意义在于,根据ASCO大会和WCLC大会上公开的结果,不论是何种类型的耐药突变,都可以从这款药物的治疗中获益。这意味着,一旦这款药物成功获批上市,EGFR抑制剂耐药的患者,等来的很可能是一款具有“通用价值”的重磅新药。
05、"奥希替尼+":个性化方案开启治疗新格局
新药虽好,但研发周期普遍比较长,从公开初步数据到正式获批很可能长达数年之久,难解患者“燃眉之急”。因此,研究者们提出了另一种思路:从“冷板凳”上发掘一些有潜力的“选手”、将现有药物组合应用,是否能够组成一支“奇兵”,克制耐药突变?
在这样的思路之下,“奥希替尼+”的联合用药方案成为了客服耐药的新突破口。
以癌细胞表面的EGFR受体为作用位点、大分子的EGFR抑制剂耐昔妥珠单抗疗效虽不温不火,但即使是对第三代EGFR抑制剂耐药的患者,尤其是其中T790M/C797S双突变的患者,仍然可以取得一定的缓解率。
耐昔妥珠单抗+奥希替尼的联合用药组合,用于第一二代EGFR抑制剂耐药的患者,整体缓解率29%;用于第三代EGFR抑制剂耐药的患者,整体缓解率13%;其中,T790M/C797S双突变的患者,整体缓解率竟达到了50%!
对于T790M/C797S反式突变的患者,第一代+第三代EGFR抑制剂的联合方案疗效非常出色。在曾公开于ASCO大会上的一项小规模临床试验中,使用第一代EGFR抑制剂吉非替尼+第三代EGFR抑制剂奥希替尼联合治疗,患者的中位无进展生存期约为22.5个月,整体缓解率高达88.9%。
当然,类似的方案还有很多,在此我们不再一一赘述,希望根据自身疾病特点进行咨询的患者,可以联系全球肿瘤医生网医学部。
肺癌脑转移不等于死亡,是时候打破魔咒了
从上述不论是病例也好、或者临床试验结果也罢,我们可以清晰地认识到,只要能够为患者选对方案,那么即使是发生了脑转移的非小细胞肺癌患者,也同样有完全摆脱癌症的可能。
当然,这一期的前提仍然是,“选对方案”。想要从浩如烟海的治疗方案中挑选出一种最合适的,首先应该明确定义患者的疾病是怎样的。
随着癌症精准治疗的发展,基因检测已经成为了每一名癌症患者确诊后必须进行的检测项目。不论是初治的患者,还是经过一系列治疗后发生了耐药的患者,都应当在基因检测的指导下选择最有可能获益的方案,才能真正有效地延长生存期。
关于基因检测、新药及临床试验项目,大家同样也可以联系全球肿瘤医生网医学部获取帮助。
参考文献/文中部分案例及图片来源
[1] The importance of Brain metastasis in EGFR Mutation Positive NSCLC Patients
[2] The different central nervous system efficacy among gefitinib, erlotinib and afatinib in patients with epidermal growth factor receptor mutation-positive non-small cell lung cancer
[3] Effect of gefitinib ('Iressa', ZD1839) on brain metastases in patients with advanced non-small-cell lung cancer
[4] Complete Remission of Multiple Brain metastases in a Patient with EGFR-Mutated Non-Small-Cell Lung Cancer Treated with First-Line Osimertinib without Radiotherapy

































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城