速递|阿替利珠单抗(Tecentriq)获批非小细胞肺癌辅助治疗的适应症
2021年10月16日,FDA批准了阿替利珠单抗(Atezolizumab,Tecentriq)的新适应症,用于辅助治疗切除术及铂类辅助化疗后的Ⅱ至ⅢA期非小细胞肺癌患者,患者应在经过FDA批准的检测后,确定表达PD-L1的肿瘤细胞比例≥1%。
FDA同时批准了伴随诊断项目,由 Ventana Medical Systems Inc.开发的VENTANA PD-L1(SP263)检测。
该批准基于Ⅲ期IMpower010试验(NCT02486718)的结果。此前8月3日,基于统一试验的结果,FDA授予该适应症优先审查资格。仅两个半月的时间,该审查就得到了正式的批准。
显著延长生存期,超过60%的患者无病生存3年
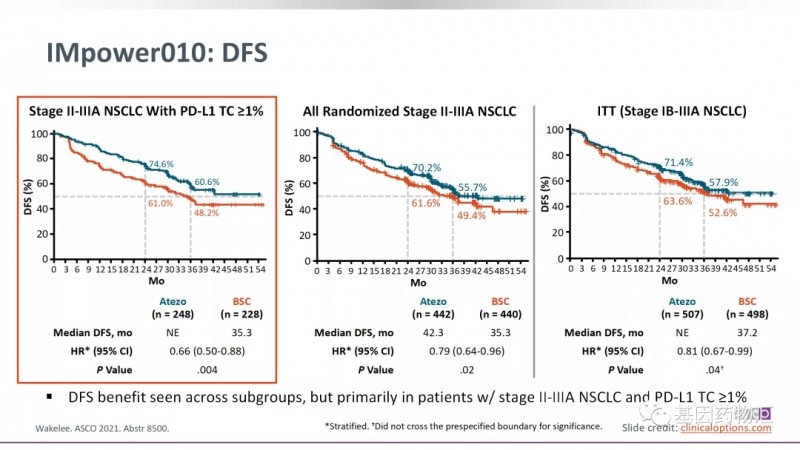
根据IMpower010试验的结果,将阿替利珠单抗作为术后辅助治疗方案,与最佳支持治疗方案相比,能够将患者疾病复发或死亡的风险降低34%。
目前试验尚未完全结束,但阿替利珠单抗的疗效已经展现出了显著的优势。在所有PD-L1表达水平的患者群体当中,阿替利珠单抗治疗的中位无病生存期为42.3个月,最佳支持治疗仅为35.3个月。PD-L1表达比例≥1%的患者中,这一优势更加明显。
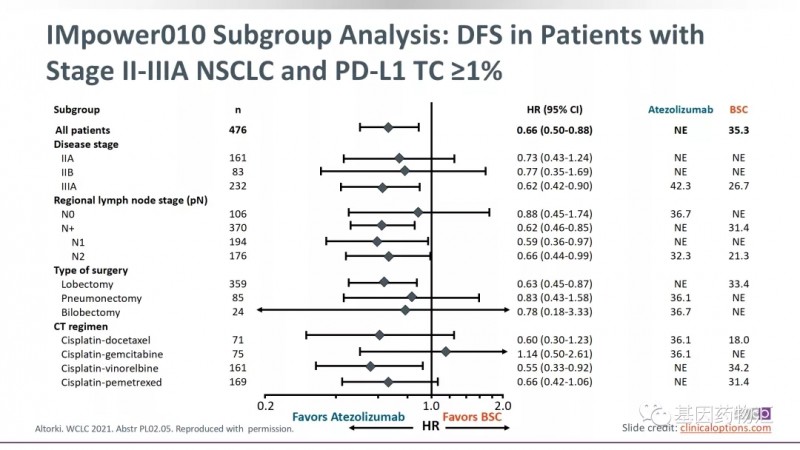
而亚组分析结果同样也显示,不论患者的分期(ⅡA、ⅡB或ⅢA)、淋巴结转移情况以及病例分型等等,阿替利珠单抗都展现出了疗效方面的显著优势。仅有少部分类型的患者,例如辅助治疗时使用了顺铂+吉西他滨方案的患者,选择最佳支持治疗时无病生存期比阿替利珠单抗更长。
辅助免疫治疗,正在开创非小细胞肺癌治疗的新时代
对于非小细胞肺癌来说,Ⅰ~Ⅲ期的患者都应当争取接受手术,但手术后如何“巩固疗效”、避免残留癌细胞而导致晚期复发和转移,是真正改善中早期患者生存期的关键。
罗氏的首席医疗管兼全球产品开发负责人,Levi Garraway医学博士在新闻稿中指出:“阿替利珠单抗是第一个、也是目前唯一一个可以用于非小细胞肺癌辅助治疗的癌症免疫疗法。这一方案开启了一个全新的时代,让早期肺癌患者也有接受免疫治疗的机会,并增加治愈的比例。”
他表示,十多年来,早期非小细胞肺癌治疗的发展一直处于一种停滞的状态,这一次的批准堪称“里程碑”,为医生与患者提供了一种能够显著降低癌症复发风险的新方案。
免疫治疗的加入,正有力地将术后辅助治疗的效果提升到一个新的高度。我们相信,未来会有更多的患者,在手术以及术后辅助方案的帮助之下,无癌生存3年、5年、10年,甚至彻底地摆脱癌症,完全回归正常生活。

































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城