乳腺癌HER2靶向药,广谱抗体偶联(ADC)新药DS8201(Enhertu、Trastuzumab Deruxtecan)乳腺癌适应症获FDA优先评审资格
1月17日,阿斯利康和第一三共宣布已收到美国FDA接受其抗体偶联药物(ADC)Enhertu(trastuzumab deruxtecan)补充生物制品许可申请(sBLA)的通知,用于既往接受过抗HER2治疗方案的不可切除或转移性HER2阳性乳腺癌成人患者的治疗。该sBLA申请也获得了优先审评资格,处方药报者付费法案(PDUFA)日期为2022年的第二季度。
其实早在2021年10月4日,FDA就授予了DS-8201(Enhertu)突破性疗法认定,用于治疗既往接受过1种或多种基于抗HER2方案的不可切除或转移性 HER2 阳性乳腺癌成年患者。这是DS-8201获得的第四个突破性疗法认定。

事实上,说起重磅抗体药物偶联物(ADC)——Enhertu(DS8201)的综合临床研究成果,可谓是“实力抢镜”,虽然以后线治疗起家,但临床数据遍布乳腺癌、胃癌、肺癌、结直肠癌,给多癌种HER2突变患者带来了新的治疗希望,展现出非凡的潜力!
在2021年9月16~21日召开的欧洲肿瘤内科学会(ESMO)年会上,DS-8201多项研究结果再次刷新,横扫肺乳胃肠四大癌种,风采不减。今天无癌家园小编就给大家梳理下这款广谱ADC新药DS-8201的最新研究进展。
乳腺癌DS8201治疗效果
01、复发风险降低72%,DS-8201挑战乳腺癌二线标准治疗
此次认定的DESTINY-Breast03的3期试验研究结果,这是首个头对头对比ADC药物(DS8201和T-DM1)治疗HER2阳性晚期乳腺癌疗效与安全性的一项多中心、开放性、随机、Ⅲ期临床研究。
纳入了先前在晚期或转移性环境中接受过曲妥珠单抗(赫赛汀)和紫杉类治疗的不可切除或转移性 HER2 阳性乳腺癌患者。值得注意的是,这些患者被允许具有临床稳定的、经治疗的脑转移。
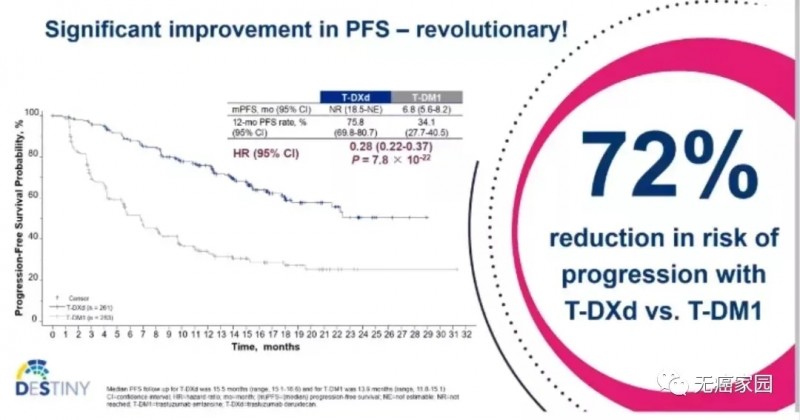
在 2021 年 ESMO 大会期间提交的试验数据显示,研究者评估的DS8201的PFS为25.1个月(95%CI,22.1-NE),而T-DM1为7.2个月(95% CI,6.8-8.3)(HR,0.27);研究组或对照组均未达到中位生存期。
上述数据表明,与TDM1相比,DS-8201能够降低HER2阳性转移性乳腺癌患者的疾病进展或死亡风险高达72% !
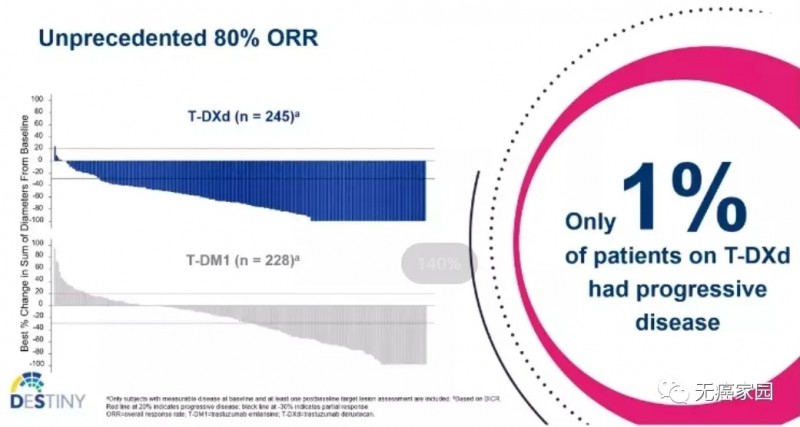
此外,DS-8201确认的客观缓解率为79.7%,而TDM1为34.2%。这表明DS-8201的疗效是TDM1的2.33倍之多!
对DS-8201有反应的反应中,完全缓解达16.1%,部分缓解为63.3%,疾病稳定16.9%,仅有1.1%的患者出现疾病进展!
02、疾病控制率100%!FDA授予HER2+乳腺癌新药ARX788快速通道
对于HER2阳性乳腺癌,其实肿瘤患者们有更多选择。
就在2021年1月,FDA授予全新抗体偶联药物ARX788快速通道指定,旨在加速这一先进抗癌疗法的上市进程,为一线治疗后进展的晚期HER2阳性乳腺癌患者带来更好的治疗选择。这也是ARX788的一个重要里程碑,期待 ARX788 尽快获得FDA批准早日上市。
这项临床试验结果在2020年12月的圣安东尼奥乳腺癌研讨会上公布,值得一提的是,这项在中国 HER2 阳性乳腺癌1期试验中,客观缓解率高达 74%,其中19 名患者中有14名有响应,疾病控制率高达100%。
在美国和澳大利亚进行的1期HER2阳性泛肿瘤试验中,客观缓解率为67%,3 名患者中有2名有反应,疾病控制率为100%。
目前,全球已启动多项ARX788的临床研究,其中一项针对既往接受过赫赛汀等一线治疗方案失败的HER2阳性乳腺癌患者的临床研究正在招募患者,有意向参加的癌友可联系无癌家园医学部进行初步评估。
胃癌DS8201治疗效果
01、疾病控制率达81%!DS-8201成为晚期胃癌治疗药物的一匹黑马
经研究显示,胃癌患者中约1/5呈HER2阳性。因此在DESTINY-Gastric01的II期临床试验中,评估了DS-8201在HER2阳性晚期胃或胃食管交界处(GEJ)腺癌患者中的有效性。
在2021年ESMO大会上,也进一步更新了DESTINY-Gastric02的结果。试验纳入了79名患者,每名患者以6.4mg/kg Q3W标准用药,这些患者先前接受过2种或多种方案(包括5-FU、含铂化疗、曲妥珠单抗)。
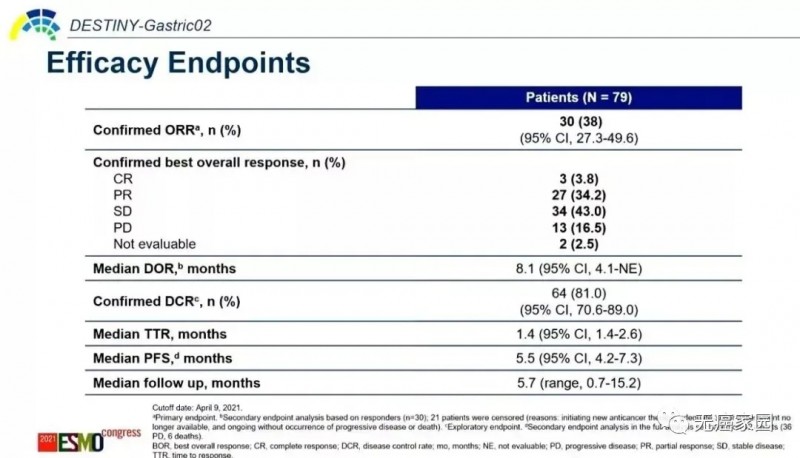
截至2021年4月9日,研究达到了主要终点和关键次要终点:
在79例可评估患者中,通过独立中央审查(ICR)评估DS8201治疗HER2+胃癌或GEJ患者的客观缓解率为38%,疾病控制率可达81%。
中位无进展生存期为5.5个月,中位缓解持续时间为8.1个月。
肺癌DS8201治疗效果
01、客观缓解率92.3%,DS-8201引领肺癌靶向治疗掀起创新革命
去年ASCO大会上发布的DESTINY-Lung01研究是针对既往往接受过一种或多种系统治疗,出现疾病进展的HER2突变型(HER2m)不可切除和/或转移性非鳞非小细胞肺癌(NSCLC)患者展开的,其中大多数患者曾接受过含铂化疗(90.5%)和抗PD-1或PD-L1治疗(54.8%)等治疗。
研究结果表明,接受DS-8201单药治疗(6.4mg / kg)的,61.9%的患者获得肿瘤缓解,疾病控制率(90.5%)和中位无进展生存期(14.0个月)得到显著改善。
在今年ESMO大会上进一步更新了数据,HER2突变型患者中,有1例患者达到完全缓解,49例达到部分缓解,疾病稳定者34例,疾病进展3例,4例无法评估,确认的客观缓解率达54.9%,疾病控制率高达92.3%!
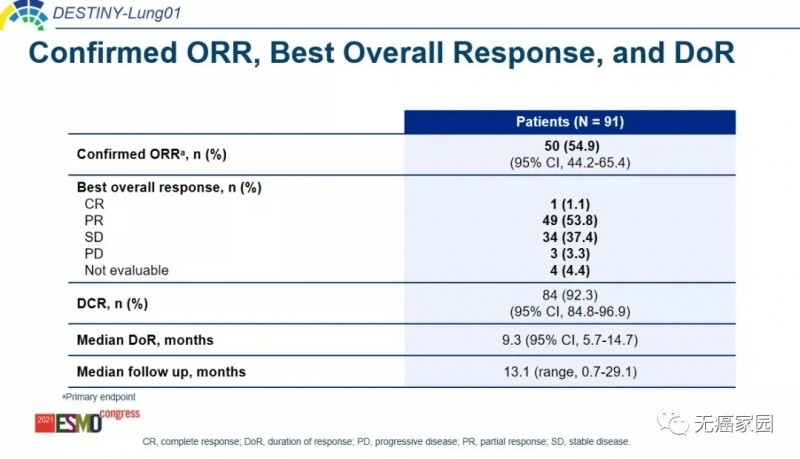
患者中位无进展生存期为8.2个月,中位总生存期为17.8个月。
研究还显示,无论HER2基因突变类型,患者都可能从DS-8201的治疗里获益。
结直肠癌DS8201治疗效果
01、疾病控制率达83%,DS8201击破HER2阳性结直肠癌的枷锁
在2020年ASCO会议上公布的DESTINY-CRC01是一项针对既定既往接受过两线及以上标准治疗的HER2阳性,不可切除和/或转移性结直肠癌患者开展的II期临床试验的方法。
此试验结果表明,经DS-8201单药治疗后,患者的肿瘤客观缓解率为45.3%,其中完全缓解率为1.9%,部分缓解率为43.4%,疾病控制率(DCR)达83.0%,患者的中位无进展生存期(PFS)为6.9个月。
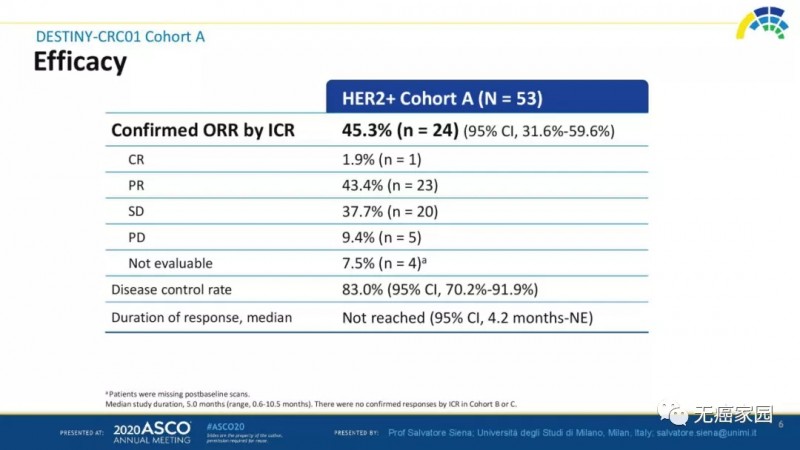
目前尚无获批用于HER2阳性结直肠癌患者的确切治疗药物,而DS-8201在肿瘤缓解率和疾病控制率方面的独特优势将突破HER2阳性结直肠癌治疗的桎梏,为广大患者带来新希望。
"靶向+化疗"强强联手,缔造抗癌新药DS-8201
DS8201,一种HER2抗体+伊立替康类化疗药物的偶联药物,属于ADC型药物类型(抗体偶联药物)。它有两部分组成:第一部分是针对HER2靶点的抗体,可以精准的识别并且结合HER2高表达甚至低表达的肿瘤细胞;第二部分是剧毒的化疗药伊立替康。这种设计会使抗体带着化疗药去找肿瘤细胞,然后精准地给肿瘤细胞下毒,毒死它们。
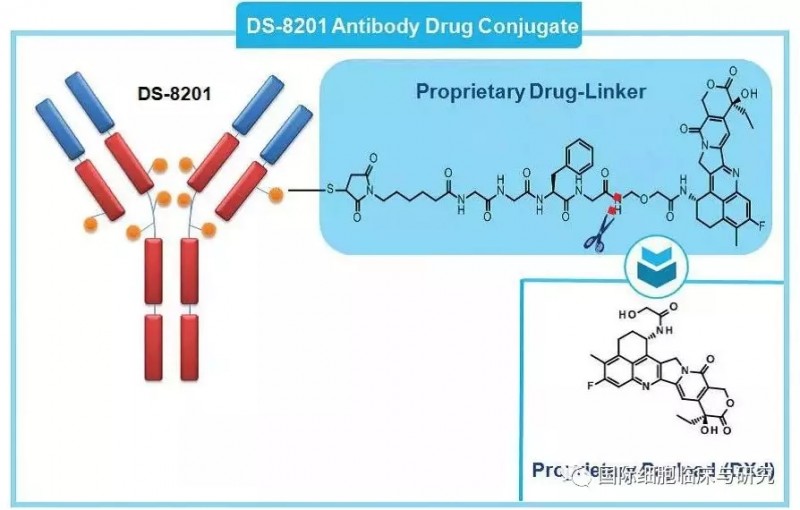
图为DS-8201的设计结构,图中橙色小圆球为化疗药(来源dsi.com)
这种药物设计结合了靶向药的精准和化疗药的高效,既避免了全身使用化疗药的毒副作用,也比单独使用靶向药具有更强的杀伤能力,一举两得。
如何检测HER2是精准治疗癌症的前提
最后,小编在这里需要提醒大家的是,如何检测HER2是关键!
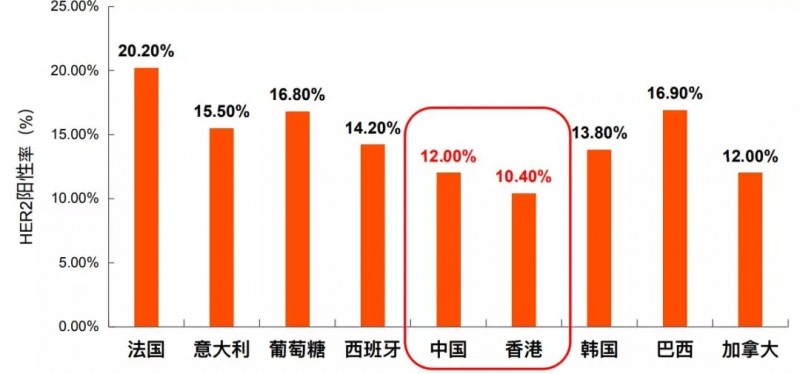
长期以来,IHC和FISH是检测HER2的金标准,临床上一项大型、非干预性、国际性流行病学研究(HER-EAGLE),共纳入4949例胃腺癌或胃食管结合部癌患者,旨在评估不同国家真实世界中的HER2阳性率 :结果显示,我国胃癌患者的HER2阳性率低于国外水平。传统的FISH/IHC遗漏将近50%的HER2/ERBB2 改变!
因此,各位癌友们一定要慎重选择检测机构,如做过检测的病友可以联系无癌家园进行解读,评估可用的治疗方案。
参考文献
https://www.businesswire.com/news/home/20220114005456/en







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城