CAR-T之父公布首个CAR-T细胞治疗实体瘤的临床试验结果,CAR-T细胞免疫疗法有望挺近癌症一线治疗
CAR-T细胞免疫疗法发展现状
随着2021年阿基仑赛注射液、瑞基奥仑赛注射液先后在中国获批上市,2022年西达基奥仑赛被美国FDA获批上市,癌症治疗领域火速掀起一阵“CAR-T热”,如果说中国在2021年正式迎来细胞免疫治疗元年,那么,可以毫不犹豫地说2022年将会迎来井喷期!
这一蜕变或许有望将“抗癌”变为“治癌”,迎来反击癌症的新时代。比起“治标不治本”经常会复发的传统疗法,调用患者体内自身免疫系统的CAR-T可以说是目前最先进的治疗手段。
的确,CAR-T技术在多种血液肿瘤,如白血病、淋巴瘤、多发性骨髓瘤中,表现出不俗的疗效,让许多濒临绝境、无药可治的血癌患者,一大半都获得了良好的疗效。
在血液性肿瘤的治疗中,CAR-T的有效率甚至超过80%,一度成为最耀眼的明星疗法,这也让CAR-T的发明者Carl June教授被冠以“CAR-T之父”之名。

“CAR-T之父”Carl June博士(图源美国癌症研究所)
然而,CAR-T治疗在实体瘤上的临床疗效差强人意。究其原因,主要在于实体瘤的细胞疗法存在不少难点,如不同类型实体瘤的异质性大、缺乏独特的肿瘤相关抗原作为CAR-T靶点、T细胞无法有效归巢到肿瘤部位、CAR-T细胞持续性不够以及肿瘤内复杂的微环境对免疫有抑制作用。
但是,CAR-T疗法在实体肿瘤方面如前列腺癌、肝癌、胃癌、胰腺癌等癌症中取得了一定的疗效,国内外学者也针对CAR-T进行了多种改造,不断地发现并开发新靶点,用于治疗多种实体肿瘤。
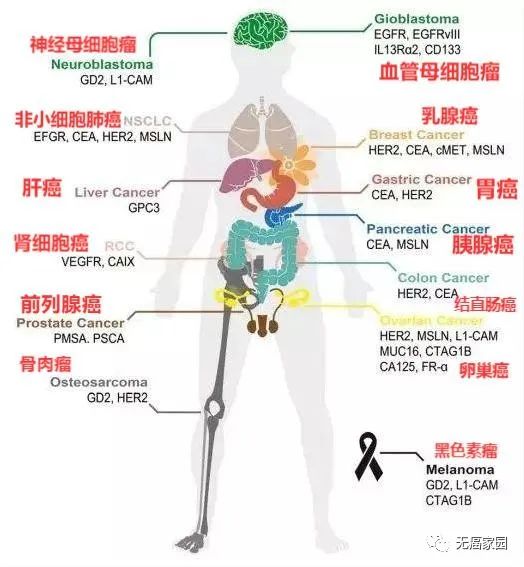
不同癌症的CAR-T靶点分类
CAR-T之父公布首个实体瘤临床试验结果
就在2022年3月21日,“CAR-T之父”Carl June教授及其研究团队在国际知名医学杂志《 Nature Medicine》上公布了首个CAR-T治疗实体瘤临床试验结果。

CAR-T疗法在实体瘤中面临的一个挑战就是免疫抑制性肿瘤微环境(TME),其特点就是高水平的多种抑制因子,包括转化生长因子 (TGF)-β。因此,针对这一抑制因子,Carl June教授及其研究团队开发出一款针对前列腺特异性膜抗原(PSMA)的CAR-T疗法,这款疗法就是对CAR-T进行优化改造,使其可以阻断TGF-β 信号转导以增强患者的抗肿瘤免疫。
通俗点讲,就是对抗肿瘤微环境中的抑制因子TGF-β来使CAR-T治疗实体瘤。该次I期临床试验数据也不负众望,不仅证实其治疗实体瘤的可行性,而且还从总体上确保其安全性。
本次临床试验共纳入18例转移性去势抵抗性前列腺癌(mCRPC)患者,其中13人接受了4个剂量水平的治疗。13人中有4人的前列腺特异性抗原(PSA)下降≥30%,有1人出现大量克隆CAR-T细胞扩增,PSA下降>98%,有5人出现≥2级的细胞因子风暴,均可控。
总的来说,此次临床研究提供了对靶向PSMA 的抗 TGF-β 的 CAR-T 疗法安全性的深入了解,而且让我们看到了细胞免疫疗法对前列腺癌的治疗突破。
攻克实体瘤再传捷报!非病毒载体CAR-T治疗前列腺癌效果喜人
其实要说CAR-T疗法针对前列腺癌的研究,临床数据较为突出的当属P-PSMA-101。
2022年2月17日,在2022年美国临床肿瘤学会泌尿生殖系统癌症专题研讨会(ASCO GU)上,Poseida Therapeutics公司公布了其自体CAR-T细胞疗法P-PSMA-101,在治疗转移性去势抵抗性前列腺癌(mCRPC)患者的1期临床试验的中期结果。

靶向治疗的理想靶点——前列腺特异性膜抗原(PSMA)
P-PSMA-101是一款针对前列腺特异性膜抗原(PSMA)的CAR-T产品,通过对患者自身的T细胞进行基因工程改造,使其可以安全有效地消除肿瘤细胞。P-PSMA-101利用Poseida专有的piggyBac DNA修饰系统开发,该系统能够产出很高比例的干细胞记忆T细胞(Tscm)。
PSMA是一种II型跨膜蛋白,通常在肾小管和十二指肠中表达,并特异性地表达于前列腺癌上皮细胞。在前列腺癌组织中,PSMA的表达明显上调。
研究显示,PSMA在超过90%的前列腺癌细胞表面都出现了过表达(比正常前列腺细胞高100~1000倍),并且在晚期和去势抵抗性前列腺癌患者癌细胞中表达水平更高。因此,PSMA称为前列腺癌诊断及治疗的重要靶点。
治疗前列腺癌,自体CAR-T细胞疗法展现强大潜力
此次公布的1期临床试验中期结果旨在评估P-PSMA-101的安全性、疗效及最大耐受剂量。截止到2021年12月31日,共纳入17例转移性去势抵抗性前列腺癌(mCRPC)患者,其中可评估患者14例。值得一提的是,这些患者平均接受七线治疗,自诊断以来的平均中位时间为6.4年。
在14例患者,分为3组剂量队列进行治疗,具体如下表:
| 剂量队列分组 | 细胞数 | 患者例数 |
| 0.25X106细胞/kg | 平均约2200万细胞 | 6数 |
| 0.75X106细胞/kg | 平均约6100万细胞 | 7数 |
| 2.0x106细胞/kg | 平均约11200万细胞 | 1数 |
试验的关键结果包括:
●71%(10/14)的患者肿瘤标志物前列腺特异性抗原(PSA)水平明显下降;
●36%(5/14)的患者PSA水平下降>50%;
●1例患者显示肿瘤完全消除,并保持10个月以上的持久缓解;
●一些患者的活体组织检查证实,干细胞记忆T细胞(Tscm)这种产品的性质可使CAR-T细胞定向转运到骨骼中,这对前列腺癌等易骨转移的疾病非常重要。
●P-PSMA-101表现出良好的安全性和耐受性。
突破CAR-T疗法局限性,力求更有效,更耐用,副作用更小
在免疫反应中,T细胞发挥着核心作用,能够有效杀死癌细胞,但苦于维持时间短暂(数天或数周不等),这意味着接受CAR-T的患者有复发的可能。
此次P-PSMA-101与一般的CAR-T细胞不同,经非病毒基因递送系统进行工程改造,从而产生很高比例的干细胞记忆T细胞(Tscm)。
Tscm细胞是目前唯一具有自我更新和长寿命的T细胞,会使候选药物更加有效、更耐用,副作用更小。
目前,无癌家园也有多款实体瘤的CAR-T临床试验正在进行招募,有意向者可咨询医学部具体评估病情!
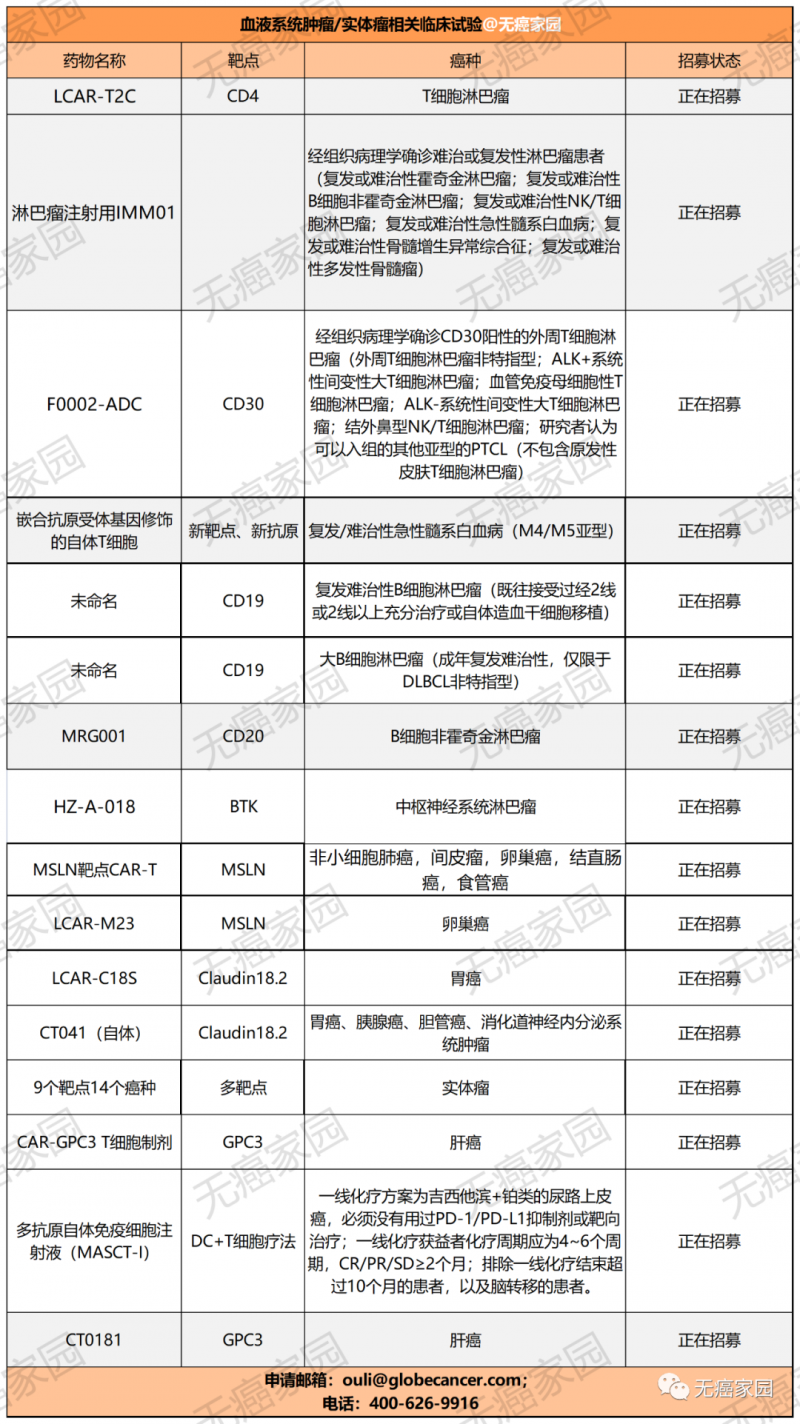
上述都是关于国外学者对于CAR-T治疗实体瘤的临床研究,其实我国医疗研究团队在CAR-T治疗实体瘤方面的临床研究也不甘落后,甚至取得的临床成果在世界中位于前列。
国产CAR-T疗法迎来新进展!剑指胃癌,CT041进入确认性Ⅱ期临床试验
Claudin18.2(CLDN18.2)是Claudin蛋白质家族的一员,位于细胞膜表面,正常情况下仅低水平表达于胃粘膜分化上皮细胞,但在病理状态下,Claudin18.2在多种肿瘤中有的表达显著上调,包括80%的胃肠道腺瘤、60%的胰腺肿瘤。此外,CLDN 18.2活化还可见于食管癌、卵巢癌和肺腺癌中,因此是具有潜力治疗癌症的热门靶点。
基于此,中国研究人员开发了国际上首个针对 Claudin18.2的CAR-T细胞。
作为国际上首个针对Claudin18.2的CAR-T细胞,CT041早在2019年ASCO年会上就崭露头角,当时总客观缓解率为33.3%就已经惊艳世界,如今更加显著的疗效无疑是锦上添花!此次的临床数据展现出对消化系统肿瘤的良好治疗前景!
国产CAR-T疗法CT041首次亮相ESMO
2021年欧洲肿瘤内科学会(ESMO)年会上,由科济药业开发的靶向Claudin18.2(CLDN18.2)自体CAR-T候选产品CT041展现了其在消化系统肿瘤中的突出疗效,可谓是大放异彩!
研究数据格外亮眼
1.所有患者的客观缓解率达48.6%,疾病控制率达73%;所有胃癌患者总客观缓解率为57.1%。
2.既往接受至少2线治疗失败的胃癌患者:客观缓解率为61.1%,疾病控制率为83.3%。
3.而且总体耐受性良好!
CT041取得成就一览
2020年5月,FDA批准了CT041用于治疗claudin18.2阳性的胃、胃食管连接处或胰腺腺癌患者的研究新药(IND)许可;
√2020年,美国FDA授予其孤儿药认定,用于治疗胃癌/胃食管结合部癌;
√2021年,CT041先后获得欧洲药品管理局(EMA)的孤儿药认定、欧洲“优先药物”(PRIME)资格;
√2022年,CT041获美国FDA授予“再生医学先进疗法”(RMAT)资格。
√2022年3月3日,CT041获中国国家药品监督管理局(NMPA)药品审评中心(CDE)同意进入确证性Ⅱ期临床试验!
截止到2022年3月3日,CT041成为全球首个且唯一进入到确证性Ⅱ期临床试验的用于治疗实体瘤的CAR-T细胞候选产品。这是CAR-T攻克实体瘤领域是里程碑般的存在,可喜可贺!
除此之外,还有多款靶向CLDN18.2的CAR-T细胞疗法。例如,由传奇生物研发的LB-1904,用于治疗胃癌或者胰腺癌,目前已经进入临床I期试验。此外,传奇生物还启动了一项靶向Claudin18.2 的CAR-T细胞制剂LCAR-C18S,用于治疗晚期胃腺癌患者,目前也正在进行临床试验招募中。
(想阅读更多关于我国CAR-T疗法在实体瘤领域取得的临床研究成果,请戳下列链接!想要评估病情是否能够接受CAR-T疗法可将病理报告、治疗经历及出院小结提交至无癌家园医学部进行初步评估!)
完全缓解率78%,初代CAR-T疗法Yescarta有望挺进一线治疗
近期关于CAR-T疗法的热点还有一个值得关注,那就是一篇在《自然•医学》发表的论文指出,CAR-T疗法axicabtagene ciloleucel(Yescarta)作为一线疗法治疗高风险大B细胞淋巴瘤患者的临床试验结果,展现出极高的完全缓解率,疗效着实令人惊艳!
研究数据显示,在37例可评估的患者中,单次输注Yescarta后,客观缓解率(ORR)为89%;其中78%的患者在中位随访15.9个月时达到完全缓解(CR)。在数据截止日期,73%的可评估患者仍然获得持续缓解,但中位缓解持续时间、无事件生存期和无进展生存期尚未达到。估计12个月时的无事件生存率为73%,无进展生存率为75%,总生存率为91%。
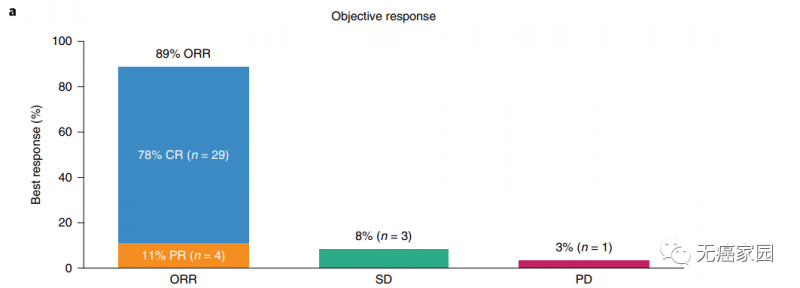
▲患者接受治疗后客观缓解率达到近90%(图源《自然•医学》论文截图)
需要格外强调的是,这是首个在高风险大B细胞淋巴瘤患者中评估一线CAR-T治疗的研究。业界对这些结果感到非常鼓舞,称Yescarta有作为一线治疗的潜力。
天价≠神药!CAR-T疗法虽好,但要理性看待
CAR-T疗法作为新型细胞疗法,近年来在全球癌症细胞免疫治疗领域,可谓是独占鳌头。
但是面对CAR-T疗法,大家还需要保持清醒,理性看待!的确有一部分晚期癌症患者采用CAR-T疗法逆转命运。但它并非万能神药,在实体瘤的治疗上依然充满挑战。
而且与其他的抗癌药一样,CAR-T疗法也有其副作用,例如细胞因子风暴、神经毒性、B细胞终身缺失等,但目前已经有很好的控制方法,能够较好地应对。
因此,基于不菲的价格和副作用,通常CAR-T疗法被用于标准治疗失败(手术、放疗、化疗、靶向治疗、PD-1治疗等)的复发难治性患者身上。
2021年我国迎来了细胞免疫治疗的元年,作为先锋的CAR-T疗法,是未来发展方向之一。CAR-T疗法主要在于改造T细胞来使其识别肿瘤细胞的特殊靶点,理论上,可以有无数种针对不同靶点的CAR-T疗法,这意味着蕴含着无限可能。
希望不久的将来,能够在国内外医学科研工作者的努力下,降低细胞疗法毒副作用,降低价格,突破实体瘤的瓶颈,让越来越多的晚期癌症患者获益!
参考文献
1.https://www.nature.com/articles/s41591-022-01726-1
2.https://www.nature.com/articles/s41591-022-01731-4

































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城