当你发现,晚期非小细胞肺癌在经过如铂类的化疗治疗后又复发或出现转移时,一定很绝望。但即使其他治疗不成功,这些患者可能仍然还有其他选择--OPDIVO。
OPDIVO是什么?
OPDIVO是一种用于治疗晚期非小细胞肺癌的处方药。
T细胞对癌细胞有什么作用?
像雷达一样,免疫系统的T细胞总是在寻找威胁。一旦T细胞识别像癌细胞这样的威胁,他们就会变得活跃,并且攻击他们,以帮助保护你的身体。
有时,癌细胞存在与T细胞上的PD-1受体结合的PD-L1和/或PD-L2标记。这种相互作用通过使T细胞变得失去活性而无法攻击癌细胞来伪装自己,使得癌细胞更容易生长。
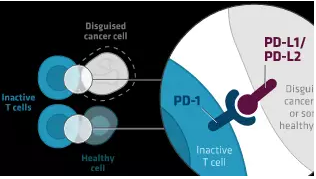
OPDIVO如何在身体内工作?
OPDIVO可能有助于T细胞再次识别和攻击癌细胞,通过阻止癌症的伪装能力。这样可以让您的T细胞激活并进行攻击。在这样做的同时,OPDIVO也可能导致您的T细胞攻击身体健康的细胞。
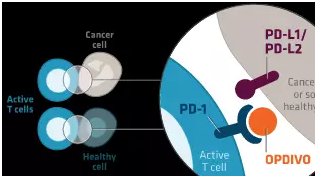
OPDIVO可以结合T细胞上的PD-1受体并阻断与PD-L1 / PD-L2的相互作用。这阻止了癌症自身的伪装能力,并激活T细胞再次攻击癌细胞。在这样做的同时,OPDIVO也可能导致您的T细胞攻击身体健康的细胞。
OPDIVO适合哪些患者?
OPDIVO可能不适合所有人,个别患者结果可能有所不同。
OPDIVO适用于成年患者:
肺癌扩散或进展;
已经尝试了含铂的化疗,但无效或耐药;
如果肿瘤具有EGFR或ALK基因突变,经过针对这些突变的靶向治疗后无效或耐药。
目前不知道OPDIVO对于小于18岁的儿童是否安全。
关于临床试验
OPDIVO是FDA批准的第一个也是的基于两项3期临床试验的免疫治疗,两项临床试验显示,经铂类化疗治疗的晚期NSCLC患者使用opdivo的寿命更长。如果您是这种类型的肺癌,OPDIVO可能是您的选择。
临床试验结果:

272例肺鳞癌患者被随机分为接受标准的多西他赛二线化疗(137例)或PD-1抑制剂Nivolumab(135例)。
与多西他赛化疗(多西紫杉醇)相比,OPDIVO被证明可以降低41%的死亡风险。 50%的患者在接受OPDIVO9.2个月仍然存活,而化疗(多西他赛)为6个月。
此外,OPDIVO被证明在20%的患者中部分或完全收缩肿瘤,而化疗(多西紫杉醇)仅为9%。
半数患者没有肿瘤恶化的时间为OPDIVO3.5个月,化疗为2个月(多西紫杉醇)。

582例晚期非鳞状细胞癌临床试验,在用铂类为基础化疗后扩散或生长的患者,292例接受OPDIVO治疗,290例接受化疗。
与多西他赛化疗(多西紫杉醇)相比,OPDIVO被证明可以降低27%的死亡风险。 50%的患者在接受OPDIVO12.2个月仍然存活,而化疗(多西他赛)为9.4个月。此外,OPDIVO被证明在19%的患者中部分或完全收缩肿瘤,而化疗(多西紫杉醇)仅为12%。
两种治疗方法在患无肿瘤恶化的生存时间长短方面没有差异。
肺癌患者可参加的opdivo临床试验
1、亚洲非小细胞肺癌患者接受二线nivolumab单药治疗的安全性研究
|
序号 |
机构名称 |
主要研究者 |
国家 |
省(州) |
城市 |
|
1 |
上海市胸科医院 |
陆舜 |
中国 |
上海 |
上海 |
|
2 |
广东省人民医院 |
涂海燕 |
中国 |
广东省 |
广州 |
|
3 |
北京肿瘤医院 |
赵军 |
中国 |
北京 |
北京 |
|
4 |
北京301医院 |
陈良安 |
中国 |
北京 |
北京 |
|
5 |
北京协和医院 |
王孟昭 |
中国 |
北京 |
北京 |
|
6 |
中国医学科学院肿瘤医院 |
王洁 |
中国 |
北京 |
北京 |
|
7 |
河南省肿瘤医院 |
马智勇 |
中国 |
河南省 |
郑州市 |
2、I期、选择性IIa期或局部肺实质复发性非小细胞肺癌免疫联合立体定向放射治疗(I-SABR)vs. 单用立体定向放射治疗(SABR)II期临床随机对照试验
临床试验号:NCT03110978
实验目的:探讨PD-1免疫治疗与SABR结合(I-SABR)能否明显提高疗效,减少复发,提高生存率。所有纳入研究的患者被随机分成两组:SABR组和I-SABR组,患者及其主管医生都会知晓患者被分配到哪一组,患者完成随访后视为试验结束。研究预计2022年结束,计划纳入140名患者,进入I-SABR组的患者将免费接受纳武单抗(Nivolumab)免疫治疗。本试验招募患者的一般要求为年龄18周岁以上,男女不限,不接受健康志愿者。
医院和研究者信息:
美国MD安德森癌症中心
张玉蛟教授
3、使用 剂量和最低副作用的,古巴研发的非小细胞肺癌疫苗联合PD-1检查点抑制剂(opdivo)进行治疗
临床试验号:NCT02955290
试验目的:随机I / II期试验研究了重组人EGF-rP64K / montanide ISA 51疫苗(CIMAvax)和nivolumab的 剂量和副作用,并了解它们治疗III-IV期非小细胞肺癌的工作原理。 疫苗治疗,如CIMAvax疫苗可能有助于减缓和阻止肿瘤生长。 单克隆抗体,如纳武单抗,可能会阻断肿瘤细胞生长和扩散所需的蛋白质。 与Nivolumab一起给予CIMAvax疫苗可能会更好地治疗IIIB-IV期非小细胞肺癌患者。
医院和研究者信息:
美国布法罗罗斯威尔派克肿瘤研究所
OPDIVO治疗案例
一名有59年吸烟史的76岁男子,因嘶哑,吞咽困难及体重减轻就诊。 耳鼻喉科检查发现左声带瘫痪。 使用增强(CT)进行检查,其显示双侧肺门区域,纵隔和颈部的肺和淋巴结病中的多个结节。 经进一步检查,他被诊断患有肺腺癌(cT1aN3M1a,IV期)(图1a,b)。 基因检测显示ALK融合基因阳性。
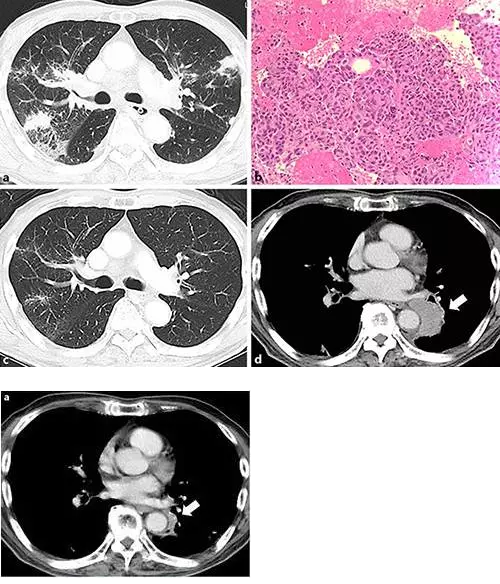
nivolumab治疗后肺癌CT检查及胃癌内镜检查。 a在给予nivolumab 5周后,肺部病变显示明显改善(箭头)。
OPDIVO治疗的相关副作用
考虑接受OPDIVO治疗前需要了解的重要事实:
OPDIVO是一种可以通过免疫系统治疗肺癌的药物。它同时可以使您的免疫系统攻击身体其他部位的正常器官和组织,并可能影响这些器官的工作方式功能。这些问题有时候会变得严重或危及生命,并可能导致死亡。这些问题可能在治疗期间甚至治疗结束后发生。OPDIVO可能有时会导致严重病情或生命危险并导致死亡。 严重的副作用可能包括
1、肺部问题(肺炎);
2、肠道问题(结肠炎)可能导致肠道内的泪液或孔洞;
3、肝脏问题(肝炎);
4、激素腺问题(特别是甲状腺,垂体,肾上腺和胰腺);
5、肾脏问题:包括肾炎和肾衰竭;
6、皮肤问题;
7、大脑炎症(脑炎);
8、其他器官的问题;
9、严重的输液反应。
使用OPDIVO时最常见的副作用包括:
感觉疲惫;
肌肉,骨骼和关节疼痛;
腹泻;
咳嗽;
便秘;
背疼;
发热;
皮疹;
皮肤瘙痒;
恶心;
呼吸急促;
食欲降低 上呼吸道感染;
虚弱。
如何获得opdivo
由于该药物还没有在中国上市,很多患者无法接受这种的免疫疗法。目前的渠道大概有四种:
| 方法 | 优点 | 缺点 |
| 在国内入组新药临床试验 | 无需旅途劳顿,花费较小 | 入组条件苛刻,并且有可能被分到对照组,使用其他药物或者安慰剂治疗 |
| 赴港澳购药,通过非正规方式在国内用药 | 较便捷,花费小 | 非正规渠道用药,无临床用药指导以及监测,药物疗效无法保证 |
| 赴欧美等国家接受正规治疗 | 医疗水平全球领先,患者可以接受系统性诊断以及治疗 | 患者需要赴海外,中介预约费用以及来回路费等花销较大,路途劳顿 |
| 赴日本.新加坡等地医院接受正规治疗 | 医疗水平远超过国内,距离较近,花费与国内持平,患者可以合法使用到药物,病得到系统规范的治疗 | 日本对接诊的国际患者审核非常严格,一般不接受在国内进行过任何治疗的患者 |
目前,对于癌症患者来说,新加坡是购买正版PD-1的 渠道,新加坡药物价格:

OPDIVO适应症及使用剂量总览
|
FDA批准时间 |
适应症 |
使用剂量 |
|
2014年12月22日 |
不可切除或转移性黑色素瘤及ipilimumab治疗后病情进展的BRAF V600E突变患者 |
3 mg/kg ,60分钟以上静脉注射,每两周注射一次 |
|
2015年3月4日 |
铂类化疗后进展的转移性非小细胞鳞癌(NSCLC)患者 |
3 mg/kg ,60分钟以上静脉注射,每两周注射一次 |
|
2015年9月30日 |
与ipilimumab联合用于治疗BRAF V600野生型,不可切除或转移性黑色素瘤患者 |
nivolumab 联合ipilimumab:nivolumab 1 mg / kg,静脉滴注60分钟,随后注射ipilimumab,每3周4次。nivolumab 单药:33 mg/kg ,60分钟以上静脉注射,每两周注射一次,直到病情进展或出现不可耐受的毒性 |
|
2015年10月9日 |
铂类化疗后进展的转移性非小细胞癌(NSCLC)患者 |
3 mg/kg ,60分钟以上静脉注射,每两周注射一次 |
|
2015年11月23日 |
既往接受过抗血管生成疗法的进展期肾细胞癌 |
3 mg/kg ,60分钟以上静脉注射,每两周注射一次 |
|
2016年5月17日 |
自体干细胞移植和本妥昔单抗治疗或三线及以上系统治疗后出现复发获进展的经典型霍奇金淋巴瘤 |
3 mg/kg ,每两周注射一次,直到病情进展或出现不可耐受的毒性 |
|
2016年11月10日 |
治疗含铂化疗后出现局部进展的复发或转移性头颈鳞状细胞癌(HNSCC) |
3 mg/kg ,每两周注射一次,直到病情进展或出现不可耐受的毒性 |
|
2017年2月2日 |
含铂化疗期间或含铂辅助化疗、新辅助化疗一年内出现疾病进展的局部晚期或转移性尿路上皮癌 |
240mg,每两周注射一次 |
|
2017年7月31日 |
氟尿嘧啶,奥沙利铂和伊立替康治疗后出现进展的MSI-H或dMMR转移性结直肠癌(成人或≥12岁儿童) |
240mg,每两周注射一次 |
|
2017年9月22日 |
接受过索拉菲尼(多吉美)治疗后的肝细胞癌患者 |
240mg,每两周注射一次 |
本手册中提供的信息不能代替与专业的肿瘤免疫专家交谈。请登录或登录全球肿瘤医生网咨询肿瘤专家意见。 更多请点击PD1专题介绍







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城