FGFR基因是什么意思,FGFR基因突变靶向药进军实体瘤,已上市和在正在进行临床试验的FGFR抑制剂有哪些
近两年,“广谱抗癌”这个概念成为了癌症靶向治疗的一大热门。越来越多的靶点被证实具有广谱抗癌的潜力,能够实现“只看突变、不看癌种”的治疗模式。
近期,一款已经获批上市、用于胆管癌治疗的FGFR抑制剂Pemigatinib,公布了其治疗多种实体瘤的初期研究数据。尽管样本量比较小,但我们仍然看到了这类药物在实体瘤治疗中的潜力!
这一次,基因药物汇就带大家详细了解一下这类对于胆管癌、肝癌、胃癌等等多类实体瘤都有非常大价值的靶向治疗药物,FGFR抑制剂。
FGFR基因是什么
FGFR的全称是成纤维细胞生长因子受体,分为1~4共四种亚型,正常情况下,这类蛋白质的“足迹”遍布几乎所有器官,贯穿了器官发育、血管生成以及淋巴管生产等等的全过程。
而这类基因的突变,可能导致的癌症也是非常多种多样的。实体瘤中,胆管癌FGFR 1~3突变检出率约有11%~45%,胃癌中也有5%~10%,多类肿瘤当中都可能见到这类突变的存在。
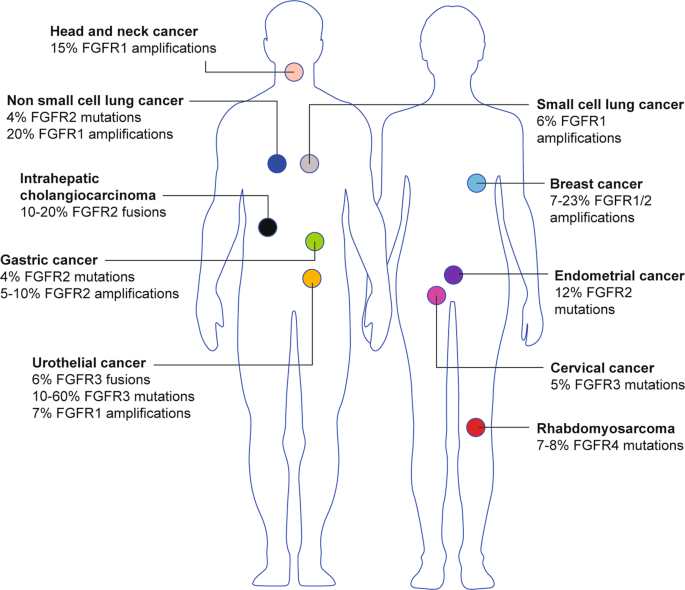
这意味着什么呢?
目前已经上市的FGFR抑制剂,主要适应症集中在胆管癌和膀胱癌上,但在这些适应症以外,FGFR还有更多没被挖掘出来的潜力。不说“广谱抗癌”,但“横跨多个癌种”是非常有希望的!
正在进行临床试验的FGFR抑制剂有哪些
基因药物汇总结过正在招募患者的FGFR抑制剂临床试验,其适应症囊括了胆管癌、肝癌以及多种其它实体瘤,包括肺癌、肾癌、乳腺癌等等,上方图中涉及的、可能存在FGFR突变的癌种,都有涉及。
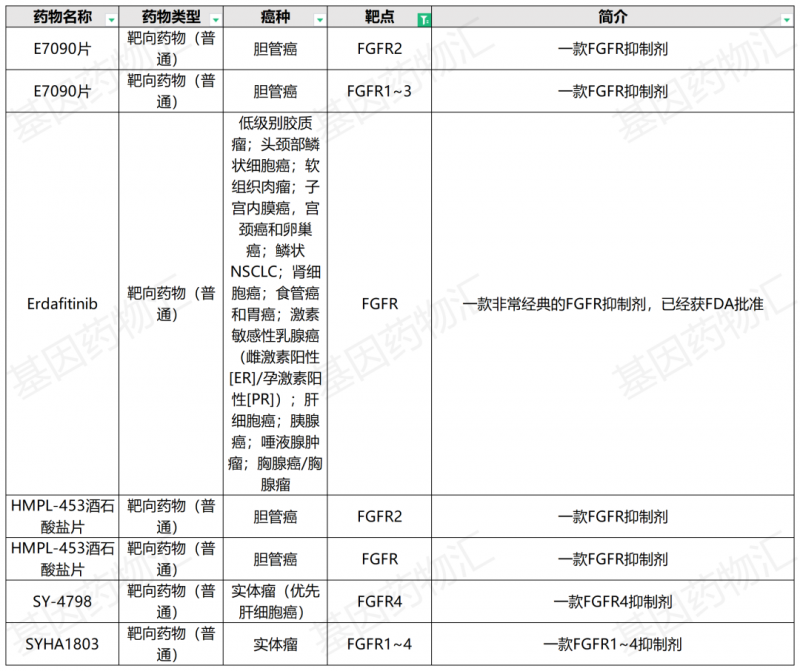
获批上市的FGFR抑制剂有哪些
目前临床上已经有多款FGFR抑制剂获批上市。
1、Bemarituzumab:无进展生存9.5个月
2021年4月20日,FDA授予安进公司研发的Bemarituzumab突破性疗法称号,用于联合改良的FOLFOX6方案(mFOLFOX6),一线治疗FGFR2b阳性、HER2阴性的局部晚期或转移性胃及胃食管交界处癌患者。
根据2021年胃肠道肿瘤专题研讨会上公开的结果,在意向性治疗(ITT)的患者共155例中,Bemarituzumab+mFOLFOX6治疗的患者中位无进展生存期9.5个月,1年无进展生存率52.5%;而使用安慰剂+mFOLFOX6治疗的患者,中位无进展生存期7.4个月,1年无进展生存率33.8%。
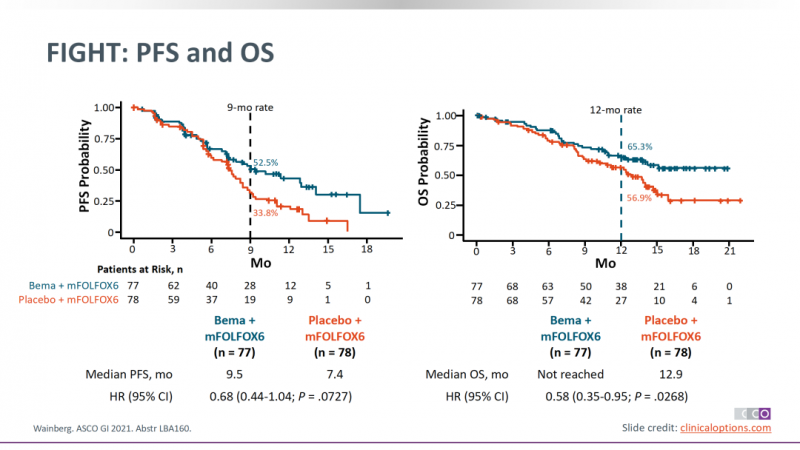
01)亚组分析:表达水平更高,生存期更长
亚组分析同样支持这一结果。在FGFR2b表达水平更高,即免疫组化(IHC)2+/3+占样本的10%以上的亚组中,Bemarituzumab+mFOLFOX6治疗的患者中位无进展生存期为14.1个月,1年无进展生存率57.0%,显著超过了安慰剂+mFOLFOX6治疗患者的7.3个月和26.4%。联合治疗组患者的中位总生存期尚未达到,而安慰剂组患者的中位总生存期为11.1个月。
在FGFR2b表达水平较高,即免疫组化(IHC)2+/3+占样本的5%以上的亚组中,Bemarituzumab+mFOLFOX6治疗的患者中位无进展生存期为10.2个月,1年无进展生存率56.3%,显著超过了安慰剂+mFOLFOX6治疗患者的7.3个月和28.6%。
02)缓解率:高至47%,持续12.2个月
在响应率及持续时间方面,Bemarituzumab+mFOLFOX6治疗的整体缓解率为47%,中位缓解持续12.2个月,显著超过了安慰剂+mFOLFOX6治疗的33%和7.1个月。
FDA在公告中称,超过10%的局部晚期或转移性胃及胃食管交界处癌患者存在FGFR2b的过表达,Bemarituzumab方案将为这部分患者提供全新的解决方案。
02、Pemigatinib:缓解率36%
2020年4月17日,首款针对胆管癌的靶向药物获得了FDA的加速批准,正式走上临床。
Pemigatinib(Pemazyre)是一款FGFR2靶点的靶向药物,获批用于治疗经治的FGFR2突变胆管癌患者。这是首款获批用于治疗胆管癌的靶向药物,为晚期胆管癌的治疗带来了零的突破。
在FIGHT-202实验中共纳入107例不可手术切除或转移性的FGFR2阳性胆管癌患者,所有患者至少接受过1种前线治疗方案并发生了进展。结果显示,患者的整体缓解率为36%,其中3例患者达到了临床完全缓解;患者中位缓解持续时间9.1个月,在达到了临床缓解的患者中,7例患者的缓解持续了超过12个月。
治疗实体瘤,潜力初显
目前针对实体瘤患者的研究还未能达到Pemigatinib的最佳剂量,因此后期研究的数据还可能会有一定的变化或提升。
根据已经公布的初期结果,Pemigatinib治疗的整体缓解率为9.4%,疾病控制率为40.6%;另有超过20%的患者暂时未评估或无法评估反应情况。
其中,FGFR融合/重排的患者整体缓解率最高,为25%;其次是FGFR突变的患者,为23.1%。
所有达到临床缓解的患者,中位缓解持续时间为7.3个月;其中能够明确存在FGFR/FGFR异常的患者,中位缓解持续时间为7.3个月。
整体来说,Pemigatinib治疗实体瘤的潜力非常值得期待!
3、Infigratinib:缓解率23.1%,无进展生存7.3个月
2021年5月29日,FDA宣布批准Infigratinib(Truseltiq)上市,用于治疗曾经接受过治疗的FGFR2融合及重排突变的局部晚期或转移性胆管癌患者。
研究结果显示,接受Infigratinib治疗的患者,整体缓解率为23.1%,中位无进展生存期7.3个月;发生响应的患者中,缓解持续超过6个月的患者占32.0%,中位缓解持续时间5.0个月。
亚组分析结果显示,曾接受过二线治疗的患者整体缓解率为34%,三线治疗及以上的患者整体缓解率为13.8%;最多的患者曾接受过8种前线治疗方式。
4、Futibatinib:缓解率37.3%,无进展生存7.2个月
4月1日,FDA授予FGFR抑制剂Futibatinib(TAS-120)突破性疗法称号,用于治疗经治的FGFR2基因重排及融合突变的局部晚期或转移性胆管癌患者。
根据2020年的ESMO大会上公开的研究结果,在最少6个月的随访期内,所有接受Futibatinib治疗的患者的整体客观缓解率达到37.3%,其中完全缓解率1.5%,部分缓解率35.8%。
整体来说,所有患者的疾病控制率达到了82.1%,中位缓解持续时间为8.3个月;所有达到临床缓解的患者,从开始接受治疗到能够被判定为临床缓解的时间中位数为2.5个月。所有患者的中位无进展生存期为7.2个月;6个月无进展生存率为61%,6个月总生存率为86%。
5、BLU-554:对肝癌有较好疗效,胆管癌试验正在进行
BLU-554是一款FGFR4抑制剂,目前其在肝癌适应症的临床试验中已经取得了一定的疗效。
根据国际肝癌大会上曾经公开的研究数据,BLU-554治疗FGF 19(FGFR4的配体)高表达的晚期肝癌患者,整体缓解率16%,疾病控制率68%。
目前,BLU-554治疗胆管癌患者的国际中心临床试验正在进行,BLU-554与PD-1抑制剂联合治疗肝癌的中国中心临床试验也已经开展。
这个靶点的临床试验项目非常多!如果胆管癌患者通过检测发现了存在这种突变,一定要用上这些药物。大家可以联系基因药物汇了解试验详情,将病历资料发送给招募中心的老师们,让老师们帮助大家做初筛,判断是否可以参加试验。
如果没做过检测也不要担心,部分项目有自己合作的检测机构,我们也有方舟援助计划帮助大家更省钱地做检测。


































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城