世界上第一位被CAR-T疗法"治愈"的幸运儿Emily18岁了,至今已经11年无癌了
2023年5月10日,Emily 已经11年没有癌症了!
时间,对于每一个癌症患者来说有着非凡的意义。因为每跨过一年,都意味着距离治愈又近了一步,而跨过10年,则意味着已经完全临床治愈,这也是所有癌症患者希望出现的奇迹。
11年无癌!世界上第一位被CAR-T"治愈"的幸运儿Emily18岁了
提到Emily Whitehead,相信有很多病友都听过她的大名。她是世界上第一位接受 CAR T 细胞治疗的白血病 (ALL) 患儿,如今,她体内癌细胞已经完全消失了11年,连前美国总统奥巴马都被她的抗癌经历震撼而亲自接见,她也成为这一史诗级疗法的代言人被载入史册。
每一年,艾米莉都会用拍照打卡的形式,宣告自己又成功的跨过一年。
今年,是艾米莉无癌生存的第11年。2023年5月10日,艾米莉庆祝自己成为首位接受 CAR T 细胞治疗后成功治愈11周年。她已从十年前那个差点被死神夺去生命的光头小女孩成为一个亭亭玉立的18岁花季少女。

2023年的Emily
2012年的Emily
Emily无疑是幸运的。但整个治疗过程中,Emily展现的持续对抗病魔的勇气,父母对医生的信任,对临床试验的支持,都是治疗获得成功不可缺少的要素,他们坚持对病情的公开,也是带给社会的满满正能量,给无数病友带来战胜癌症的信心。
然而,今年的照片将是最后一张照片。
艾米莉的父母说,作为一个家庭,我们不再以癌症发生后的岁月为标准。艾米丽现在已成年,她已准备好继续她的生活,超越癌症,并以更多方式改变世界。艾米丽现在被认为已经痊愈,并且最近庆祝了她的 18 岁生日。她期待几周后高中毕业,今年秋天她将在宾夕法尼亚州立大学上大学。
全球癌症治疗变革--CAR-T疗法十年里程碑事件
Emily无疑是幸运的。但这个时刻并不仅仅对她意义重大,这也是医学领域的一个重要里程碑,这意味着CAR-T疗法将给全球带来历史性的变革。我们在为Emily庆祝的同时,也一起回顾下CAR-T疗法披荆斩棘,走向巅峰的十年。
01、2012:第一位儿科患者接受CAR-T
2012年4月,Emily 成为第一个接受实验性新型 CAR-T 细胞疗法的儿科患者。在两次复发并用尽所有标准治疗后,她参加了一项评估 CAR-T 药物 Kymriah 治疗急性淋巴细胞白血病的 I 期临床试验。她的 T 细胞被提取出来并用 CAR 进行基因改造,然后将这些靶向 CAR-T 细胞的癌细胞重新注入她的血液中。 2012 年 5 月,这个历史性的时刻,Emily被证实癌症被完全清除,此后一直处于缓解状态。
02、2014:FDA 授予CAR-T "突破性疗法"称号
2014年7月,诺华成为第一家获得FDA突破性治疗指定的 CAR-T 细胞疗法的制药公司,当时代号为 CTL019 的 CAR-T疗法是全球领先的,早期临床数据显示 CTL019 治疗成人和儿童患者复发/难治性急性淋巴细胞白血病结果积极。此后,全世界都注意到了这些曾鲜为人知的疗法的挽救生命的潜力。
03、2017:FDA 批准前两种CAR-T疗法:Kymriah 和 Yescarta
2017 年是 CAR-T 具有里程碑意义的一年,因为两种CAR-T疗法获批上市。
2017年8月,诺华推出的名为 Kymriah 的 CAR-T 疗法获批上市。这种针对 B 细胞急性淋巴细胞白血病 (ALL) 的一次性治疗在三个月后显示出对无标准治疗无反应患者的 83% 完全缓解率!
2017年10月,FDA批准了第二款CAR-T疗法。吉利德是第二家将 CAR-T 疗法推向市场的公司。这家大型制药公司在 FDA 批准 Kite 的 CAR-T 细胞疗法 Yescarta 前几周收购了CAR-T 开发商 Kite Pharma。该疗法使 72% 的侵袭性 B 细胞非霍奇金淋巴瘤患者获得缓解,其中51%的患者获得完全缓解。
04、2019:中国研发新型CAR-T疗法率先突破实体瘤瓶颈
在实体肿瘤领域,我们国家领跑全球,取得备受世界瞩目的成绩,研发出了国际上首个靶向Claudin18.2的实体瘤CAR-T疗法。
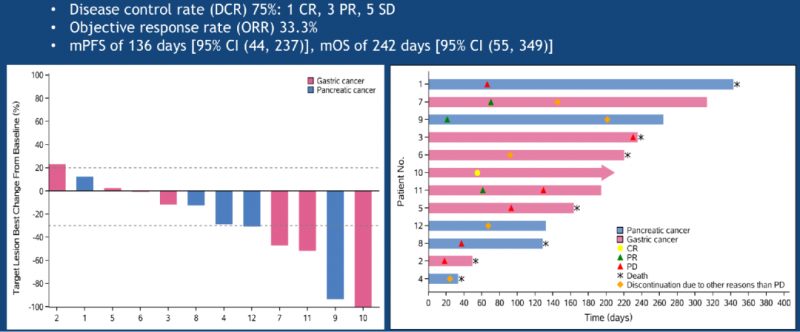
2019 ASCO年会上,中国研发的CAR-Claudin18.2 T 细胞治疗胃癌/胰腺癌的临床数据震撼全场,靶向claudin18.2 CAR T细胞治疗12例转移性腺癌(胃癌7例,胰腺癌5例),总客观缓解率为33.3%,未发生严重不良事件、治疗相关死亡或严重神经毒性。
05、2020:中国CAR-T细胞疗法-CT041在美国获批临床
2020年5月,FDA批准了CT041人源化抗claudin18.2自体嵌合抗原受体CAR-T细胞用于治疗claudin18.2阳性的胃,胃食管连接处或胰腺腺癌患者的研究新药(IND)许可!这意味着由中国自主研发的,世界上第一个针对claudin18.2靶向的CAR-T细胞疗法-CT041将正式在美国开展临床试验,中国的CAR-T疗法登上世界舞台!
这项多中心,1b期临床试验评估自体CT041细胞疗法在晚期胃癌或胰腺癌中的安全性和有效性。
此外,2020年7月,第三款CAR-T疗法Tecartus获得FDA批准用于复发性或难治性套细胞淋巴瘤。
06、2021:FDA批准两款CAR-T疗法
尽管全球都笼罩在新冠疫情的阴霾下,但CAR-T 在血液恶性肿瘤的临床开发和监管认可丝毫没有停下脚步。
2021年2月,FDA 批准了第四个 CAR-T 细胞疗法。Breyanzi 是由百时美施贵宝公司联合 Juno Therapeutics 开发的,用于治疗某些类型的非霍奇金淋巴瘤。虽然该疗法治疗后的完全缓解率为54%!
2021年3月,FDA 批准了第五款,也是首款针对BCMA靶点的CAR-T疗法,用于多发性骨髓瘤。这就是由 Bluebird Bio 和 Bristol-Myers Squibb 开发的 Abecma 。
07、2021:中国开启CAR-T细胞治疗元年
2021年,中国的肿瘤患者终于迎来了细胞免疫治疗元年!两款CAR-T疗法先后获批。
2021年6月,国内首款CAR-T疗法,复兴凯特的阿基伦塞注射液上市,治疗复发难治性淋巴瘤。这是第一个独立开发的 CAR-T,并在美国获得 1 类生物制剂产品地位。
该批准是根据 RELIANCE 研究,也是中国当时最大的 CAR-T 临床研究。据报道,总的客观缓解率(ORR) 为 77.6%,完全缓解率(CR )为 51.7%。
2021年9月,第二款CAR-T疗法,药明巨诺的瑞基奥伦塞注射液在中国成功上市,治疗复发难治性淋巴瘤。
08、2022:首款国产CAR-T疗法Carvykti在美国获批上市
FDA批准传奇生物的靶向BCMA CAR-T疗法--Carvykti 上市,用于治疗复发或难治性多发性骨髓瘤(R/R MM)患者,这些患者既往接受过四种或四种以上的治疗,包括蛋白酶体抑制剂、免疫调节剂和抗CD38单克隆抗体,给晚期走投无路的患者带来了新的选择,同时它也有了自己的大名--西达基奥仑赛。值得一提的是,这是首款国产的CAR-T免疫疗法获得FDA批准上市,意味着中国的CAR-T疗法正式登上世界舞台!2022年2月28日,这是中国抗癌史上又一值得镌刻的里程碑!
总缓解率(ORR)竟然高达98%(95%CI:92.7-99.7),更值得一提的是,78%的患者获得了严格的完全缓解(sCR,95%CI:68.8-86.1),这意味着即使是晚期患者,近80%在接受CAR-T治疗后,病灶也完全消失了!
09、2022:沈琳教授团队实体瘤CAR-T疗法成果登顶《nature medicine》
2022年5月9日,国内胃肠道领域享负盛名的北京大学肿瘤医院沈琳教授团队开展的Claudin18.2 CAR-T(CT041)疗法最新1 期试验中期结果在国际权威学术期刊《Nature Medicine》在线发表,显示 CT041 具有显着的疗效和出色的耐受性,总体客观缓解率(ORR)高达48.6%,再次引起轰动!
这是距离2021年ESMO大会上公布数据后,再次让全球瞩目!这款由中国自主研发的,世界上第一个获得临床试验许可(IND)的针对claudin18.2靶向的CAR-T细胞疗法-CT041已经成功登上世界舞台!中国的抗癌新药研究闪耀全球!骄傲!客观缓解率高达48.6%!沈琳教授团队实体瘤CAR-T疗法成果发表
10、2022:CAR-T 患者缓解10年
2022 年5 月 10日标志着 Emily Whitehead 10 周年,她是第一位接受 CAR-T 治疗其 ALL 的儿科患者,已经摆脱癌症——这对于她和全球都是具有里程碑意义的时刻,值得庆祝。
此外,全球首批接受CAR-T疗法的幸存者,还有有两位成人患者至今持续缓解时间超过十年!这是目前已知的最长的CAR-T治疗后的响应时间!对两名患者的分析也登上了国际顶级期刊《Nature》上。CAR-T疗法已成为人类攻克癌症历史上最值得镌刻的里程碑之一,为癌症患者创下了长生存“神话”。
2023精彩预告!3大CAR-T疗法即将上市
01、白血病--赫基仑赛(CAR-T)
药品信息
药物名称:赫基仑赛
研发公司:合源生物
药物介绍:赫基仑赛是一款靶向CD19 CAR-T细胞治疗产品,用于治疗成人复发或难治性B细胞型急性淋巴细胞白血病(r/r B-ALL)。临床数据显示:赫基仑赛注射液对于r/r B-ALL患者显示了持久的高缓解率(ORR达82.1%)。2022年12月,NMPA已正式受理赫基仑赛注射液(拟定)的新药上市申请。
CDE受理时间:2022年12月
02、骨髓瘤--伊基仑赛(CAR-T)药品信息
药物名称:伊基仑赛
研发公司:信达生物/驯鹿生物
药物介绍:伊基仑赛由信达生物和驯鹿生物联合开发的全人源靶向BCMA的自体CAR-T细胞疗法,2022年6月,伊基仑赛的上市申请被NMPA受理并被纳入优先审评,用于治疗复发/难治性多发性骨髓瘤。值得一提的是,这是国内首款申请上市的靶向BCMA的自体CAR-T细胞产品。
CDE受理时间:2022年6月
03、骨髓瘤--泽沃基奥仑赛(CAR-T)药品信息
药物名称:泽沃基奥仑赛(zevorcabtagene autoleucel)
研发公司:科济药业
药物介绍:泽沃基奥仑赛是一款全人抗自体BCMA CAR-T细胞治疗产品,用于治疗复发/难治多发性骨髓瘤。2022年10月,泽沃基奥仑赛的上市申请获得NMPA受理,并被拟纳入优先审评。
CDE受理时间:2022年10月
中国CAR-T疗法领跑全球,造福患者
曾经,这种先进的治疗技术一直掌握在医疗发达国家,很多病友只能苦苦等待国内的临床试验审批等一列流程走完,但是癌症患者真的等不起,有无数的病友们在等待中遗憾离开。这一切将被改写!
据2020年发表在顶级期刊《Nature》的文献显示,截止到2020年6月30日,截至2020年6月,357个CAR-T试验在中国,在美国有256个试验,58个试验在其他国家,中国CAR-T研究已经超越美国成为临床试验最多的国家,领跑全球!
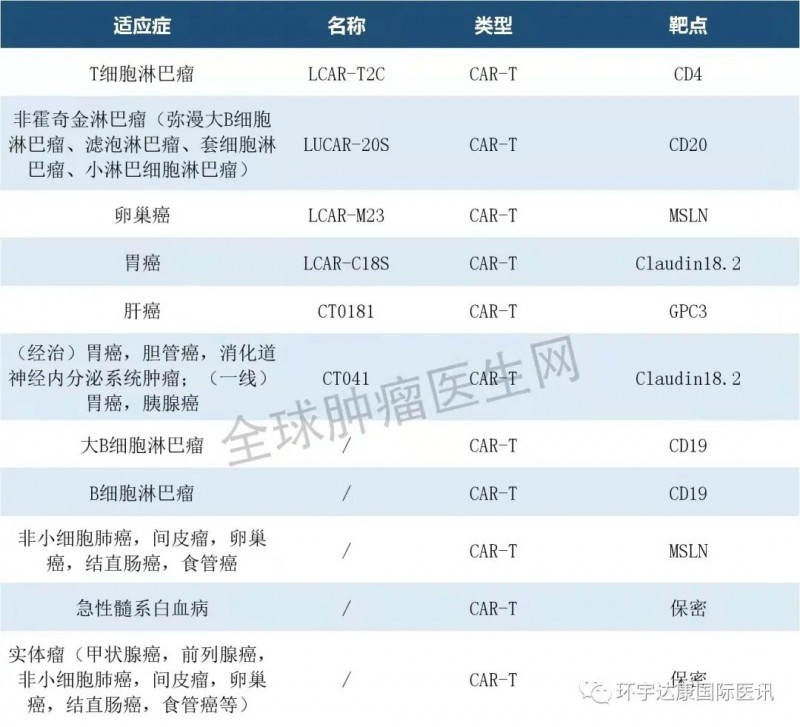
好消息是,目前国内的CAR-T疗法正在招募各类实体瘤和血液肿瘤患者,这意味着,大家有机会免费接受这种全球前瞻疗法的治疗,这是中国患者的福音!(注:部分项目已停止招募,详情咨询医学部评估匹配)
申请流程
1.按要求将病历资料提交至全球肿瘤医生网医学部;
2.医学部初步评估后匹配合适的临床试验;
3.向相应的试验中心提交病历资料;
4.评估通过后协助患者参加临床试验。
经过近30年的发展,CAR-T细胞疗法已成为肿瘤治疗领域的一大新兴支柱,迄今为止,CAR-T技术已经发展到了第五代,使用膜受体(第五代)的 CAR-T 细胞根据不同的原理起作用,还添加了安全门控系统,使CAR-T疗法具有更好的安全性和更宽的治疗窗口。在个性化医疗的时代,无论是单一疗法还是联合疗法,CAR-T无疑是医药领域火热的研究对象,希望今后能够取得更多突破,在血液肿瘤和实体瘤的治疗上展现其独特的实力!

































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城