中国新型TCR-T细胞疗法TAEST16001获美国FDA新药申请批准,更多的TCR-T疗法为肉瘤、肝癌、宫颈癌、胰腺癌等带来生存希望
近期国际知名期刊《Cell Rep Med》报道了我国首个获美国FDA研究性新药申请批准(IND)的TCR-T细胞产品——TAEST16001的Ⅰ期临床研究成果,为过继性T细胞免疫疗法在晚期软组织肉瘤的临床转化中迈出了关键一步,也有望成为全球第二款上市的针对实体瘤的TCR-T细胞产品!
我国首款TCR-T产品IND获批,剑指滑膜肉瘤

▲截图源自“PMC”
TAEST16001是香雪生命科学技术公司自主研发的TCR-T细胞产品,本次Ⅰ期临床试验共入组12例HLA-A*02:01阳性且表达NY-ESO-1抗原的晚期软组织肉瘤患者。其中10例患有滑膜肉瘤,2例患有脂肪肉瘤(1例粘液样脂肪肉瘤,1例去分化脂肪肉瘤),中位年龄为33(25-67)岁,58.3%(7/12)的患者为男性。83.3%的患者入组前接受过至少2种化学药物治疗。入组后,所有患者均接受改良淋巴细胞清除术,之后给予TAEST16001细胞输注治疗。
经过43天的中位治疗时间后,其中9名(75%)患者显示肿瘤消退(图1),中位缓解时间(TTR)为1.9个月,中位缓解持续时间为13.1个月,6例(50%)患者在第一次放射学评估后肿瘤负荷持续下降。在主要分析时,12例患者中有5例获得部分缓解,客观缓解率(ORR)为41.7%(95%CI,15.2–72.3)。5例[41.7%(95%CI,15.2–72.3)]患者疾病稳定,疾病控制率为83.3%(95%CI,51.6–97.9)。中位无进展生存期(PFS)为7.2个月(95%CI,2.5–11.8)。
图1 单个可评估患者的最佳临床反应
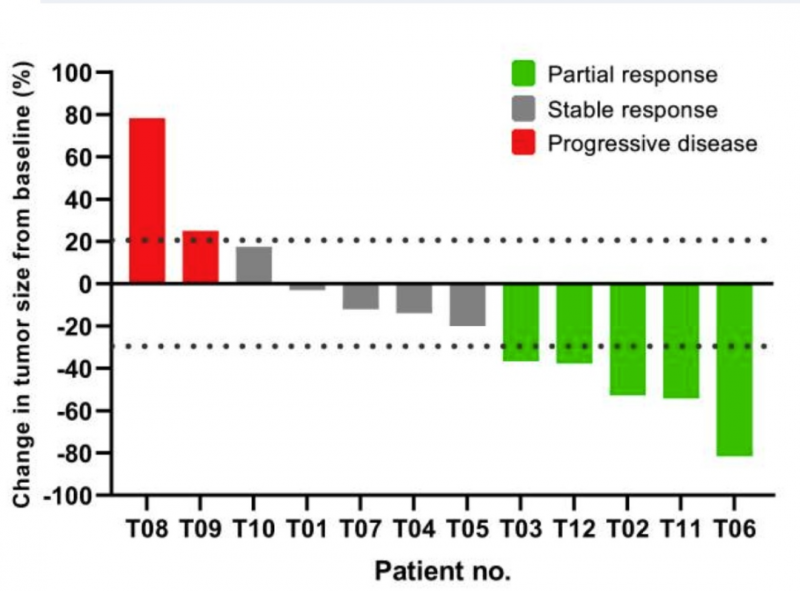
▲图源“Cell Rep Med”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
TCR-T疗法:实体瘤克星
“T细胞受体工程化T细胞疗法”即“TCR-T(engineered T cell receptor-T cell,TCR-T)细胞疗法”,是从患者自身获取外周血单个核细胞(PBMC)样本,通过基因工程改造的方法,将筛选到的高亲和力T细胞受体(TCR)导入T细胞,使其能寻找并特异性识别肿瘤抗原,并精准地杀死癌细胞。
2022年初,美国食品和药物管理局(FDA)批准了一款名为“Kimmtrack”的TCR-T疗法,用于治疗葡萄膜黑色素瘤,自此打开了实体瘤治疗的新格局。
如何寻求TCR-T疗法帮助
目前有几款研发中的TCR-T疗法正急招乙型肝炎病毒相关肝细胞癌、头颈部肿瘤(口腔癌、喉癌等)、晚期宫颈癌、肛门癌患者。
想参加临床试验的患者可将近期病理报告、治疗经历、出院小结等资料,提交至医学部,进行初步评估。
TCR-T对抗乙肝病毒相关肝细胞癌,抗癌与抗病毒双管齐下
SCG101是一种乙肝抗原特异性的TCR-T细胞疗法,由星汉德生物公司研发,可特异性靶向HBV抗原相关T细胞表位,具有抗肿瘤和抗病毒的双重功效,可有效清除HBV-HCC肿瘤细胞、HBV-DNA整合的癌前病变细胞、HBV感染细胞,达到“一箭双雕”的效果!
2023年6月,国际细胞与基因治疗大会(ISCT)上公布了SCG101的突破性临床数据。本次临床试验有一例乙型肝炎病毒(HBV)相关肝细胞癌(HCC)患者入组,入组后给予单剂SCG101输注治疗,且未接受其他抗肿瘤治疗,治疗结果如下:
1、肿瘤缓解:患者在治疗第28天,肿瘤靶病灶比基线缩小66%,达到部分缓解(PR);并在治疗第4个月时,病灶进一步缩小74.5%;另一处病灶则完全消失。截至数据统计时,该患者仍处于持续缓解状态,肿瘤未进展时间>6.9个月。
图2 HBV相关肝细胞癌患者,回输SCG101前后影像学变化
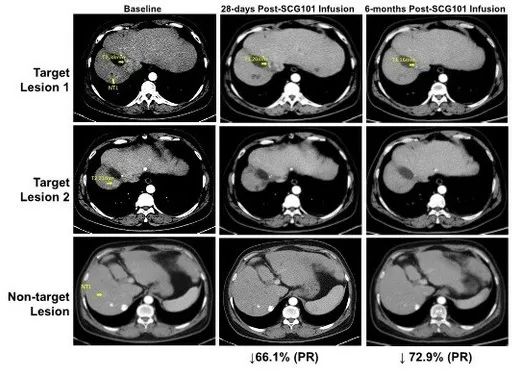
▲图源“CISION”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
2、HBV感染改善:回输SCG101前后,患者肝脏免疫组化结果显示,乙肝表面抗原阳性肝细胞达到100%清除;HBsAg(HBV血清学标志)在治疗前高达557.96 IU/mL,输注SCG101第7天,该值降至1.3 IU/mL,第28天降至0.08 IU/mL(详见图3)。
图3 输注SCG101前后,HBsAg值变化
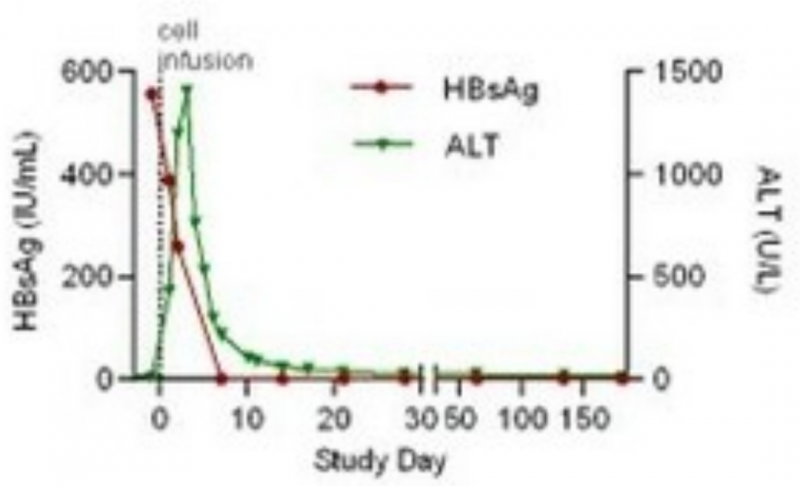
▲图源“CISION”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
TCR-T治疗宫颈癌,疗效持续超过29个月
近期一款特异性靶向MAGE A3/A6(黑色素瘤相关抗原-A3/A6)的TCR-T细胞产品——“KITE-718”,在17例转移性实体瘤中表现出优异的疗效。其中,4例宫颈癌患者出现不同程度的缓解。1例转移性宫颈癌患者因原发性宫颈癌并有淋巴结转移,接受放射治疗加6周期顺铂治疗,获得完全缓解,肿瘤完全消失,疗效持续>29个月。
据悉,MAGE A3/A6抗原普遍存在于宫颈癌、卵巢癌、肺癌、膀胱癌、头颈癌、食管癌等多种癌种中。
胰腺癌经TCR-T治疗,转移灶消退,部分缓解率达72%
一例患有KRAS突变的进行性转移性胰腺癌患者,经手术、放化疗治疗无效后,癌细胞扩散至肺部。入组后,接受环磷酰胺+托珠单抗的预处理治疗,之后回输靶向KRASG12D的TCR-T细胞。
结果显示,经TCR-T治疗后第21天,该患者的血小板计数和绝对中性粒细胞恢复;治疗第1个月的计算机断层扫描显示,患者肺转移病灶消退;治疗后6个月,部分缓解(PR)率达72%。
图4 TCR-T治疗前后,患者胸部计算机断层扫描对比
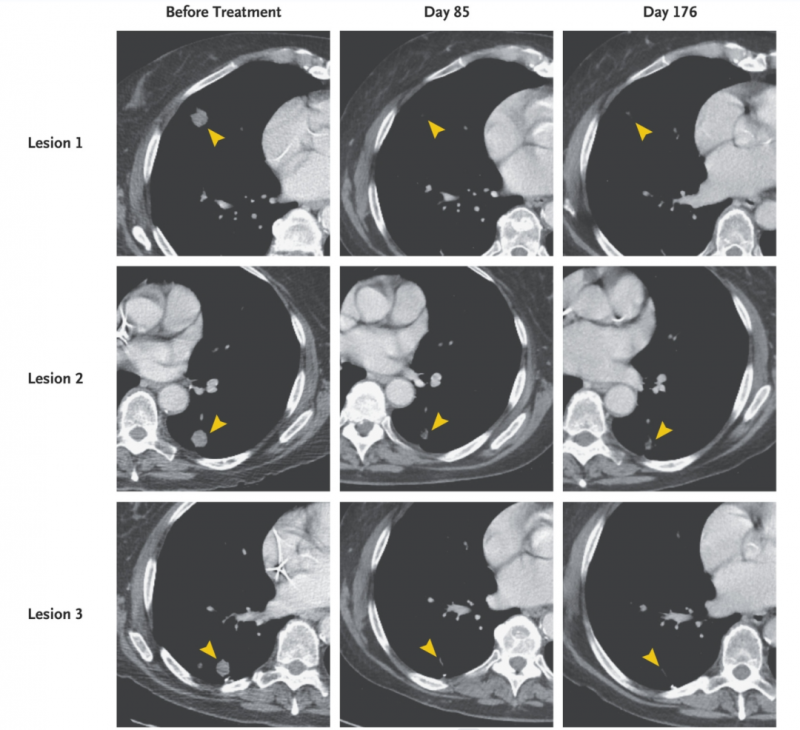
▲图源“NEJM”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
小编有话说
TCR-T疗法虽与CAR-T同属于T细胞疗法,但其在治疗非小细胞肺癌、肝癌、滑膜肉瘤、宫颈癌、黑色素瘤等多款实体瘤领域具有独特的优势,临床研究已在一定程度上,证实了TCR-T疗法在治疗癌症和病毒感染方面的可行性、安全性和有效性,并开创了一种“双管齐下”的针对癌症和病毒感染的新型治疗方案。希望随着越来越多临床研究的不断开展,会有更多的TCR-T细胞产品问世,让更多患者受益!
如果您也想寻求TCR-T细胞疗法或国内外其他治疗新技术的帮助,可先将病理报告等相关资料,提交至医学部,初步评估病情。
参考资料
[1]Pan Q,et al.Phase 1 clinical trial to assess safety and efficacy of NY-ESO-1-specific TCR T cells in HLA-A∗02:01 patients with advanced soft tissue sarcoma.Cell Rep Med. 2023 Aug 15;4(8):101133.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10439245/
[2]https://www.nejm.org/doi/full/10.1056/NEJMoa2119662
[3]https://hk.prnasia.com/story/406654-2.shtml

































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城