CLDN18.2 CAR-T治疗胰腺癌一个月后肿瘤完全消失,临床缓解8个月
2024年3月26日,安斯泰来制药集团宣布,日本厚生劳动省于2024年3月26日批准了VYLOY(zolbetuximab)的新药上市申请,作为首创靶向Claudin 18.2 (CLDN18.2)的单克隆抗体,zolbetuximab用于治疗Claudin 18.2阳性的不可切除晚期或复发性胃癌。VYLOY成为目前世界首个且唯一被批准的CLDN18.2靶向疗法。

截图源自prnewswire官网
Claudin18.2(CLDN18.2)是Claudin蛋白质家族的一员,位于细胞膜表面,正常情况下仅低水平表达于胃粘膜分化上皮细胞,但在病理状态下,Claudin18.2在多种肿瘤中有的表达显著上调,包括80%的胃肠道腺瘤、60%的胰腺肿瘤。此外,CLDN 18.2活化还可见于食管癌、卵巢癌和肺腺癌中,因此是具有潜力治疗癌症的热门靶点。
面对如此“穷凶极恶”的胰腺癌,医学研究者们并没有气馁,而是将目光投向近几年来的热门疗法——嵌合抗原受体T细胞免疫(CAR-T)疗法。
治疗1个月后肿瘤完全消失!临床缓解8个月!CAR-T疗法直击胰腺癌
2024年2月29日,国际知名杂志《Front Immunol》刊登了一则关于靶向claudin18.2的CAR-T细胞疗法治疗晚期胰腺癌患者达到完全缓解疗效的病例报告,引起医学界人士的广泛关注,这表明CAR-T疗法的成功不仅在恶性血液肿瘤方面有目共睹,并且已经延续到实体瘤范畴,尤其是被称为“癌王之王”的胰腺癌领域。

截图源自《Front Immunol》官网
这例72岁男子因胆管占位性病变及糖类抗原19-9(CA19-9)水平升高,于2021年6月11日在香港玛丽医院接受胰十二指肠切除术。术后病理显示胰腺导管腺癌(pT2N2M0,III 期)。随后接受8个周期的吉西他滨联合卡培他滨方案作为术后化疗,直至2022年2月。辅助化疗期间血清CA19-9水平持续升高并达到100 μ/mL以上,但CT扫描未见肿瘤复发迹象。然而,2022年8月5日磁共振成像(MRI)显示肝转移和腹膜转移,这表明疾病进展。因此,化疗方案调整为替加氟、吉美嘧啶和奥替拉西钾联合用药。不幸的是,2022年9月20日,患者左侧气管旁淋巴结肿大,提示胰腺癌细胞已转移至颈部淋巴结。
随后,患者转诊后进一步治疗转移性胰腺癌,自2022年10月1日起接受2个周期的FOLFIRINOX方案(氟尿嘧啶、亚叶酸、伊立替康、奥沙利铂)治疗。在 FOLFIRINOX 化疗期间,患者出现疲劳、恶心、呕吐、体重减轻、中性粒细胞减少和贫血。由于耐受性差,患者拒绝继续FOLFIRINOX方案。鉴于多线治疗后肿瘤复发转移(图1A),患者及其家属强烈要求参与CAR-T细胞治疗的临床试验。
因此,通过免疫化学检测肿瘤组织中claudin18.2的表达情况,结果显示claudin18.2高表达(肿瘤细胞阳性率≥70%)(图1B)。因此,该患者参加了claudin18.2靶向CAR-T细胞疗法的临床试验(NCT05620732)。
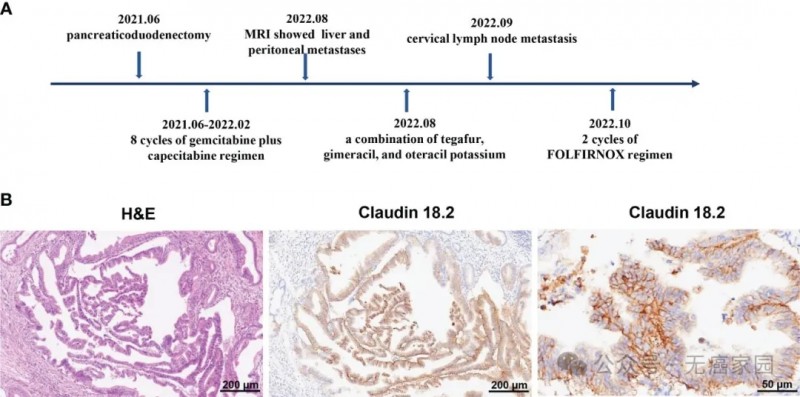
图1:(A)claudin18.2靶向CAR-T疗法之前的多线疗法的时间线,包括胰十二指肠切除术和辅助化疗,以及多发转移。(B)术后病理显示胰腺导管腺癌。左边是肿瘤组织的苏木精和伊红(H&E)染色(原始放大倍数100×),中间是claudin 18.2的免疫组织化学(IHC)染色(原始放大倍数100×),右边是claudin 18.2的IHC染色(原始放大倍数100×)。原始放大倍数400×)。
为了制造靶向claudin18.2的CAR-T细胞,我们于2022年9月30日从患者的外周血中采集了自体T细胞,然后进行基因工程改造以表达含有人源化抗claudin18.2的嵌合抗原受体(CAR)单链可变片段(scFv)。随后,患者于2022年11月16日接受FC方案的淋巴清除化疗。
经过经验性抗感染治疗和支持治疗后,患者临床病情好转。鉴于患者年龄较大、耐受性较差,于2022年11月21日单次输注claudin 18.2靶向CAR-T细胞进行治疗,中间经历轻微的炎症反应及腹泻后,患者的第14天外周血中CAR-T细胞扩增达到峰值水平。令人惊讶的是,CAR-T细胞输注1个月后,肿瘤标志物CA19-9的水平从1100 U/mL显著下降至25.85U/mL,并达到正常范围,并且PET-CT显示肿瘤标志物CA19-9的水平完全消失。肿瘤病变包括颈部淋巴结转移和肺转移(图2A、B)。经过临床评估,患者在 Claudin 18.2 靶向 CAR-T 细胞治疗后 1 个月获得完全缓解。此外,在claudin 18.2靶向CAR-T细胞治疗后1个月,中枢记忆CD4+ T细胞的比例明显增加,但中枢记忆CD8+ T细胞的比例在第17天达到峰值,然后经历了下降。CAR-T细胞治疗5个月后CA19-9维持正常水平,PET-CT扫描显示CAR-T细胞治疗8个月后颈部和肺部病变没有复发。
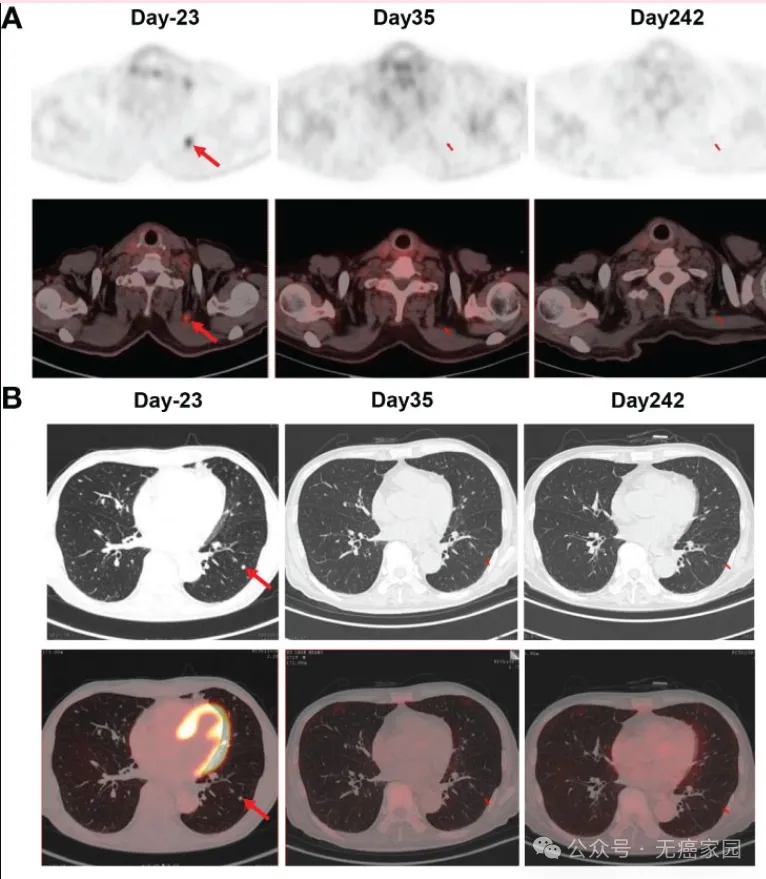
图2:(A) PET/CT显示claudin18.2靶向CAR-T细胞治疗1个月后颈部淋巴结转移消失,CAR-T细胞输注后8个月仍保持缓解状态。(B) PET/CT显示claudin18.2靶向CAR-T细胞治疗1个月后肺转移消失,CAR-T细胞输注后8个月仍保持缓解状态。
晚期胰腺癌患者的中位生存时间为 4~8个月。尽管该患者在claudin18.2靶向CAR-T细胞治疗后8个月最终出现抗原阴性复发,但本研究表明claudin18.2靶向CAR-T细胞疗法在转移性胰腺癌中具有优异的疗效。截至目前,该患者在接受claudin18.2靶向CAR-T细胞治疗后已存活12个月。
此外,EGFR和MSLN在胰腺癌细胞中也高表达,这些靶点已在临床试验中得到探索。在一项1期临床试验中,16例患者接受了抗EGFR CAR-T细胞治疗,4例患者在2~4个月内获得部分缓解,8例患者在2~4个月内获得疾病稳定。在另一项 1 期临床试验中,6 例难治性胰腺癌患者接受了 MSLN 特异性 CAR-T 细胞治疗,只有 2 例患者达到疾病稳定,无进展生存时间分别为 3.8 和 5.4 个月。在这两项临床试验中,不良事件是可控且可逆的。与这两项1期临床试验相比,本次研究中的患者获得了更深、更长的缓解时间。
目前无癌家园有多种针对Claudin18.2的新疗法正在招募胃癌,胰腺癌等实体肿瘤患者,如CAR-T细胞疗法CT041、SZ9287注射液及Claudin18.2单克隆抗体MIL93注射液。
有意向的患者可向医学部提交病理报告、治疗经历等资料进行初步评估。

































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城