2025年一定要知道的五大胃癌新疗法,100%患者实现肿瘤控制
高达100%患者肿瘤不同程度缩小或控制稳定!2025年,CAR-T,TIL,癌症疫苗等创新疗法为胃癌患者带来新的曙光!
在中国,胃癌是最令人望而生畏的癌症之一,全球将近一半的新发胃癌患者和死亡病例都在中国!更可怕的是,在中国大部分患者确诊时已处于中晚期,治疗的方式非常有限,患者的生存面临着严峻的考验。
近年来,针对HER2,PD-L1,MET,FGFR2,claudin18.2等靶点的药物纷纷问世,为胃癌开启了一个全新的治疗模式,创造了新的可能性。
一、疾病控制率高达100%!国研单抗ASKB589初战告捷
ASKB589 是 AskGene研发的一种创新生物药物,它是一种针对 CLDN 18.2 的重组人源化单克隆抗体。该药物通过与表达 CLDN18.2 的癌细胞高亲和力结合,介导抗体依赖性细胞介导的细胞毒作用 (ADCC) 和补体依赖性细胞毒作用 (CDC)。ASKB589 旨在治疗 G/GEJ 癌、胰腺癌以及表达 CLDN18.2 的其他癌症类型。
2024年美国临床肿瘤学会胃肠道肿瘤研讨会(ASCO GI)上公布了这款国研药物的鼓舞人心的最新数据。ASKB589 联合化疗 (CAPOX) 和 PD-1 抑制剂作为局部晚期、复发和转移性胃 (G) 或胃食管连接部 (GEJ) 腺癌患者的一线治疗,疾病控制率高达100%!
截至 2023 年 12 月 20 日,共有 62 名 CLDN18.2 表达阳性的晚期胃癌患者接受了ASKB589 联合 CAPOX 和 PD-1 抑制剂治疗。
结果显示:客观缓解率(ORR)高达80%(36 名)患者达到部分缓解,肿瘤病灶显著缩小30%以上,还有2名幸运的患者肿瘤靶病灶完全消失!9 名(20.0%)患者达到疾病稳定,整体疾病控制率高达 100%,这意味着所有患者的肿瘤靶病灶都出现了不同程度的缩小或控制稳定!
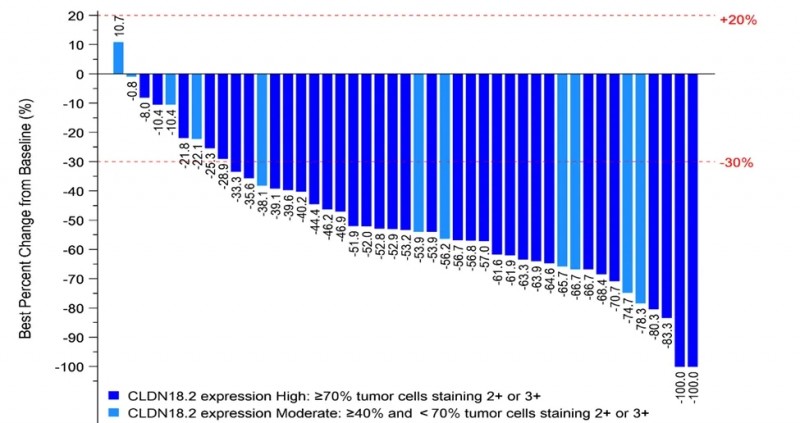
值得国内病友们振奋的是,目前这款药物临床试验仍在在中国招募患者,已有大量胃癌患者通过医学部成功入组!如想检测相关靶点或了解详情的病友可以致电医学部进行评估。
二、HER2 双特异抗体ZW25横空出世,4年随访数据亮出满分答卷
泽尼达妥单抗(zanidatamab,ZW25)是一种基于Zymeworks的Azymetric TM 平台的双特异性抗体,其可以同时结合HER2的两个非重叠表位,称为双互补位结合,可以双重阻断HER2信号,增加HER2蛋白从细胞表面的结合和去除,具有更强的抗HER2驱动肿瘤生长的作用。这样一个新型双特异性抗体,跨癌肿有效,副作用轻微,令学术界十分激动。
5月29,泽尼达妥单抗在中国获批上市,用于既往接受过全身治疗的HER2高表达(IHC3+)的不可切除局部晚期或转移性胆道癌患者。
值得胃癌病友们振奋的是,2025年ASCO年会上,这款新型药物公布了代号为ZWI-ZW25-201研究针对胃癌长达4年的随访数据,为一线治疗添了份扎实的 “定心丸”。
这项名为 ZWI-ZW25-201 的 Ⅱ 期研究,让患者在接受泽尼达妥单抗治疗的同时,联合医生选择的标准化疗方案(比如 CAPOX、FP 或 mFOLFOX6)。截至 2024 年 7 月 28 日,患者平均随访了 48 个月(也就是 4 年),数据充分证明了这款药的长期效果和安全性。
结果显示:在所有参与评估的 42 名患者中,客观缓解率(ORR)高达76% ;而经过中心实验室确认的 HER2 阳性(ccHER2+)患者(共 37 人)中,这一比例更是高达 84%。更让人放心的是,90% 的患者肿瘤都比治疗前变小了,而且起效很快,平均 1.3 个月就能看到效果。所有患者中,缓解持续时间(DOR)平均能维持 18.7 个月;ccHER2 + 患者则能维持 20.4 个月。
三、97%患者肿瘤靶病灶显著缩小或稳定!FG-M108疗效喜人
FG-M108是明济生物自主研发的靶向CLDN18.2的ADCC增强型单克隆抗体,以适中亲和力高特异性的靶向CLDN18.2阳性肿瘤细胞,并通过增强的ADCC效应等充分调动患者机体的免疫功能来杀伤肿瘤。
2024年欧洲肿瘤内科学会(ESMO)年会上,FG-M108公布了FG-M108联合卡培他滨和奥沙利铂(CAPOX)一线治疗局灶晚期不可切除或者转移性胃/胃食管交界部(G/GEJ)腺癌的最新临床试验结果,非常振奋人心!
截止至2024年7月18日,入组了52名患有HER2-/CLDN18.2+(IHC 1+/2+/3+≥10%)晚期或转移性胃癌/胃食管交界腺癌的中国受试者。
结果显示:51例疗效可评估的受试者中,36例受试者属于CLDN18.2中高表达的患者(IHC 2+/3+≥40%),客观缓解率(ORR)高达81%(cORR为78%),疾病控制率(DCR)为97%!
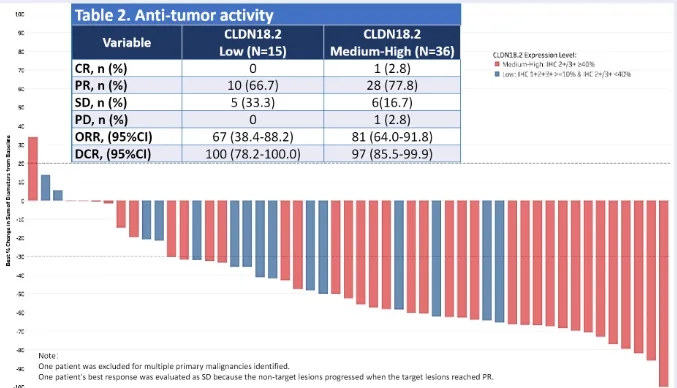
值得国内病友们振奋的是,目前这款药物临床试验仍在在中国招募患者,已有大量胃癌患者通过医学部成功入组!如想检测相关靶点或了解详情的病友可以致电医学部进行评估。
四、生存期翻倍!全球首个实体瘤 CAR-T 疗法改写晚期胃癌生存记录,上市在即
舒瑞基奥仑赛注射液是目前全球唯一一款在中国和美国获得临床试验许可(IND)的CLDN18.2 CAR-T细胞治疗,有望成为全球首创产品!
2025年ASCO盛会上,中国研究人员公布了全球首个针对实体瘤特异性靶点 Claudin18.2 的 CAR-T 细胞疗法--CT041(舒瑞基奥仑赛注射液,Satri-cel )随机对照试验的卓越数据,并发表于国际重磅期刊《柳叶刀》杂志上,引起巨大轰动!证实了 satri - cel 治疗显著延长了既往接受过治疗的 CLDN18.2 阳性胃癌或胃食管交界处癌患者的无进展生存期,并显著提高了总生存期,且安全性可控,有望改写晚期胃癌生存记录!
这项在中国24个研究中心开展的开放标签、多中心、随机对照试验 (RCT) 旨在比较 CAR-T疗法Satri-cel 与标准治疗 (SOC) 在 CLDN18.2 阳性、至少两线既往治疗失败的晚期胃食管交界处 (G/GEJC) 患者中的疗效和安全性。
当患者对传统治疗耐药后,往往陷入无药可医的绝境。2022 年 3 月 22 日至 2024 年 7 月 29 日期间,研究团队采用 2:1 随机分组,156 例 CLDN18.2 阳性、至少两线治疗失败的患者被分为 Satri-cel 治疗组(104 例)与标准治疗(TPC)组(52 例)。Satri-cel 组接受 250×10⁶个细胞输注,最多 3 次;TPC 组则由医生选择阿帕替尼、紫杉醇等常规药物治疗。值得关注的是,TPC 组患者在病情进展或不耐受时,符合条件者可交叉接受 Satri-cel 治疗,这一设计更贴近真实临床场景。
数据截止至 2024 年 10 月 18 日的分析结果堪称震撼!
生存期显著延长
无进展生存期:9.07 个月VS3.45 个月。在 ITT 人群中,独立审查委员会评估的 Satri - cel 组中位无进展生存期为 3.25 个月,TPC 组中位无进展生存期为 1.77 个月。疾病进展或死亡风险直降 63%!
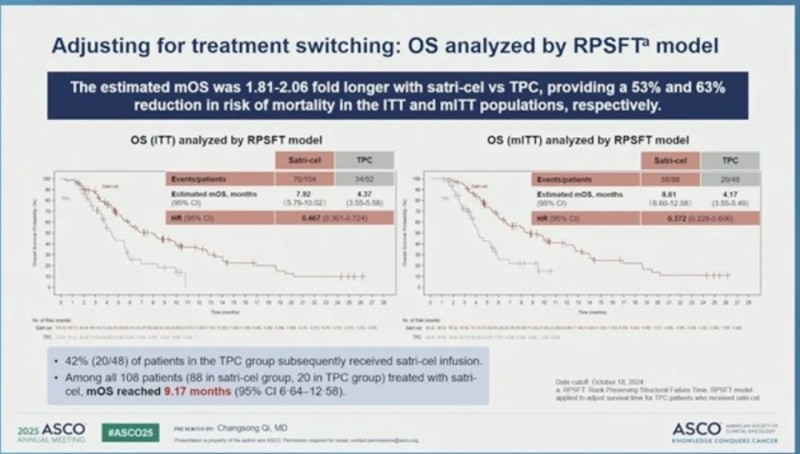
总生存期:14.42 个月VS11.33 个月。在 ITT 人群中,satri - cel 组的中位总生存期为 7.92 个月,TPC 组的中位总生存期为 5.49 个月。
更值得一提的是,汇总所有接受 Satri-cel 输注的 108 例患者,mOS 达 9.17 个月,远超 TPC(医生选择的治疗) 组未接受该治疗患者的 3.98 个月,充分证实了 Satri-cel 的卓越疗效。
22%晚期胃癌肿瘤显著缩小
经独立审查委员会评估,satri - cel 组确诊客观缓解率为 22%(104 名患者中 23 名),TPC 组为 4%(52 名患者中 2 名);satri - cel 组疾病控制率为 63%(104 名患者中 65 名),TPC 组为 25%(52 名患者中 13 名)。
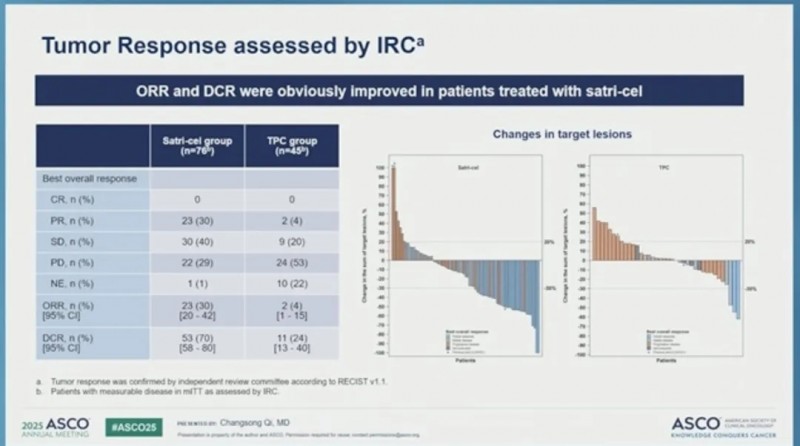
该研究的主要研究者、北京肿瘤医院沈琳教授表示:“CT041-ST-01试验是全球首个CAR-T细胞治疗实体瘤的随机对照临床研究。对于既往接受过大量治疗、治疗选择极其有限且预后不佳的晚期胃癌/胃食管交界处癌患者,satri-cel展现了突破性的疗效和显著的临床获益,包括显著提高的无进展生存期(PFS)、总生存期(OS)和肿瘤缓解率。这为那些无法通过其他疗法治愈的患者带来了新的希望。我们正在进一步探索satri-cel在辅助治疗和一线序贯治疗中的潜力,旨在更早地干预疾病进程,延长患者生存期,并最终寻求治愈方案。”
这项试验的成功,不仅为晚期 G/GEJC 癌患者点亮了生命之光,更标志着实体瘤细胞治疗时代的真正来临。随着 Satri-cel 加速迈向临床应用,我们有理由期待,未来将有更多癌症患者受益于这一创新疗法,见证生命奇迹的发生!
好消息是,近期,这款CAR-T疗法启动了针对胃癌术后的临床试验,目前招募病理结果为T4N0M0的患者,在化疗结束42天之内可接受CAR-T用于预防复发,申请额病友可以提交病历至电医学部进行评估。
五、疾病控制率86.7%!SHR-A1904初期结果公布
SHR-A1904是恒瑞医药自主研发且具有知识产权的靶向Claudin18.2的ADC,其有效载荷是拓扑异构酶抑制剂(TOPOi),通过与肿瘤细胞表面的靶抗原结合,使得药物被内吞进入细胞后释放小分子毒素杀伤肿瘤细胞。
2024ESMO大会公布了SHR-A1904治疗Claudin18.2阳性GC/GEJC患者的积极数据。
截至2024年3月18日,共有73例GC/GEJC患者入组。98.6%的患者存在远处转移,31.5%的患者接受了≥3线治疗。结果显示:在6.0mg/kg剂量组,患者的ORR和DCR分别为55.6%(5/9;95% CI,21.2-86.3)和88.9%(8/9;95% CI,51.8-99.7),在8.0mg/kg剂量组,患者的ORR和DCR分别为36.7%(11/30;95% CI,19.9-56.1)和86.7%(26/30;95% CI,69.3-96.2)。
相信上面这些在研药物给了晚期胃癌患者新的希望,同时也能看出,随着新型临床研究的推进,对检测提出了更高要求,需要全面了解患者的基因图谱 ,已经做了检测的病友可提交病历至医学部初步评估获得用药方案及临床试验推荐。相信胃癌患者的明天会越来越好。

































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城