国产mRNA癌症疫苗EVM14全球临床首例入组,控病率最高80%,更多的癌症疫苗横扫肺癌、肠癌、卵巢癌等
2025年10月14日,据“PR Newswire”报道,云顶新耀肿瘤相关抗原(TAA)癌症疫苗EVM14,在美国开展的全球多中心I期临床试验已完成首例患者入组。这是该疫苗继获美国FDA、中国NMPA新药临床试验申请(IND)批准后,取得的又一重要临床进展,更标志着我国自主研发的mRNA平台在全球临床开发中迈出关键一步。
该疫苗凭借独特作用机制,有望通过联合疗法增强疗效、延缓疾病复发,补充现有治疗方案,为患者长期无癌生存带来希望。我们期待这一创新疗法在全球多中心临床试验中充分释放治疗潜力,为全球患者增添治疗选择、改善生活质量——这不仅是国产mRNA技术的重要突破,更将为全球抗癌事业注入新动能,让更多患者看到生命延续的曙光!

▲截图源自“PR Newswire”
mRNA癌症疫苗重磅突破!国研EVM14疫苗覆盖96%肺鳞癌
EVM14是云顶新耀基于专有mRNA平台开发的即用型治疗性mRNA癌症疫苗,属无菌无防腐剂的mRNA-脂质纳米颗粒(mRNA-LNP)制剂。其核心成分为编码5种肿瘤相关抗原(TAA)的mRNA溶液,通过脂质纳米颗粒系统包裹而成。
其作用机制为:经肌肉注射后,EVM14被抗原呈递细胞(APC)摄取并翻译为靶抗原;抗原经加工后,由主要组织相容性复合体(MHC)分子呈递给T细胞,进而活化抗原特异性T细胞;活化的T细胞可迁移至肿瘤组织,识别并杀伤表达靶抗原的肿瘤细胞。
该疫苗旨在治疗鳞状细胞癌,包括鳞状非小细胞肺癌(sq-NSCLC)和头颈部鳞状细胞癌(HNSCC)。在目标癌种中,96%的sq-NSCLC患者与97%的HNSCC患者,至少表达5个靶基因中的1个,覆盖范围广泛。
临床前数据显示,EVM14与免疫检查点抑制剂(ICI,如抗PD-1或抗CTLA-4抗体)联合使用,可显著增强抗肿瘤活性、降低复发率,为联合疗法的临床探索提供支持。同时,该疫苗能诱导免疫记忆、预防肿瘤复发,为患者实现长期无癌生存带来希望。
BNT116疫苗联合Cemiplimab破解晚期非小细胞肺癌PD-1进展困局,疾病控制率高达80%
BNT116是一款研究性治疗性RNA-脂质体癌症疫苗,核心成分包含6种mRNA,每种mRNA均编码1个共同的肿瘤相关抗原。在经多线治疗的非小细胞肺癌(NSCLC)患者中,该疫苗已展现出可控的安全性;尤其当它与cemiplimab联合使用时,更能体现出治疗效果。
为进一步验证BNT116的临床价值,研究团队开展了首次人体开放标签I期LuCa-MERIT-1(NCT05142189)临床试验,旨在评估BNT116单药或联合cemiplimab用药的安全性与临床活性。该研究共纳入20例接受PD-1抑制剂治疗后疾病进展的晚期非小细胞肺癌患者,入组后统一接受BNT116+cemiplimab的联合治疗。
结果显示:在20例患者中,10%(2例)达到部分缓解(PR),70%(14例)达到疾病稳定(SD),疾病控制率(DCR)高达80%;生存指标方面,患者的中位疾病控制持续时间为6.2个月(95%Cl:4.0~未达到),中位无进展生存期(PFS)为5.5个月(95%Cl:2.9~9.5)。
▲截图源自“BMJ”
综上,本初步分析显示,BNT116+cemiplimab具有可控的安全性,并在既往接受PD-1抑制剂治疗但出现疾病进展的患者中显示出令人鼓舞的疾病控制率(DCR)和无进展生存期(PFS)。
全球首创!CIMAvax-EGF疫苗助肺癌患者活过4年,突破晚期肺癌生存期天花板
除BNT116疫苗外,古巴肺癌疫苗(CIMAvax-EGF)在肺癌治疗领域的效果同样显著。它是由人重组EGF与载体蛋白重组P64化学结合制成的治疗性癌症疫苗,靶点精准指向非小细胞肺癌(NSCLC)的关键分子——人类表皮生长因子受体(EGFR)。作为全球首个获得专利与注册的非小细胞肺癌治疗性疫苗,同时也是首个针对晚期肺癌的治疗性疫苗,目前已在古巴、秘鲁、阿根廷、哥伦比亚、波斯尼亚和黑塞哥维那、白俄罗斯等国获批临床使用。
《人类疫苗和免疫治疗》杂志曾报道过一则CIMAvax-EGF的经典治疗案例:一位IIIb/IV期非小细胞肺癌患者经该疫苗治疗后,肿瘤显著缩小,自确诊起存活时长达到48个月(4年),远超晚期肺癌患者的平均预期寿命。
该案例中的患者为54岁女性,确诊时已处于IIIb期非小细胞肺癌。就诊时,她已出现2个月的咯血加重症状,还伴随体重下降、食欲不振及骨痛。胸部CT扫描显示,其左下叶肺后基底节存在一个9cm×5.8cm×7.2cm的“大体积、分叶状、不均匀增强肿块”,左上叶另有一个较小的毛刺状病变;经活检确诊为浸润性、中度分化鳞状细胞癌。进一步检查中,CT未发现胸壁肌肉受累,骨扫描结果为阴性,最终明确诊断为T4N1M0-IIIb期非小细胞肺癌。
患者的治疗按阶段有序推进:首先接受3个疗程的紫杉醇+卡铂联合化疗,治疗后肿瘤缩小至7cm×6cm×5cm;随后转入同步放化疗阶段,方案为2个疗程顺铂联合30次60Gy放射治疗;放化疗结束2个月后,患者入组并开始接受CIMAvax-EGF疫苗治疗。
结果显示:疫苗治疗后的效果呈现出持续改善的趋势,治疗前的CT复查显示,患者左下叶病变已缩小至3cm×3cm(详见下图A),左上叶病变直径<1cm,同时存在放射治疗引发的包裹性胸腔积液;疫苗治疗3个月后,左下叶肿瘤进一步缩小至2cm×2.1cm(详见下图B);治疗6个月后,肿瘤体积降至1.5cm×2.3cm(详见下图C),较初始放化疗后的大小缩小30%,且后续趋于稳定,同期患者的胸腔积液减少、局部淋巴结缩小。
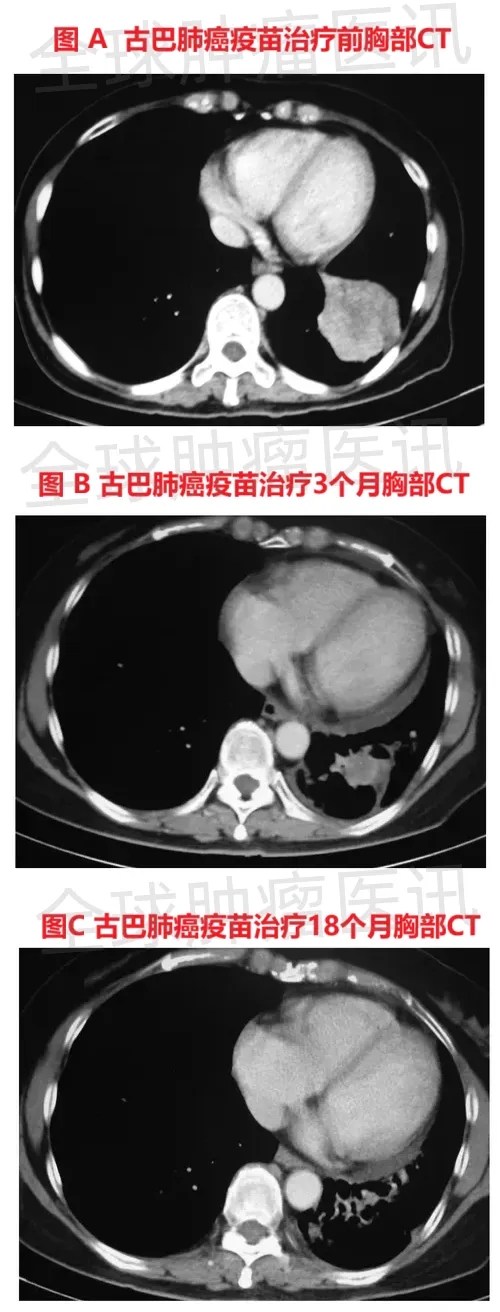
▲图源“Hum VaccImmunother”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
停止疫苗治疗3个月后(即疫苗治疗总时长18个月时),胸部CT显示肿瘤大小与6个月前相比“无明显变化”;在最后一次随访(停止疫苗注射28个月后)时,患者身体状况良好、健康状态稳定,ECOG体力状态评分始终维持在0分(代表完全正常活动,无体力限制)。
综上,这位IIIb期非小细胞肺癌患者自确诊起实现了48个月的长期生存,这对预期寿命较短的晚期肺癌患者而言极为难得。
中国患者如何寻求癌症疫苗帮助
目前,癌症疫苗中临床疗效及预防复发效果较突出的是树突状细胞疫苗、mRNA癌症疫苗、古巴肺癌疫、个性化新抗原疫苗等。
1、树突状细胞(DC)疫苗:在日本、德国等,用于临床辅助治疗多种癌症,包括皮肤癌、肝癌、肺癌、肾癌、乳腺癌等,是癌症患者的新希望!
2、mRNA癌症疫苗:正在针对肺鳞癌、肝癌、结直肠癌、黑色素瘤、食道癌、三阴性乳腺癌、头颈部肿瘤等多款恶性实体瘤,开展临床研究。
3、古巴肺癌疫苗(CIMAvax-EGF):中国患者现无需出国,可通过医学部,向古巴医疗部门申请肺癌疫苗,以延长生存期,提高生活质量!
想寻求国内外癌症疫苗或其他治疗新技术帮助的患者,可先将治疗经历、病理报告、出院小结等资料,提交到医学部,进行初步评估或了解详细的入排标准。
GVAX结肠疫苗点亮MMRp型结直肠癌治疗曙光,中位总生存达213天
错配修复缺陷型(MMRp)结直肠癌(CRC)对单药程序性细胞死亡蛋白1(PD1)抑制剂治疗无效,因此探索更有效的联合治疗方案成为临床需求。
ColonGVAX疫苗是一款同种异体、全细胞型粒细胞-巨噬细胞集落刺激因子分泌型细胞免疫疗法,可诱导针对肿瘤相关抗原的T细胞免疫。此前研究已证实,该疫苗联合低剂量环磷酰胺(Cy)能抑制调节性T细胞,为进一步联合PD1抑制剂奠定基础。近期一项单组临床研究,便聚焦评估“GVAX/Cy+PD1抑制剂帕博利珠单抗(pembrolizumab)”方案,用于治疗晚期MMR pCRC的临床疗效。该研究共纳入17例晚期转移性MMRpCRC患者,患者中位年龄为58岁,(范围:44~85岁)。
结果显示:按RECIST1.1标准,意向治疗人群的疾病控制率(DCR)为18%(17例中3例);按免疫相关疗效评价标准(irRC),DCR提升至29%(17例中5例)。其中,3例患者达到病情稳定(SD);按irRC标准,5例患者的最佳缓解为SD。另有2例对本研究治疗反应不一的患者,在后续接受其他治疗(1例用瑞戈非尼,1例用曲氟尿苷/替吡嘧啶)时,成功获得客观缓解。
在生存数据方面,患者中位无进展生存期(PFS)为82天(95%Cl:48~97天,详见下图A),中位总生存期(OS)为213天(95%Cl:179~441天,详见下图B),6个月OS率达65%(95%Cl:46%~92%)。生化缓解层面,17例患者中7例(占比41%)出现癌胚抗原(CEA)下降≥30%的生化缓解。
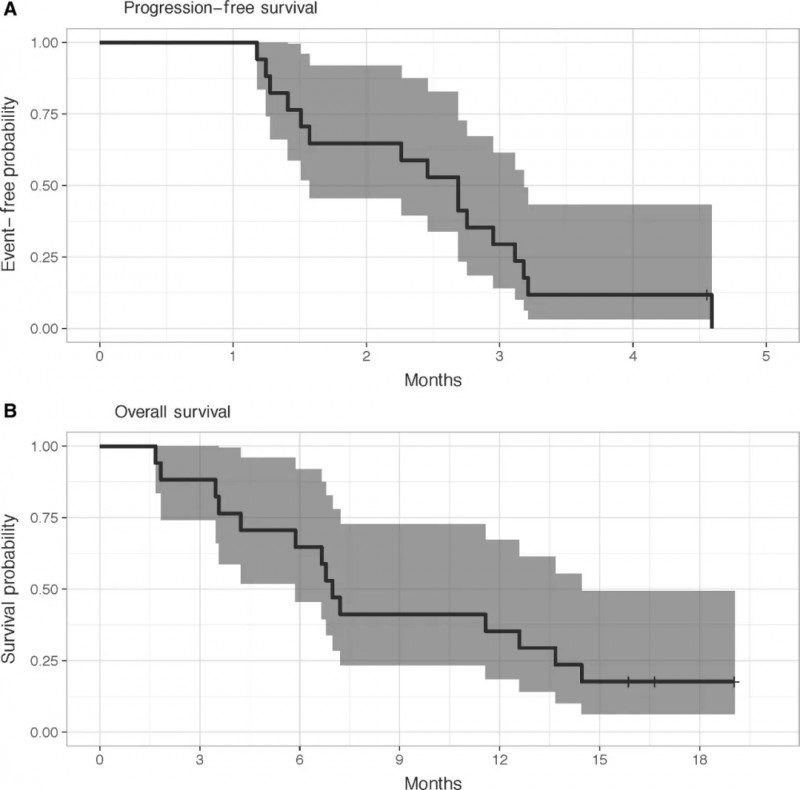
▲图源“Cancer Med”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
13线治疗后仍破局!mRNA-2416疫苗单药SD率31%,助卵巢癌患者病灶近消退
mRNA-2416是一款由脂质纳米颗粒包裹的新型信使RNA(mRNA)疗法,首次人体I/II期开放标签研究(NCT03323398)共纳入61例患者,中位年龄为65岁(年龄范围:23~82岁),涵盖卵巢癌(30%)、头颈部鳞状细胞癌(15%)、肉瘤(10%)等多个癌种。研究将患者分为两组:A组(39例)接受mRNA-2416单药重复瘤内注射,B组(22例)接受mRNA-2416联合durvalumab静脉注射。
结果显示:两组疗效与生存数据存在一定差异:A组中可评估疗效的29例患者,病情稳定(SD)率为31%;B组中可评估疗效的19例患者,11%的患者达SD,其中1例接受4.0mg剂量的卵巢癌患者还获得了部分缓解(PR)。生存指标方面,A组中位无进展生存期(PFS)为60天(95%Cl:50~108天),B组中位PFS为50天(95%Cl:38~55天)。
值得特别关注的是1例63岁浆液性输卵管/卵巢癌患者:该患者此前已接受过13线全身治疗,虽按RECIST标准其最佳疗效判定为SD,但注射病灶在4次治疗后接近消退,周围未注射的病灶在治疗第4周期也明显变平(详见下图),展现出该疗法在局部病灶控制上的潜力。
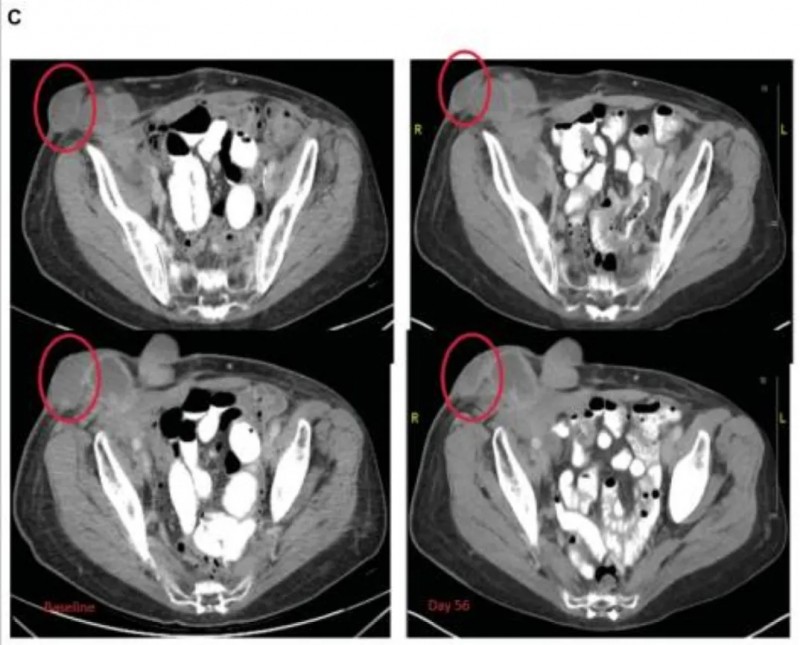
▲图源“Oncologist”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
小编寄语
近年随着多种抗癌新药、新技术(如DC细胞、mRNA癌症疫苗、CAR-T、TCR-T等)的出现,癌症逐渐进入精准治疗时代,患者的生存率也得以提高!但癌症作为一种高度突变且复杂的疾病,现阶段很难依靠单一手段达到预期效果,目前较为理想的抗癌手段是在权威医院明确诊断的基础上,应用传统治疗(手术、放化疗)+新型抗癌技术(细胞免疫疗法、癌症疫苗、营养支持等)联合应用,以巩固治疗效果、减低癌症复发/转移风险、最大限度地延长患者的生存时间!
如果您对目前的治疗不满意,或想寻求DC疫苗、LK101肝癌疫苗、古巴肺癌疫苗等新型抗癌疗法的帮助,可将近期病理检查结果、血象或影像学检查报告、治疗经历等资料,提交至医学部,进行初步评估或申请国内外抗癌专家会诊!
参考资料
[1]Atmaca A,et al.1486 Preliminary results from LuCa-MERIT-1, a phase I trial evaluating BNT116, a fixed antigen mRNA vaccine, plus cemiplimab in advanced non-small cell lung cancer after progression on PD-1 inhibition[J]. 2024.
https://jitc.bmj.com/content/12/Suppl_3/A1716
[2]]Cheng J Y,et al.CIMAvax EGF vaccine for stage IIIb/IV non-small cell lung carcinoma[J]. Human Vaccines & Immunotherapeutics, 2012, 8(12): 1799-1801.
https://www.tandfonline.com/doi/full/10.4161/hv.21744#d1e107
[3]Yarchoan M,et al.A phase 2 study of GVAX colon vaccine with cyclophosphamide and pembrolizumab in patients with mismatch repair proficient advanced colorectal cancer. Cancer Med. 2020 Feb;9(4):1485-1494.
https://onlinelibrary.wiley.com/doi/10.1002/cam4.2763
[4]Sullivan RJ,et al.First-in-human phase I/II, open-label study of mRNA-2416 alone or combined with durvalumab in patients with advanced solid tumors and ovarian cancer. Oncologist. 2025 Jun 4;30(6):oyaf115.
https://pmc.ncbi.nlm.nih.gov/articles/PMC12166121/
[5]https://www.prnewswire.com/apac/news-releases/everest-medicines-announces-first-patient-enrolled-in-a-global-multi-center-phase-i-clinical-trial-of-tumor-associated-antigen-cancer-vaccine-evm14-302582820.html

































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城