2025年11月6日NCCN指南更新,德达博妥单抗(Dato-DXd、Datroway、Datopotamab deruxtecan,DS-1062a)成EGFR耐药肺癌二线首选,控病率逼近80%
2025年11月6日,美国国家综合癌症网络(NCCN)发布《非小细胞肺癌(NSCLC)临床实践指南》1.2026版。相比8.2025版,新版指南的核心更新为:经FDA加速批准的德达博妥单抗(Dato-DXd,商品名Datroway®),被列为EGFR突变型NSCLC患者一线治疗进展后的首选治疗方案,这为EGFR耐药患者开辟了更精准的治疗新路径,点亮了持续生存的新曙光!
▲截图源自“OncLive”
靶向Trop-2再添猛将!德达博妥单抗上市申请获CDE受理,HR+/HER2-乳腺癌患者迎新选择
德达博妥单抗(Dato-DXd,通用名datopotamabderuxtecan,商品名Datroway,代号DS-1062a)是第一三共和阿斯利康联合开发的靶向Trop-2(滋养层细胞表面抗原-2)的DXd抗体偶联药物(ADC),其有效载荷为高效拓扑异构酶I抑制剂。
2024年3月16日,该药用于成人既往接受过系统治疗的HR阳性、HER2阴性不可切除或转移性乳腺癌治疗的上市申请,获中国国家药品监督管理局药品审评中心(CDE)受理,最快或将于2025年第三季度(Q3)获批。
Dato-DXd双线研究发力,晚期非小细胞肺癌疾病控制率高达78.8%,中位总生存13.6个月
德达博妥单抗(Dato-DXd)的相关批准基于TROPION-Lung05(NCT04484142)II期研究与TROPION-Lung01(NCT04656652)III期研究的汇总数据。
其中,TROPION-Lung05 II期研究(NCT04484142)针对一线靶向治疗和铂类化疗进展后、存在可靶向基因组改变的晚期/转移性非小细胞肺癌(NSCLC)患者,评估了Dato-DXd的安全性与疗效,以填补此类患者未满足的治疗需求。
该研究共入组137例接受Dato-DXd治疗的患者,中位研究持续时间15.2个月,中位治疗持续时间4.4个月,患者中位年龄为61岁(范围:29-79岁)。其中56.9%存在EGFR突变(49.6%为19号外显子缺失、L858R突变和/或T790M突变),24.8%存在ALK重排,71.5%既往接受过至少三线晚期/转移性疾病治疗。
结果显示:总体确认客观缓解率(ORR)为35.8%(95%CI:27.8%-44.4%),含4例完全缓解(CR,2.9%)和45例部分缓解(PR,32.8%,图2),涵盖多种突变类型;其中EGFR突变患者ORR达43.6%(95%CI:32.4%-55.3%),ALK重排患者ORR为23.5%(95%CI:10.7%-41.2%)。中位缓解持续时间(DOR)为7.0个月(95%CI:4.2-9.8个月),疾病控制率(DCR)达78.8%(95%CI:71.0%-85.3%)。
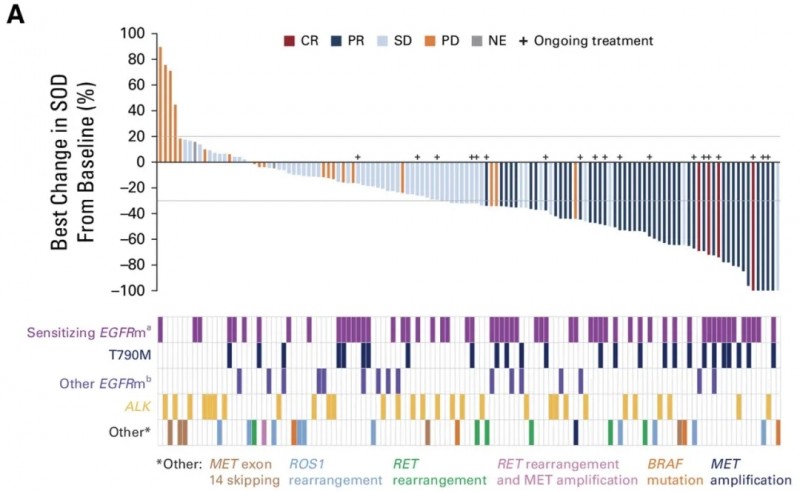
▲图源“JCO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
中位无进展生存期(PFS)为5.4个月(95%CI:4.7-7.0个月,详见下图A),中位总生存期(OS)为13.6个月(95%CI:9.9个月-无法评估,详见下图B)。
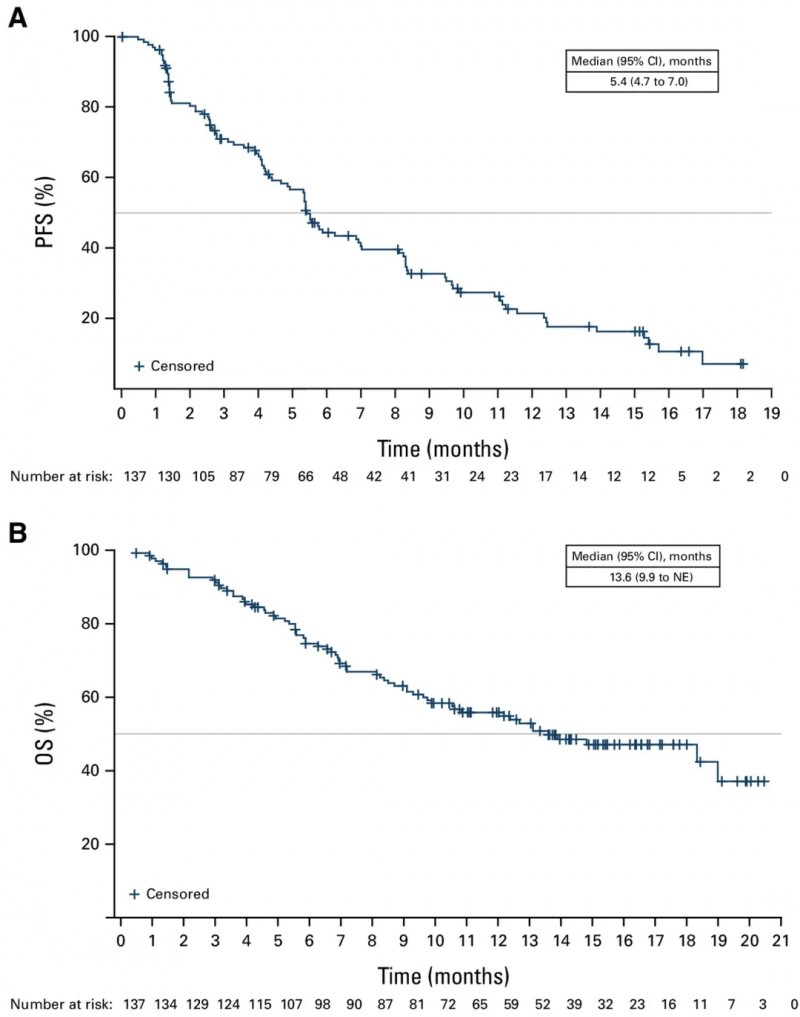
▲图源“JCO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
此外,TROPION-Lung01 III期研究显示,Dato-DXd组中位总生存期(OS)12.9个月(95%CI:11.0-13.9个月)vs多西他赛组11.8个月(95%CI:10.1-12.8个月),中位无进展生存期(PFS)4.4个月(95%CI:4.2-5.6个月)vs多西他赛组3.7个月(95%CI:2.9-4.2个月)。
综上,在既往经多线治疗且存在可靶向基因组改变的晚期/转移性NSCLC患者中,Dato-DXd展现出令人鼓舞且持久的抗肿瘤活性。
多款肺癌新药上市在即,国内多中心招募进行中……
相信看了上面的数据,肺癌或其他实体瘤患者一定燃起了新的希望!好消息是,目前我国有多款在研的抗癌新药,正在开展临床研究,现已有大量患者通过抗癌新药招募中心,成功入组接受抗癌新药的治疗!
【JYP0322】
1、药品名称:JYP0322(ROS1抑制剂)。
2、临床分期:Ⅲ期。
3、治疗线数:标准治疗失败。
4、突变基因:ROS1。
5、适合人群:ROS1阳性局部晚期或转移性非小细胞肺癌。
【Vx-001疫苗】
1、药品名称:Vx-001注射液(mRNA癌症疫苗)。
2、临床分期:Ⅰ期。
3、治疗线数:标准治疗失败。
4、突变基因:无靶点要求。
5、适合人群:晚期实体瘤/非小细胞肺癌,HLA-A*0201型(多肽呈递的基序仅与该HLA分子匹配)、TERT表达阳性且肿瘤浸润淋巴细胞(CD3/CD8 TILs)表达为阴性。
【JWTCR001】
1、药品名称:JWTCR001(TCR-T疗法)。
2、临床分期:Ⅰ期、Ⅱ期。
3、治疗线数:标准治疗失败。
4、适合人群:经治失败的鳞状非小细胞肺癌、食管鳞癌(含胃-食管交界部鳞癌)、滑膜肉瘤、卵巢癌等。
申请流程
想申请抗癌新药临床试验的患者,需将近期病理报告、基因检测报告等资料汇总后,提交至医学部,进行初步评估。
我们的专家将为您全面分析解读检测报告,预计一个工作日内电话联系推荐用药方案,并匹配适合患者入组的临床试验项目。注:作为国内权威的肿瘤患者服务平台,我们承诺对所有受试者的个人信息保密,并保证在整个过程中,遵循国家临床研究相关的法律法规。
小编寄语
近年来,肺癌的治疗已经取得了长足的进展,逆转了晚期患者的生存期,除了上面整理的内容,还有更多的新药正在研发中。如果您对现有治疗方案不满意,或想了解肺癌更多抗癌新药/新技术的更多讯息,可将治疗经历、近期病理检查报告、出院小结等,提交至医学部,进行初步评估。
参考资料
[1]Sands J,et al.Datopotamab deruxtecan in advanced or metastatic non–small cell lung cancer with actionable genomic alterations: results from the phase II TROPION-Lung05 study[J]. Journal of Clinical Oncology, 2025, 43(10): 1254-1265.
https://ascopubs.org/doi/10.1200/JCO-24-01349
[2]https://www.onclive.com/view/nccn-releases-nsclc-guideline-update-dato-dxd-designated-as-a-preferred-second-line-regimen-in-egfr-mutated-disease

































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城