HBV-mRNA疫苗WGc-0201注射液新药IND在华获批,更多的癌症疫苗惠及肺癌/胃癌/肝癌等五大癌种
“有没有一种治疗方法,不用承受化疗放疗的痛苦,只需打几针疫苗,既能精准控制癌症,又不会对正常身体组织造成重创?”这不仅是无数癌症患者最迫切的期盼,更是所有关注生命健康、期盼癌症治疗突破的人共同的心声。如今,这份曾遥不可及的期待正一步步照进现实——癌症疫苗横空出世,为深陷绝境的癌症患者点亮了重生的希望。
就在2025年11月18日,中国国家药监局药品审评中心(CDE)官网传来重磅消息:威斯津生物自主研发的1类新药WGc-0201注射液正式获批临床,拟用于治疗乙型肝炎病毒(HBV)阳性肝细胞癌。更值得关注的是,这款mRNA肿瘤治疗疫苗已于今年10月斩获美国FDA的IND批准,实现中美双轨临床推进的关键突破!癌症疫苗走向临床普及的脚步,正离我们越来越近!
▲截图源自“NMPA”
WGc-0201疫苗重锤晚期乙型肝炎相关肝细胞癌,首次人体试验实现70%疾病控制率
晚期乙型肝炎相关肝细胞癌(HCC)存在巨大未满足医疗需求,而mRNA疫苗已成为极具前景的癌症免疫治疗平台。
WGc-0201是一款新型mRNA治疗性疫苗,以编码乙型肝炎病毒(HBV)相关HCC抗原的mRNA为骨架,采用脂质纳米颗粒(LNP)递送技术。其首次人体临床试验(NCT05738447)共纳入12例HCC患者,均接受多次肌注给药。
试验结果显示,10例患者可评估疗效,疾病控制率(DCR)达70%;所有剂量组中位无进展生存期(PFS)为2.6个月(95%CI:0.70-4.53)。此外,IFN-γELISPOT分析证实疫苗可诱导抗原特异性T细胞反应,彰显出强大的免疫原性。
▲截图源自“ESMO”
综上,该首次人体试验表明,mRNA治疗性疫苗WGc-0201在晚期HBV相关HCC患者中,具备良好的安全性、强大的免疫原性及令人鼓舞的抗肿瘤活性。这些积极结果不仅验证了WGc-0201的治疗潜力,更为后续深入研究奠定了坚实基础。
2025癌症患者必须知道的九大癌症治疗性疫苗,覆盖五大高发癌种
尽管多款癌症疫苗仍处于研发阶段,但全球范围内已有包括古巴肺癌疫苗在内的多款癌症疫苗相继获批。更振奋的是,截至2025年11月,多项癌症疫苗临床试验已取得重要进展,覆盖肺癌、肝癌、胰腺癌、黑色素瘤、胃癌等多种难治性癌种。
【一】肺癌疫苗
BI1361849-mRNA疫苗:近半数非小细胞肺癌患者病情稳定,中位总生存超1年
BI1361849(CV9202)是一款活性癌症免疫治疗药物,由鱼精蛋白配制的序列优化mRNA构成,可编码6种非小细胞肺癌相关抗原(包括MUC-1、MAGE-C1、MAGE-C2、NY-ESO-1、5T4、survivin),旨在诱导靶向免疫反应。其联合局部放疗治疗非小细胞肺癌的Ib期临床试验(NCT01915524)疗效喜人。
结果显示:46.2%(12/26)的患者达到病情稳定(SD);截至末次随访,1例患者已确认达到部分缓解(PR),肿瘤缩小具备可测量性;6例未接受放射治疗的入组患者,病变缩小超15%。此外,入组患者的中位无进展生存期(PFS)达2.87个月,自首次BI1361849治疗起的中位总生存期(OS)为13.95个月。
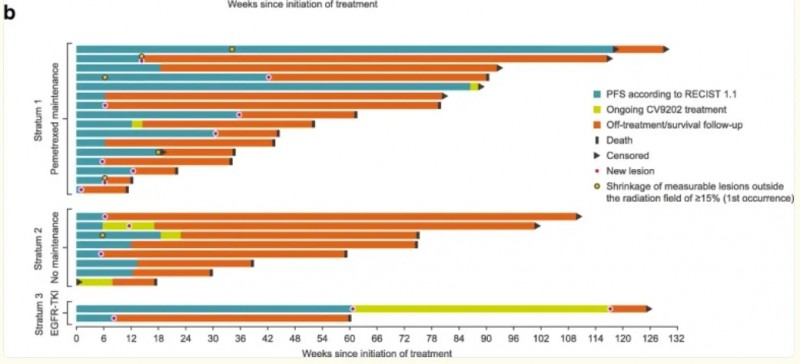
▲图源“J Immunother Cancer”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
Cimavax-EGF疫苗:靠“断养料” 饿死肺癌细胞,5年生存率提高23%,一例 存活5年无复发
大名鼎鼎的古巴肺癌疫苗(CIMAvax-EGF),是一款针对晚期肺癌(尤其非小细胞肺癌)的治疗性疫苗。其抗癌原理是通过阻断癌细胞生长必需的养料——表皮生长因子(EGF),进而将癌细胞“活活饿死”。
其Ⅲ期临床研究纳入405例一线化疗后的晚期非小细胞肺癌(NSCLC)患者,随机分为两组:对照组接受支持性治疗,疫苗接种组接受CIMAvax-EGF接种。结果显示,疫苗接种组中位总生存期(OS)达12.43个月,显著优于对照组的9.43个月;长期生存率同样亮眼,2年生存率为37%vs对照组20%,5年生存率更是达到23%,而对照组为0%。

加拿大广播公司(CBC)也曾报道过一则振奋人心的案例:68岁的终生吸烟者M先生,5年前确诊晚期非小细胞肺癌时已接受多次放化疗,但医生坦言,癌症一旦复发便无计可施,当时预估他的生存期不足一年。不愿放弃的M先生,于2011年抱着最后一丝希望远赴古巴,接受了CIMAvax-EGF疫苗治疗。
令所有人意外的是,治疗后M先生的病情迎来“奇迹般”缓解:连续治疗3个月,症状显著减轻,癌细胞得到有效控制。此后他每月定期接种以维持生活质量,如今5年多过去,肺癌始终未复发,这样的结果连主治医生都直呼“不可思议”。这位医生坦言:“我见过不少患者对化疗有短期反应,但几乎都会快速复发,像这样存活五年的情况,实在太罕见了。”
【二】肝癌疫苗
LK101注射液:我国首个个性化mRNA编辑疫苗,肝癌复发率直降一半
LK101注射液是一款通过编码肿瘤新生抗原的mRNA体外转染树突细胞(DC)制备的疫苗,兼具mRNA疫苗和DC疫苗的优势,能为患者带来长期抗癌效应,且具有耐受性好、安全性高的特点。
2023年3月15日,LK101注射液的新药临床试验申请(IND)获国家药品监督管理局药品审评中心(CDE)批准(受理号:CXSL2200612),用于治疗晚期实体瘤。它不仅是国内首个获批进入临床阶段的个性化肿瘤新生抗原疫苗,也是首个获批临床的完全个性化mRNA编辑产品。
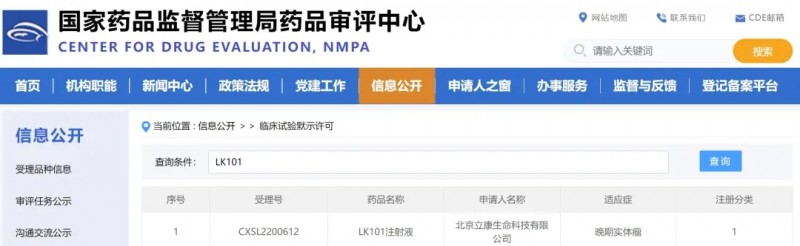
LK101注射液治疗肝细胞癌的首次人体临床研究(NCT03674073)数据,在2024年ASCO大会上公布,其中复发率数据对比尤为显著:疫苗接种组1年复发率18.2%、2年复发率36.4%,对照组则分别为33.3%和51.4%;两组中位随访时间分别为48.4个月和38.8个月,消融对照组有3名患者死亡,而所有接种疫苗的12名患者均存活,意味着他们的生存期已长达4年以上!
除肝细胞癌外,LK101注射液在肺癌治疗领域的探索也已启动。近日,评估LK101注射液用于晚期肺癌患者有效性和安全性的随机、开放、多队列Ⅱ期临床试验启动会在北京成功召开,标志着我国在肿瘤个体化免疫治疗领域迈出重要一步。
中国患者如何寻求癌症疫苗帮助
目前,癌症疫苗中临床疗效及预防复发效果较突出的是树突状细胞疫苗、mRNA癌症疫苗、古巴肺癌疫、个性化新抗原疫苗等。
1、树突状细胞(DC)疫苗:在日本、德国等,用于临床辅助治疗多种癌症,包括皮肤癌、肝癌、肺癌、肾癌、乳腺癌等,是癌症患者的新希望!
2、mRNA癌症疫苗:正在针对肺鳞癌、肝癌、结直肠癌、黑色素瘤、食道癌、三阴性乳腺癌、头颈部肿瘤等多款恶性实体瘤,开展临床研究。
3、古巴肺癌疫苗(CIMAvax-EGF):好消息是,中国患者现无需出国,可通过医学部,向古巴医疗部门申请肺癌疫苗,以延长生存期,提高生活质量!
想寻求国内外癌症疫苗或其他治疗新技术帮助的患者,可先将治疗经历、病理报告、出院小结等资料,提交到医学部,进行初步评估或了解详细的入排标准。
【三】胰腺癌疫苗
BNT122:胰腺癌中位无复发生存超1年
BNT122(自体cevumeran、RO7198457)是一款个体化新抗原mRNA疫苗,可编码20余种特异性新抗原,用于治疗胰腺导管腺癌(PDAC),旨在降低疾病复发风险、延长患者生存期。
Ⅰ期临床研究数据显示:接种疫苗但未诱导出疫苗特异性T细胞的患者,中位无复发生存期(RFS)仍长达13.4个月。
值得关注的是,其中29号患者的血清CA19-9水平升高,且出现7mm的新发肝脏病变,但该病灶在后续影像学检查中完全消失(下图为该患者接种BNT122疫苗前后的腹部MRI对比)。这表明,BNT122疫苗可能具备清除肿瘤微转移的潜在能力。
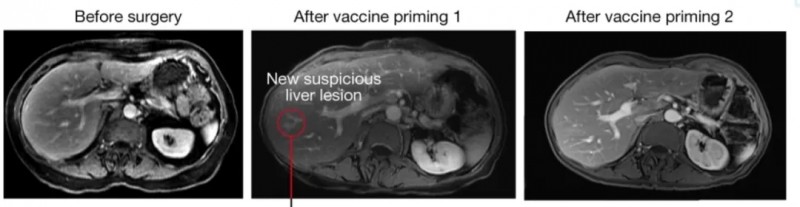
▲图源“nature”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
WT1-DC疫苗:胰腺癌中位总生存超3.5年
新型WT1肽脉冲树突状细胞(WT1-DC)疫苗,主要适用于胰腺导管腺癌(PDAC)患者。《癌症免疫治疗杂志》报道的一项研究共纳入10例不可切除PDAC患者,入组后接受白蛋白结合型紫杉醇联合吉西他滨治疗,同时联合WT1-DC疫苗回输。
结果显示,9例可评估患者的中位无进展生存期(PFS)达2.23年,中位总生存期(OS)达3.52年。经CE-CT评估,所有患者肿瘤负荷均有所下降,降幅介于0.0%~57.4%之间;其中7例(6例局部晚期、1例转移性)达到部分缓解(PR),3例实现病情长期稳定。
值得一提的是,4例接受R0切除的局部晚期患者中,3例持续呈WT1-DTH阳性,且自治疗启动后均存活超4.5年。下图为1例代表性PDAC患者接受WT1-DC疫苗治疗前后的影像对比。
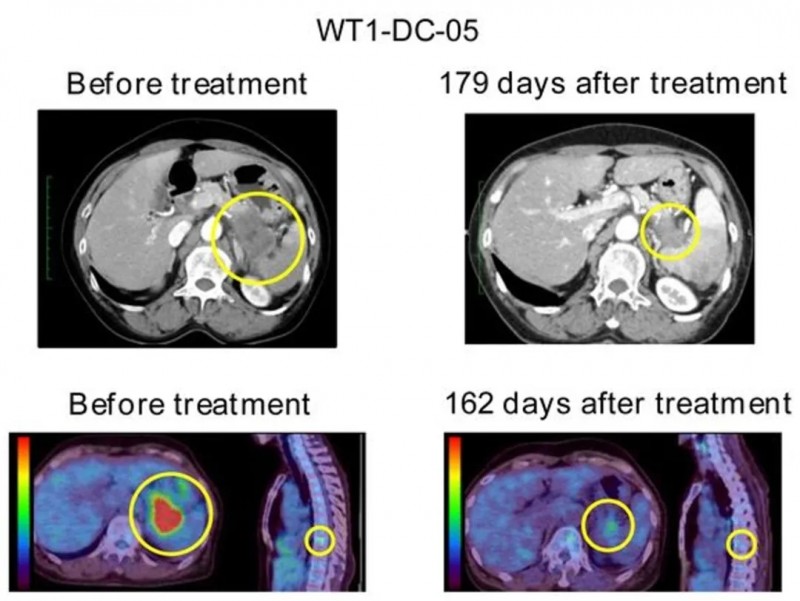
▲图源“J Immunother Cancer”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
ELI-002疫苗:KRAS阳性胰腺癌完全缓解率达24%
ELI-002是一款美国研发的KRAS阳性实体瘤治疗性疫苗,精准靶向结直肠癌(突变率52%)与胰腺导管腺癌(突变率93%)两大癌种。其核心成分AMP-mKRAS-肽宛如“信号塔”,可引导免疫系统精准识别并歼灭携带KRAS突变的癌细胞,为这两类难治性肿瘤提供了全新治疗方向。
《Nature》近期公布了ELI-002的1期AMPLIFY-201临床研究(NCT05726864)成果,2年随访数据表现惊艳。结果显示:25例入组患者的中位无复发生存期(RFS)与总生存期(OS)均达16.33个月(详见下图);此外,治疗6个月时,77%(n=23)的患者肿瘤标志物水平下降,其中6例(24%)达到完全缓解(CR),癌细胞近乎被清除。
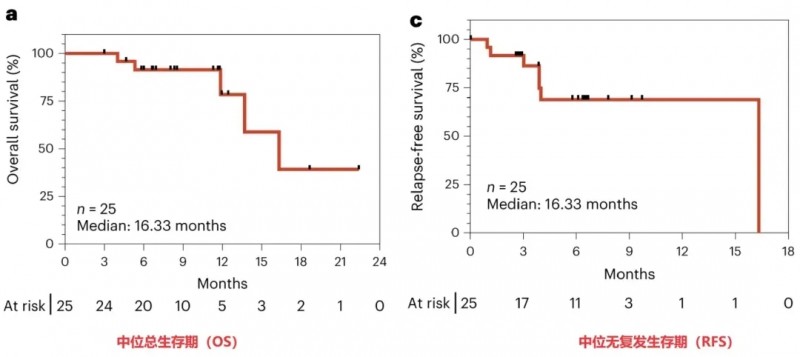
▲图源“nature medicine”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
【四】胃癌疫苗
Neo-MoDC疫苗:首个胃癌治疗里程碑,患者肿瘤消失并持续缓解25个月
Neo-MoDC疫苗是我国自主研发的载有新抗原的单核细胞衍生树突状细胞(DC)疫苗,核心机制是充分激活机体免疫系统、促进T细胞富集,进而调动T细胞对全身癌细胞发起强效攻击。
2022年,《Nature》子刊报道了一则重磅临床案例:一名晚期胃癌患者经Neo-MoDC疫苗联合PD-1疗法治疗后,实现完全且持久的缓解。这也是全球首个新抗原DC疫苗联合PD-1疗法达成晚期胃癌完全持久缓解的案例,标志着DC疫苗治疗领域的重大突破。
该患者确诊为IV期(BormannIII型)转移性胃癌,此前虽接受过D2根治性远端胃切除术及FOLFOX方案治疗,但仍发生腹膜与淋巴结转移。临床已无合适治疗方案时,患者入组接受Neo-MoDC疫苗联合免疫检查点抑制剂(PD-1)治疗。
结果令人振奋:联合治疗后,患者肿瘤迅速缩小,最终病灶完全消失,且这一缓解状态已持续长达25个月,下图展示了该患者在治疗前、治疗期间目标肿瘤病变的代表性图像(详见下图)。
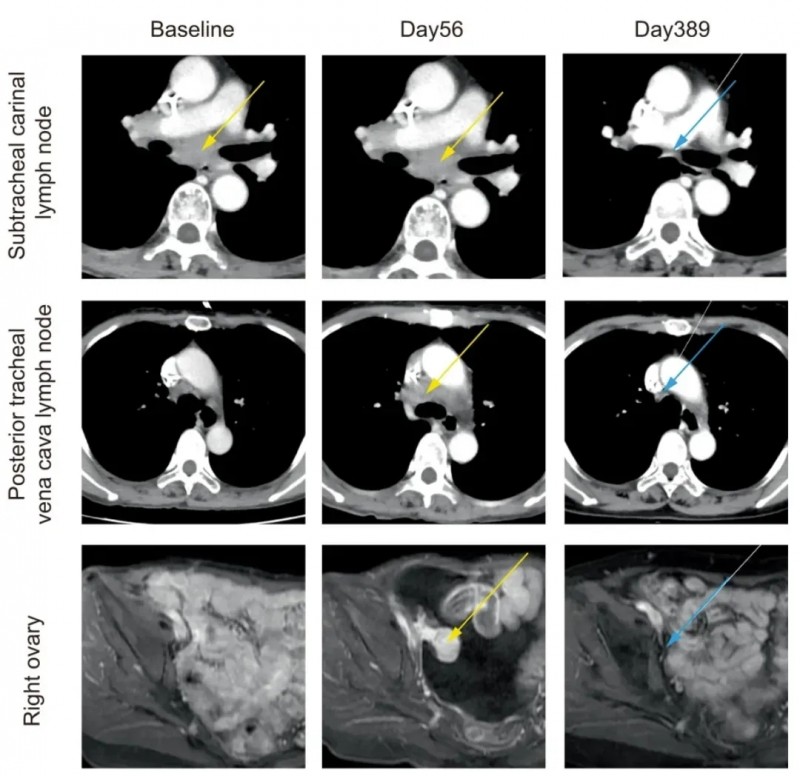
▲图源“npj”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
【五】黑色素瘤疫苗
mRNA-4157:黑色素瘤远处转移/死亡风险降62%
mRNA-4157(V940)是新型mRNA个体化新抗原疗法(INT),依据患者肿瘤DNA独特突变特征设计生产,含编码34种新抗原的合成mRNA。注射后可诱导特异性T细胞反应,训练并激活抗肿瘤免疫,识别攻击特定癌细胞,实现黑色素瘤防治目标,已获美国FDA“突破性疗法认定”。
IIb期临床试验显示:其与派姆单抗联用,可使高危III/IV期黑色素瘤患者远处转移或死亡风险降低62%、复发或死亡风险降低49%,显著延长生存期。与派姆单抗单药组相比,联合组无复发生存期(RFS)、无远处转移生存期(DMFS)明显延长:18个月RFS率单药组62.2%vs联合组78.6%,18个月DMFS率单药组76.8%vs联合组91.8%。
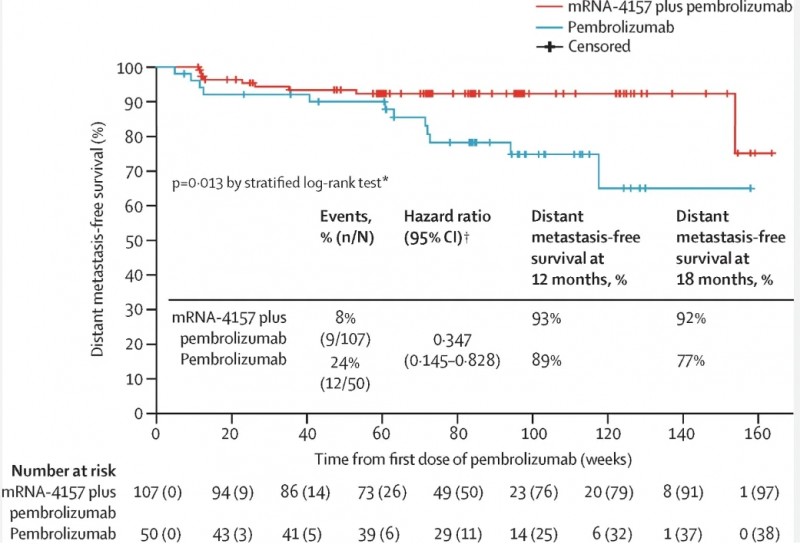
▲图源“Lancet”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
据BBC报道,52岁的史蒂夫・杨(SteveYoung)作为首批报名参加临床试验的患者之一,已完成了该疫苗接种。
他于去年8月确诊II期黑色素瘤并手术切除,作为首批受试者已完成接种,他表示:“虽然做了手术,但可能有未发现的癌细胞,能参与临床试验很幸运——这让我不是坐以待毙,而是主动对抗潜在敌人,也是阻止癌症复发的最佳机会。”
▲图源“BBC”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
IO102-IO103:首款针对IDO和PD-L1的免疫调节疫苗,近半数黑色素瘤患者完全缓解
PD-1抑制剂是治疗转移性黑色素瘤(MM)的有效手段,但超过50%的患者会因耐药出现病情进展。而IO102-IO103是首创针对IDO和PD-L1的双靶点免疫调节疫苗,由IO102和IO103两种疫苗组成,均可激发并训练患者体内特定T细胞:IO102诱导免疫细胞攻击细胞内的吲哚胺-2,3-双加氧酶(IDO,酶);IO103诱导免疫细胞攻击细胞膜上的程序性死亡配体1(PD-L1,蛋白质),助力免疫细胞识别并“记住”特定癌细胞,最终清除肿瘤微环境中的肿瘤细胞与免疫抑制细胞。
1/2期临床试验(NCT03047928)数据显示:客观缓解率(ORR)高达80%(95%CI:62.7%~90.5%),其中43%的患者达到完全缓解(CR),37%达到部分缓解(PR);中位无进展生存期(PFS)长达26个月(95%CI:15.4~69个月)。
下图为患者MM42接受IO102-IO103疫苗治疗前、治疗后(回输9次)的PET-CT图像,呈现靶病变的FDG代谢变化。
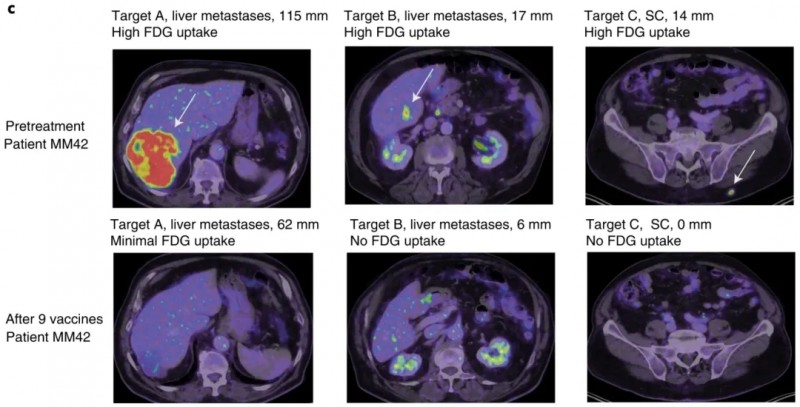
▲图源“Nat Med”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
小编寄语
作为新型抗癌疗法的代表,癌症疫苗历经数十载发展,已从早期基础研究逐步迈向临床试验阶段,更已有古巴肺癌疫苗等正式获批产品问世——其将患者5年生存率从0提升至23%,尽显临床价值。而我国在癌症疫苗领域同样成果频出,多款候选疫苗处于火热研发阶段。以针对肝细胞癌的LK101为例,其首次人体临床研究(NCT03674073)中,12名入组患者生存期均超过4年!种种进展无不表明,癌症疫苗已离我们越来越近,“打一针唤醒免疫系统,重新识别并杀伤癌细胞”的设想,或将很快从愿景变为现实,而非遥不可及的天方夜谭!
更振奋人心的是,我国目前已有多款癌症疫苗临床试验陆续开展,且正式启动患者招募。有意向参与的癌友,可将治疗经历、近期病理检查结果等,提交至医学部,了解详细入排标准并进行初步评估。
参考资料
[1]Liu J, Zhu Y,et al. 1504P An exploratory study on the mRNA WGc-0201 vaccine against advanced hepatitis B related hepatocellular carcinoma in a prospective open-label and first-in-human clinical trial[J]. Annals of Oncology, 2025, 36: S902.
https://www.annalsofoncology.org/article/S0923-7534(25)03054-6/fulltext
[2]Papachristofilou A,et al.Phase Ib evaluation of a self-adjuvanted protamine formulated mRNA-based active cancer immunotherapy, BI1361849 (CV9202), combined with local radiation treatment in patients with stage IV non-small cell lung cancer. J Immunother Cancer. 2019 Feb 8;7(1):38.
https://pmc.ncbi.nlm.nih.gov/articles/PMC6368815/
[3]Rojas L A,et al.Personalized RNA neoantigen vaccines stimulate T cells in pancreatic cancer[J].Nature,2023,618(7963):144-150.
https://www.nature.com/articles/s41586-023-06063-y
[4]Koido S,et al.Dendritic cells pulsed with multifunctional Wilms' tumor 1 (WT1) peptides combined with multiagent chemotherapy modulate the tumor microenvironment and enable conversion surgery in pancreatic cancer. J Immunother Cancer. 2024 Oct 8;12(10):e009765.
https://jitc.bmj.com/content/12/10/e009765.long
[5]Pant S,et al.Lymph-node-targeted, mKRAS-specific amphiphile vaccine in pancr%eatic and colorectal cancer: the phase 1 AMPLIFY-201 trial[J].Nature medicine,2024:1-12.
https://www.nature.com/articles/s41591-023-02760-3
[6]Guo Z,et al.Durable complete response to neoantigen-loaded dendritic-cell vaccine following anti-PD-1 therapy in metastatic gastric cancer.NPJ Precis Oncol.2022 Jun 3;6(1):34.
https://www.nature.com/articles/s41698-022-00279-3
[7]Weber J S,et al.Individualised neoantigen therapy mRNA-4157 (V940) plus pembrolizumab versus pembrolizumab monotherapy in resected melanoma (KEYNOTE-942): a randomised, phase 2b study[J]. The Lancet, 2024, 403(10427): 632-644.
https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(23)02268-7/abstract
[8]Kjeldsen JW,et al.A phase 1/2 trial of an immune-modulatory vaccine against IDO/PD-L1 in combination with nivolumab in metastatic melanoma. Nat Med. 2021 Dec;27(12):2212-2223. doi: 10.1038/s41591-021-01544-x. Epub 2021 Dec 9. Erratum in: Nat Med. 2022 Apr;28(4):871.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8904254/

































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城