靶向CLDN18.2/4-1BB的双特异性抗体药物Givastomig首次人体研究结果公布
“化疗耐药、免疫无效,难道真的没救了?”这是无数晚期胃食管癌患者的绝望呐喊。作为我国高发的恶性肿瘤,胃食管癌(GEC)晚期患者的治疗选择极为有限,既往疗法疗效不佳且副作用明显,临床上迫切需要有效的治疗方案。
近日传来喜讯,我国自主研发的CLDN18.2/4-1BB双特异性抗体Givastomig的首次人体研究结果公布,为这类患者带来了全新曙光。这款具备“肿瘤局部条件性免疫激活”特性的国研新药,在临床研究中展现出可控的安全性和明确的抗肿瘤活性,更有望破解传统免疫疗法“系统性激活导致毒副作用大”的痛点,为实体瘤精准治疗开辟新路径。

首次人体研究数据亮眼:安全性可控,16%患者肿瘤缩小
Givastomig的惊艳之处,在于其独特的“双靶点设计”和“条件性激活”机制,彻底颠覆了传统免疫疗法的作用逻辑。作为我国自主研发的新一代双特异性抗体,它一端精准靶向肿瘤细胞表面的CLDN18.2抗原,另一端则瞄准免疫T细胞表面的4-1BB分子,形成“肿瘤细胞-抗体-T细胞”的三元复合物,实现“精准识别+局部激活”的双重效果。
CLDN18.2是一种紧密连接蛋白,在胃癌、胃食管癌、胰腺癌等多种实体瘤中高特异性表达,而在正常组织中几乎不暴露,是理想的肿瘤靶向靶点。4-1BB则是T细胞激活的关键共刺激分子,激活后能显著增强T细胞的杀伤活性和存活时间。但传统4-1BB激动剂容易系统性激活全身T细胞,导致严重的免疫相关不良反应,限制了其临床应用。
Givastomig完美解决了这一难题:它只有在同时结合肿瘤细胞上的CLDN18.2和T细胞上的4-1BB时,才会激活T细胞。这种“条件性激活”模式,能让免疫反应精准局限在肿瘤微环境内,在高效杀伤癌细胞的同时,最大程度避免对正常组织的损伤,显著降低系统性副作用风险,这也是其相较于传统免疫疗法和单一靶点药物的核心优势。
近日公布的Givastomig首次人体研究结果,全面验证了这款国研双抗的安全性和抗肿瘤活性。这项研究共纳入75例晚期实体瘤患者,涵盖剂量递增和剂量扩展两个阶段,重点评估了不同剂量Givastomig单药治疗的效果。
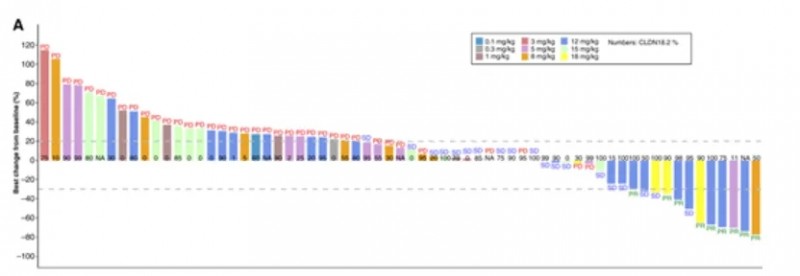
在抗肿瘤活性方面,针对CLDN18.2阳性的胃食管癌患者,当剂量超过5 mg/kg时,客观缓解率(ORR)达到16%(N=43),意味着近五分之一的患者用药后肿瘤显著缩小。值得注意的是,缓解患者的CLDN18.2表达范围广泛,从11%到100%均有获益,这表明即使是CLDN18.2低表达的患者,也可能从Givastomig治疗中获益,极大拓宽了潜在受益人群。
胃癌患者一定要检测的新兴靶点--Claudin18.2
Claudin 18.2是一个泛肿瘤的靶点,在多种上皮肿瘤当中都有表达,尤其在胃癌和胰腺癌中存在较高的表达。在胃癌或胃食管结合部癌中,高达60%的患者检测到Claudin 18.2的高度表达,成为近两年最具潜力的热门靶点,已有大量药物取得卓越的临床数据,为胃癌患者带来新曙光!
2024年6月25日,FDA批准zolbetuximab上市,联合含氟嘧啶和铂类化疗用于一线治疗治疗 CLDN18.2 阳性、不可切除、晚期或复发性胃癌或胃食管交界腺癌患者。这是第一个也是唯一一个靶向治疗患有CLDN18.2 阳性这种毁灭性疾病的新选择!

除了上面获批的药物,还有更多的新药正在研发中,包括ADC药物、MET抑制剂、PD-1/PD-L1抑制剂等等,大家可以根据当前疾病的发展情况以及分子分型进行选择,也可联系医学部了解详细招募标准,进行入组评估。
相信上面这些在研药物给了晚期胃癌患者新的希望,同时也能看出,随着新型临床研究的推进,对检测提出了更高要求,需要全面了解患者的基因图谱 ,已经做了检测的病友可提交病历至医学部初步评估获得用药方案及临床试验推荐。相信胃癌患者的明天会越来越好。

































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城