肝癌免疫治疗,肝癌免疫疗法,肝癌PD-1、肝癌PD-L1多款免疫联合疗法治疗
肝癌、肺癌和胃癌被称为中国癌症的三座大山,是中国最常见的三种癌症。今天小编要给大家讲解的就是肝癌。据2019年1月国家癌症中心发布的全国癌症报告中显示,肝癌新发病例46.6万,死亡比例42.2万,新发死亡比例为90.5%。由于发病的隐匿性、治疗的复杂性、超高的死亡率,肝癌在绝大多数中国人眼中被视作“癌中之王”。
除了“起病隐袭”外,肝癌还有个最为致命的特点早期极难被发现及确诊。目前仅有20%的患者能够在初次确诊后采取手术等根治性治疗,将近80%的患者一经发现就已到晚期,与彻底无进展生存的机会失之交臂。
中国是肝癌大国,肝癌人口占比超过全球患者的50%。这也从另外一个角度印证了肝癌是中国“癌中之王”的称号。它是中国发病率最高的五种癌症之一,在很长的一段时间里都缺乏足够的治疗手段。也正是因为治疗防范的欠缺,中国肝癌患者的5年生存率仅为12%,中晚期肝癌患者的5年生存率更是低至3%。
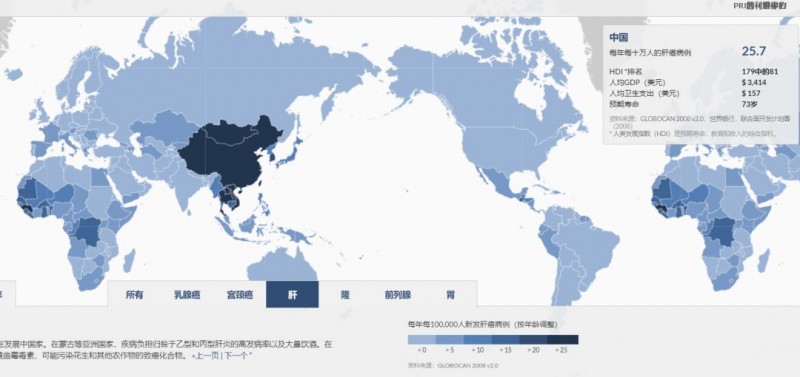
图为肝癌全球足迹
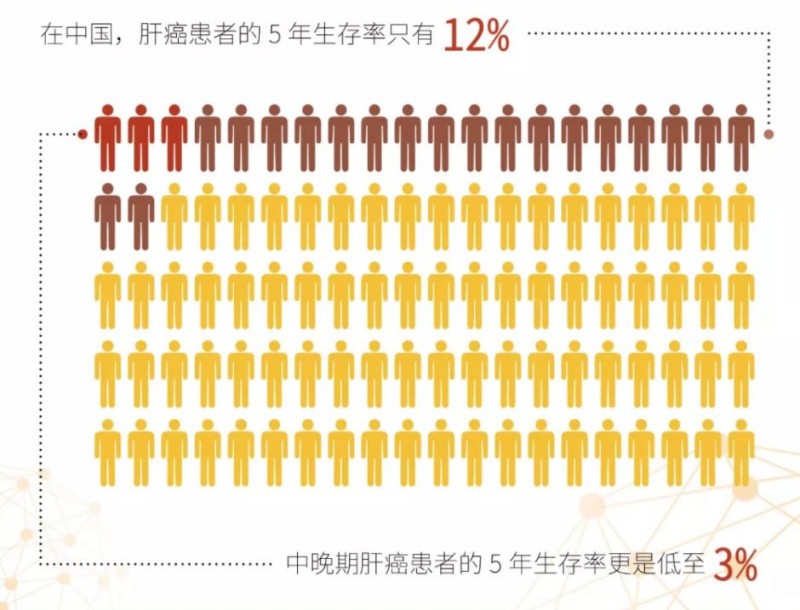
肝癌难上加难的治疗困境
肝癌死亡率高,主要在于早期病症隐秘,一经发现已是晚期,手术切除已经无法根治,预后较差。通常对于部分无法手术切除的晚期肝癌患者,主要的治疗手段包括:放射治疗,局部消融治疗、介入性肝动脉化疗栓塞(TACE)及系统治疗。
系统治疗一直是晚期肝癌治疗的重要阵地,除了以化疗、靶向治疗为主,就在今年3月4日,我国自主研发的免疫检查点抑制剂—卡瑞利珠单抗获批晚期肝癌适应症,标志着中国首个肝癌免疫疗法的到来。
不过,由于免疫过程和肿瘤微环境的复杂多变性,多种机制的共同作用影响免疫检查点药物(PD-1/PD-L1抗体)的疗效。在单药免疫治疗中,虽然O药和K药的效力较高,已被FDA批准,但是单药免疫治疗未能改善患者的OS,因此对肝癌患者的疗效十分有限。
多种免疫联合治疗,疗效锦上添花
随着各项研究的不段深入,联合免疫疗法应运而生,许多PD-1/PD-L1单抗开始寻找各自适合的治疗搭档,在肝癌疾病进展和提高患者生存期方面表现出亮眼的效果。这说明,联合免疫治疗很可能贯穿于肝癌治疗的全程,将成为未来的主流趋势之一。
在2020年HCC-TAG大会上,医学博士Anthony El-Khoueiry表示,继一系列针对肝细胞癌(HCC)的III期单药阴性试验之后,研究人员正在通过免疫疗法联合方案找到更好的结果。通常对于晚期肝癌患者来说,常见的联合药物分为4类:联合抗VEGF/VEGFR抗体、联合化疗、联合EGFR-TKI药物、联合CTLA-4抑制剂。那么下面小编就盘点一些研究结果瞩目的免疫联合治疗方案。
01、GO30140研究:肝癌免疫联合治疗带来惊人客观缓解率
在2019 亚太原发性肝癌专家(APPLE )会议上公布了GO30140研究中HCC患者治疗的观察结果。这是一项PD-L1抗体与抗血管生成药物联合的临床研究,其中阿替利珠单抗(atezolizumab)联合贝伐珠单抗(bevacizumab)联合疗法(简称为“T A”)对两组不可切除或转移性肝细胞癌(HCC)患者的一线治疗效果强。“T A”堪称为近十年来肝癌领域的里程碑式研究。
在试验A组中,患者采用阿替利珠单抗联合贝伐珠单抗治疗,中位随访时间为12.4个月,确认的客观缓解率(ORR)为36%,其中完全缓解率(CRR)为12%。每个mRECIST的ORR为39%,CRR为15%。未达到中位反应持续时间。68%~76%的患者持续反应。
在试验F组中,60例患者被分配为阿替利珠单抗联合贝伐珠单抗联合疗法组和阿替利珠单抗单一疗法组,中位随访时间为6.6个月。与atezolizumab单药治疗相比,该组合疗法可将疾病进展或死亡的风险降低45%。联合治疗组的中位PFS为5.6个月,而单药治疗组为3.4个月。
02、IMbrave150:III期研究显示肝癌迎来无进展生存希望
2019年11月22日,罗氏宣布一项旨在评估PD-L1免疫抑制剂阿替利珠单抗联合贝伐珠单抗用于治疗既往未接受过系统性治疗的不可切除的肝细胞癌(HCC)患者的研究——IMbrave 150 Ⅲ期临床试验取得双终点阳性结果,这一联合免疫方案取得令业界鼓舞的结果,成为10年来首个临床研究证实优于现有标准疗法索拉非尼的全新疗法。
IMbrave150是一项在501例既往未接受过系统性治疗的不可切除的HCC患者。患者按照2∶1的比例随机接受阿替利珠单抗和贝伐珠单抗联合治疗或索拉非尼治疗。患者接受联合治疗或对照组治疗,直至出现不可接受的毒性或研究者确定无临床获益。根据目前公布的结果显示,阿替利珠单抗与贝伐珠单抗免疫联合疗法在总生存期(OS)和无进展生存期(PFS)上都达到了显著的改善。
【研究试验数据】
1. 联合治疗组中位OS尚未达到,索拉菲尼组中位OS为13.2个月(10.4个月~NE)。
2. 与索拉非尼组相比,联合治疗组患者的死亡风险降低42%(风险比为0.58),同时使疾病恶化或死亡风险降低41%(风险比为0.59)。
3. 与索拉非尼组相比,联合治疗组还能延缓患者报告生活质量发生恶化的时间(11.2个月 vs 3.6个月)。
4. 联合治疗组肿瘤的ORR达到27%,其中CRR达6%。
5. 联合治疗组中位PFS为6.8个月,明显长于索拉非尼组的4.3个月。
6. 根据使用RECIST 1.1标准进行的独立评估,与索拉非尼组相比,联合治疗组的ORR更高(27% vs 12%)。使用HCC mRECIST标准进行组合的ORR接近3倍(33%vs 13%)。
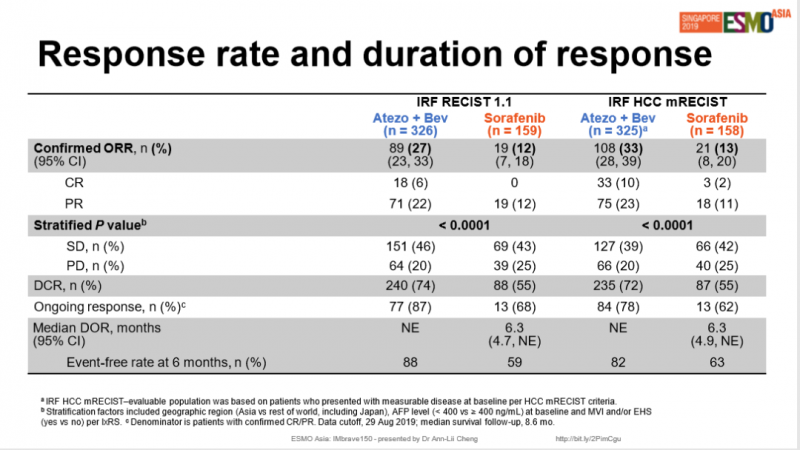
图为两组患者的确定ORR、P值等
阿替利珠单抗与贝伐珠单抗免疫联合疗法打破了晚期肝癌一线治疗的僵局,与标准疗法索拉非尼相比,OS和PFS均有显著延长。而且此试验中的缓解持续时间还没达到,甚至有不少患者达到CR,即肿瘤完全消失,这样的结果可以称得上“惊艳”。这也凸显了免疫治疗的优势——一旦有效,往往长期有效。
相比以往的一线治疗方式,“T A”不仅在疗效上效果显著,而且安全性也得到了认可,在肝癌治疗领域有了重大突破。
03、KEYNOTE-524/Study 116:FDA授予肝癌突破性疗法认定
2019年7月23日,默沙东和卫材联合宣布,美国FDA已经授予帕博丽珠单抗(Pembrolizumab,K药)与仑伐替尼(Lenvatinib)的KL组合疗法针对不能局部治疗的晚期不可切除的HCC患者的一线治疗突破性疗法认定,也就是可用于晚期HCC二线治疗。
这项研究数据分别按mRECIST和RECIST1.1标准进行评估,其中ORR分别为43.3%和53.3%,疾病控制率(DCR)分别为96.7%和90.0%。中位PFS为9.7个月,6、12个月生存率分别为83.3%和59.8%。最常见的治疗期间不良事件(TEAE)为食欲减低(63%)和高血压(60%),且未观察到新的不良事件。
这项研究表明,仑伐替尼联合K药的治疗确实能给晚期肝癌患者带来更大的希望,是安全且有效的联合疗法。
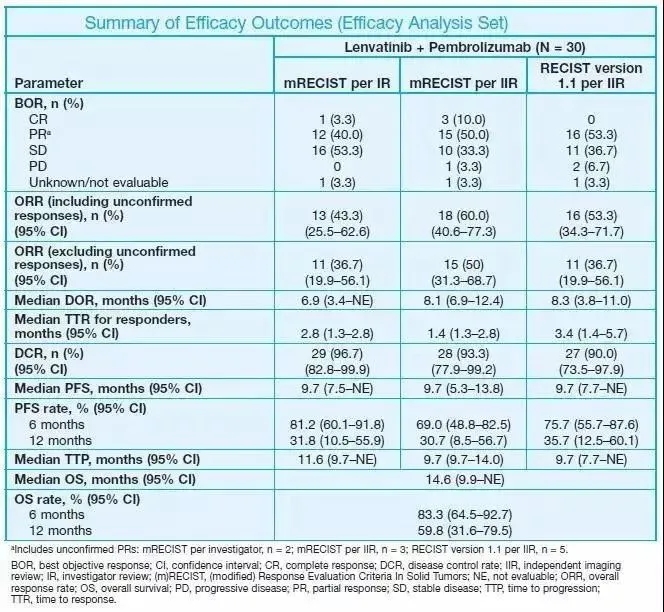
图为KEYNOTE-524/Study 116疗效结果总结
04、I/II CheckMate-040:首款晚期HCC双免疫疗法
2020年3月10日,美国FDA加速批准了nivolumab(Opdivo)联合ipilimumab(Yervoy)治疗先前接受过索拉非尼(Nexavar)治疗的肝细胞癌(HCC)患者。这是针对晚期肝癌的首款也是目前唯一一款用于晚期肝细胞的双免疫联合疗法。
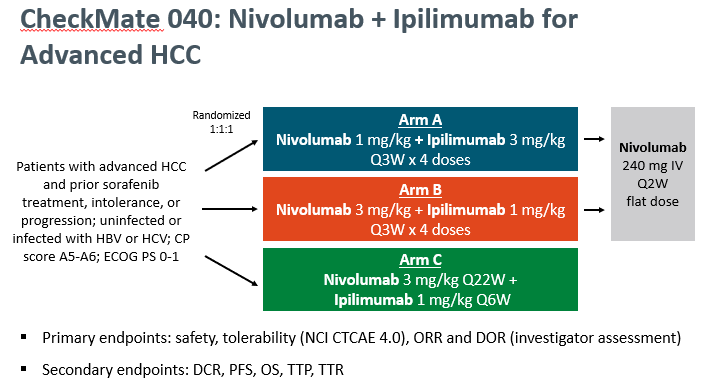
图为I/II CheckMate-040研究试验设计方案
此次批准是基于I/II CheckMate-040研究(NCT01658878)的结果,其中nivolumab和ipilimumab的组合可达到33%的客观缓解率(ORR),其中包括8%的CRR和24%的部分缓解率(PRR)。此外,持续反应时间从4.6到30.5+月不等,其中88%的患者反应持续≥6个月,56%的反应持续≥12个月,31%的反应持续≥24个月。
这意味着先前接受过索拉菲尼耐药的晚期肝细胞癌患者将多了一种全新的治疗选择。
肝癌靶向免疫治疗方案大盘点
2020年1月6日,国家卫生健康委发布《原发性肝癌诊疗规范(2019版)》中发布的系统治疗方案及先后顺序,给癌友们做一个简单的介绍及用药指导。
国内外肝癌获批药物
| 获批日期 | FDA获批肝癌药物 | 适应症 | 国内获批情况 |
| 2007-11 | Sorafenib(索拉非尼,Nexavar) | 用于治疗无法期初的肝细胞癌或肝癌 | 国内已上市且入医保 |
| 2018-8 | Lenvatinib(乐伐替尼,Lenvima) | 用于不可切除的肝细胞癌一线治疗 | 国内上市 |
| 2017-4 | Regorafenib(瑞戈非尼,Stivarga) | 用于索拉菲尼耐药肝癌的二线治疗 | 国内已上市且入医保 |
| 2017-9 | Nivolumab(纳武单抗,Opdivo) | 用于索拉菲尼耐药肝癌的二线治疗 | 国内上市 |
| 2018-11 | Pembrolizumab(派姆单抗,Keytruda) | 用于索拉菲尼耐药肝癌的二线治疗 | 国内上市 |
| 2019-1 | Cabozantinib(卡博替尼,Cabometyx) | 用于索拉菲尼耐药肝癌的二线治疗 | 国内上市 |
| 2019-5 | Ramucirumab(雷莫芦单抗,Cyramza) | 用于甲胎蛋白(AFP)≥400ng/ml且之前已接受过索莱菲尼(多吉美)治疗的肝细胞癌患者单药治疗 | 中国大陆未上市(可以美国、香港购买,但价格昂贵) |
一、一线治疗用药
索拉非尼( Sorafenib) 对于不同国家地区、不同肝病背景的晚期肝癌患者都具有一定的生存获益( 证据等级 1)。
仑伐替尼(Lenvatinib)适用于不可切除的 中国肝癌的分期方案(CNLC) IIb、IIIa、IIIb期、肝功能 Child-Pugh A级的肝癌患者, 其一线治疗效果不劣于索拉非尼, 乙型肝炎病毒(HBV)相关肝癌具有较好的生存获益(证据等级 1)。
FOLFOX4方案在我国被批准用于治疗不适合手术切除或局部治疗的局部晚期和转移性肝癌(证据等级 1)。
奥沙利铂的系统化疗联合索拉非尼可使客观缓解率有所提高,无进展生存时间和总生存时间均有延长,且安全性良好(证据等级 3)。
对于肝功能和体力状态良好的患者,可考虑此联合治疗,但尚需临床随机对照研究提供高级别循证医学证据。另外,三氧化二砷对中晚期肝癌具有一 定的姑息治疗作用(证据等级 3)。
二、二线治疗用药
瑞戈非尼( Regorafenib)被批准用于既往接受过索拉非尼治疗的 CNLC IIb、IIIa和 IIIb 期肝癌患者(证据等级 1)。
美国FDA批准纳武利尤单抗( Nivolumab)和帕博利珠单抗( Pembrolizumab)用于既往索拉非尼治疗后进展或无法耐受索拉非尼的肝癌患者(证据等级 2)。目前,中国企业自主研发的免疫检查点抑制剂,如卡瑞利珠单克隆抗体、特瑞普利单克隆抗体、信迪利单克隆抗体等正在 开展临床研究。
美国 FDA 批准卡博替尼用于一线系统治疗后进展的肝癌患者(证据等级 1),批准雷莫芦单克隆抗体用于血清AFP水平≥400ng/mL 肝癌患者的二线治疗(证据等级 1)。但是, 这两种药物尚未在国内上市。国产小分子抗血管生成靶向药物阿帕替尼用于肝癌患者二线治疗的临床研究正在进行中。
小编有话说
免疫肿瘤药物在临床研究中显示出较于既往的标准治疗方案的优势,如具有较长的疗效持续时间和生存时间等,使得业界对免疫疗法的应用前景以及与其他治疗手段的联合寄予厚望。
肝癌的病因特别复杂,为进一步提升肝癌治疗的效果,需要以“组合拳”,即免疫肿瘤药物联合介入治疗、抗血管生成药物、化疗和其他免疫肿瘤药物等是目前临床研究的重点和热点。此外,时刻关注前沿药物的进展及临床效果才能让癌友们寻求更多治疗选择。

黎功
北京清华长庚医院主任医师
教授 硕士生导师

Andrew Xiuxuan Zhu
麻省总医院肝癌研究中心主任
科室:肝癌
专长:结直肠癌、食管癌、胆囊癌、胃肠癌、胰腺癌、肝癌
参考文献
1.https://www.esmo.org/newsroom/press-office/esmo-asia-congress-2019-imbrave150-atezolizumab-bevacizumab-hepatocellular-carcinoma-hcc-cheng
2.https://www.onclive.com/web-exclusives/fda-approves-nivolumabipilimumab-for-advanced-hcc
3.http://www.medsci.cn/article/show_article.do?id=124e1844e341
4.http://www.medsci.cn/article/show_article.do?id=742f1e7000ae
5.http://news.bioon.com/article/6747106.html
6.https://www.onclive.com/conference-coverage/hcc-tag-2020/immunotherapy-combinations-show-promise-in-advanced-hcc?p=1


































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城