肝内胆管癌新药,口服靶向药,FGFR抑制剂,FGFR靶向药Futibatinib(TAS-120),胆管癌临床试验ICP-192招募中
根据2020年ESMO大会提前公开的海报,一款针对多种实体瘤的新药futibatinib即将在大会上公开其治疗FGFR2融合/重排阳性肝内胆管癌患者的Ⅱ期研究中期数据。
无进展生存7.2个月,整体缓解率37.3%
根据目前公开的研究结果,在最少6个月的随访期内,所有接受futibatinib治疗的患者的整体客观缓解率达到37.3%,其中完全缓解率1.5%,部分缓解率35.8%。
整体来说,所有患者的疾病控制率达到了82.1%,中位缓解持续时间为8.3个月;所有达到临床缓解的患者,从开始接受治疗到能够被判定为临床缓解的时间中位数为2.5个月。
所有患者的中位无进展生存期为7.2个月;6个月无进展生存率为61%,6个月总生存率为86%。
3级以上不良事件发生率57%,多数患者需调整用药剂量或中断用药
在不良反应方面,因futibatinib治疗而发生3级或以上不良事件的患者占57%,10%的患者报告了严重的不良事件。在所有患者中,66%因发生不良事件而进行了用药剂量调整;其中,55%的患者曾经中断用药,51%的患者曾经降低用药剂量。
27%的患者经历了3级或以上的高磷酸盐血症,均可对症用药治疗,没有患者因高磷酸盐血症终止治疗。
54%的患者因疾病进展或放疗后遗症而停止用药,治疗期间无患者死亡。
该研究的Ⅰ期剂量递增试验将futibatinib的最大耐受剂量确定为20 mg qd。
Futibatinib:靶向FGFR,泛癌种治疗潜力强大
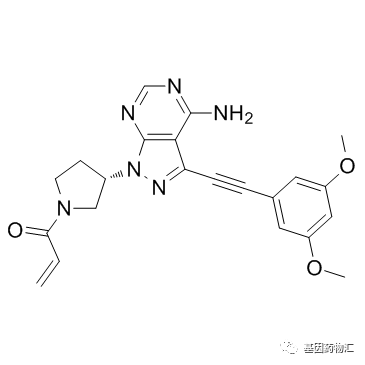
Futibatinib(TAS-120)
Futibatinib(TAS-120)是一款口服药物,为高选择性、不可逆的FGFR抑制剂药物,对于FGFR1~4均有较好的抑制效果。
目前,已经公开的futibatinib临床试验除本次公开中期结果的Ⅱ期胆管癌试验外,还有联合吉西他滨+顺铂治疗FGFR2基因重排阳性的晚期、转移性或复发性不可切除胆管癌的Ⅲ期FOENIX-CCA3研究(NCT04093362),以无进展生存期、临床缓解率、缓解持续时间、总生存期和安全性与耐受性为终点;futibatinib治疗FGFR扩增阳性的局部晚期或转移性乳腺癌的Ⅱ期临床研究(NCT04024436)也在进行,计划评估组内168例患者的缓解率、临床获益率及6个月无进展生存率。
此外,futibatinib治疗晚期或转移性实体瘤、晚期或转移性胃及胃食管交界处癌的Ⅱ期临床研究也在招募患者。我们会持续关注研究进展,并为患者传递最新咨询。
我国自主研发新药ICP-192重磅登场,填补临床空白
目前,针对胆管癌的靶向药物非常少,仅有今年4月获批的pemigatinib(Pemazyre)一款,且尚未进入中国市场。本次公开中期研究结果的futibatinib距离正式获批还需要较长的时间,国内胆管癌患者的治疗需求仍存在大量空白,亟待更多新药填补。
幸而,乘着2017年中国国家食品药品监督管理局加入ICH的“东风”,近几年国内药物研发进展迅速,创新药物数量井喷式增长。我国自主研发的肝内胆管癌新药也开始投入临床试验,针对FGFR2靶点的重磅新药ICP-192面世,开始免费招收患者了!
ICP-192:二代FGFR抑制剂,四大优势显著
我国药企北京诺诚健华医药科技有限公司自主研发的ICP-192属于二代FGFR抑制剂药物,与以厄达替尼为代表的经典一代FGFR-TKI药物相比,具有特异性更强、药效更持久、对于耐药突变仍然有效、具备泛癌种治疗潜力这四项巨大优势。关于ICP-192更详细的资料可以咨询全球肿瘤医生网医学部。
在已经完成的ICP-192 Ⅰ期安全性临床试验中数据显示:剂量为2~12 mg时ICP-192安全状况良好,大多数不良反应为1~2级,未报告治疗相关的剂量限制性毒性;而试验同时也证实,8 mg剂量时已达到有效药物浓度(数据截止到2019年12月)。
目前,ICP-192治疗肝内胆管癌的Ⅱ期临床试验正在开展,国内患者免费用药的机会来了!
免费用药机会来了!ICP-192治疗肝内胆管癌临床试验重磅开启!
由上海市东方医院牵头,国内30家医疗机构共同参与,采用我国自主研发创新药物ICP-192治疗FGFR2易位/融合突变的肝内胆管癌患者的临床试验正式开始招募患者了!
试验名称:一项评价ICP-192在实体瘤受试者中的安全性、耐受性、药代动力学的单中心、非随机、开放性I期临床试验
临床分期:Ⅱa期
纳入标准:
1、年龄18~75岁(含两端),男性或女性;
2、(剂量递增阶段)ECOG体力评分为0~1分,
2、(剂量扩展阶段)ECOG体力评分为0~2分;
3、(剂量递增阶段)经组织病理学证实的不可切除或者转移的肝内胆管癌,已知的治疗方式无效或复发的,或标准治疗下仍发生进展、不耐受标准治疗或不存在标准治疗的患者;
3、(剂量扩展阶段)经组织或细胞病理学证实的不可切除、 复发或转移性肝内胆管癌,一线化疗失败或不能耐受(2次减量仍不能耐受),或新辅助/辅助化疗后6个月内进展或复发的患者;
4、存在FGFR易位/融合突变;
5、详细纳入及排除标准可咨询无癌家园医学部(400-626-9916)。







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城