实体瘤血液肿瘤新CAR-T细胞免疫疗法AUTO3、JNJ-4528和ALLO-501联合ALLO-647疗效不俗
近两年兴起的嵌合抗原受体T(CAR-T)细胞疗法可谓是肿瘤免疫治疗中的一匹黑马,它的出现代表了个性化癌症治疗的重大进步,特别是给血液系统恶性肿瘤患者带来重生的希望。
2017年更是被称为CAR-T疗法的元年。这是由于FDA在2017年先后批准了全球首先的两个,也是目前仅有的两个CAR-T细胞疗法商业产品:诺华的Kymriah(淋巴瘤)与吉利德的Yescarta(白血病),由此癌症免疫治疗进入了一个新时代。
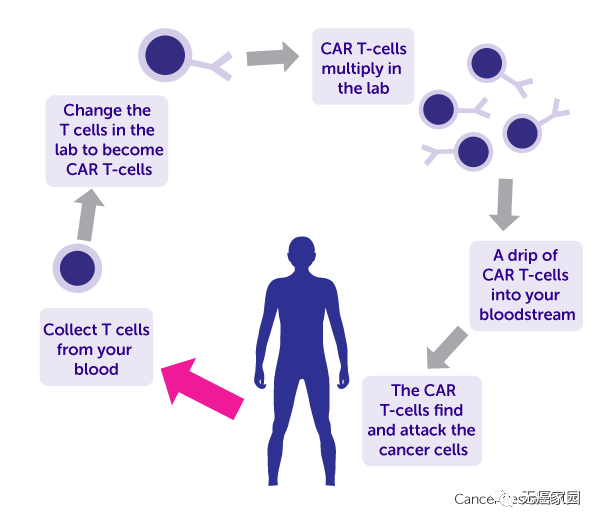
而此次2020年欧洲医学肿瘤学会虚拟大会(ESMO 2020)上,公布了一款双特异性CAR-T产品AUTO3的临床研究数据,针对复发性/难治性弥漫性大B细胞淋巴瘤(DLBCL)。
从更新的数据显示出AUTO3具有积极的安全性和有效性,并且能够有效减低患者的肿瘤复发率。
93%完全缓解患者未复发,双靶向CAR-T疗效过硬
AUTO3是一款双重CAR-T细胞产品,相较于血液肿瘤的肿瘤细胞中国的祖传靶点——CD19,此款产品还兼具CD22。
通过同时靶向两种B细胞抗原,AUTO3被设计成可最大程度减少B细胞恶性肿瘤患者因单一抗原丢失而引起的复发。
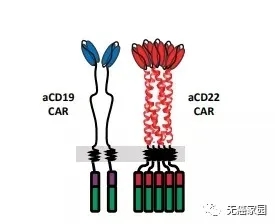
图片来源:autolus
数据截止到2020年8月13日,此研究中有35例复发性/难治性弥漫性大B细胞淋巴瘤患者接受AUTO3输注,以评估其安全性和有效性。
在35例患者中,可评估的有30例,客观缓解率为68%,完全缓解率为54%;在第一天接受pembrolizumab(派姆单抗)预处理(RP2D)的队列中(N=20),客观缓解率为71%,完全缓解率为64%。
迈阿密大学米勒医学院的医学教授Craig Moskowitz表示:“与获得批准的CD19 CAR-T相比,AUTO3具有更优的耐受性和安全性,并且到目前为止,完全缓解的效果也很持久。在中位随访为6个月的所有剂量队列中,达到完全缓解的患者中有93%未复发。”
疗效与已上市CAR-T相当,AUTO3安全性更胜一筹
从疗效上来看,AUTO3与Yescarta、Kymriah这两款已经上市的CAR-T细胞的完全缓解率相差无几。但是在安全性方面更胜一筹,AUTO3的耐受性良好,没有≥3级的细胞因子释放综合征(CRS),神经毒性(NT)发生率较低。
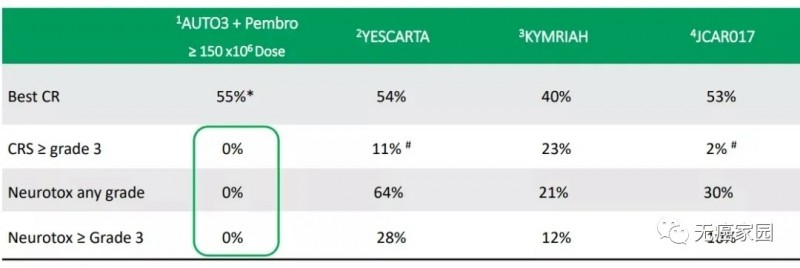
图片来源:Autolus公司今年3月简报
无癌家园专家点评
该疗法具有新型靶向特性以用于治疗B细胞恶性肿瘤,旨在减少细胞因子释放综合征(CRS)。(想要了解更多关于血液肿瘤的CAR-T疗法请持续关注无癌家园医学部400-626-9916。)
百花齐放,多款新型CAR-T疗法征伐血液肿瘤
除了上述提到的CAR-T细胞疗法外,还有多款新型CAR-T疗法在国际血液淋巴肿瘤领域乃至整个肿瘤领域备受关注。
1、总缓解率100%!BCMA CAR-T疗法JNJ-4528疗效强劲
JNJ-4528是一种研究性B细胞成熟抗原(BCMA)导向的CAR-T疗法,用于治疗复发或难治性多发性骨髓瘤(RRMM)。这些患者在治疗前平均接受过5种前期疗法,76%的患者接受过5种治疗,86%的患者对5种疗法耐药,其中包括CD38治疗,而且对蛋白酶抑制剂PI和免疫调节剂IMiD双重耐药。简单说就是复发难治、后续缺乏有效的疗法。
此款CAR-T疗法的原理与目前的PD-1/L1不同,它是直接利用患者体内的T细胞,将其在体外进行改造,大量复制后再会输到患者体内,以达到杀灭癌细胞的目的。
在2020年ASCO大会上公布了此项Ib/II期CARTITUDE-1临床研究的最新数据,总共纳入29例难治性多发性骨髓瘤患者,在接受JNJ-4528细胞疗法后,效果令人惊喜。

【研究结果】
客观缓解率高达100%,其中完全缓解率为76%,非常好或更好的部分缓解率为21%,部分缓解率为3%。
完全缓解中位时间为2个月(1~9个月),26例患者无进展,6个月无进展生存率为93%,最长反应持续时间为15个月。安全性整体可控。
2、总缓解率达78%,通用型ALLO-501联合ALLO-647疗效不俗
2020年ASCO大会上公布的ALPHA研究是关于ALLO-501和ALLO-647应用于复发/难治大B细胞或滤泡性淋巴瘤(R/R LBCL/FL)的首次人体研究数据。研究对象为曾接受过至少2线治疗的R/R LBCL/FL,其中接受过靶向CD19细胞治疗的患者也可入组。

截至2020年1月20日,共招募了12例患者,9例接受了ALLO-501的3个DL治疗(以40/120/360×106三个剂量水平),1例患者在淋巴细胞清除治疗之前因肾损伤停止治疗,2例在治疗开始后终止。中位治疗线数3次(2-4次)。所有患者ALLO-647治疗剂量为39mg。
研究结果显示,总缓解率达78%,3例完全缓解,4例部分缓解。不过,据该公司报道,最初缓解的患者中有3例在6个月内复发。
据报道,ALLO-501中的编码TCR α的基因被敲除,以期降低移植物抗宿主病(GvHD),而CD52基因被破坏,则允许抗CD52单克隆抗体ALLO-647的使用,以选择性清除宿主淋巴细胞并延长宿主淋巴细胞清除状态。本次在试验中接受治疗的患者中也确实中没有观察到GvHD。
血液肿瘤!实体瘤!新型CAR-T疗法通通不放过
除了上述在提到的CAR-T疗法在血液肿瘤方面的突破性临床研究外,目前国内正在积极开展血液肿瘤及实体瘤的CAR-T临床研究。若想若想参加可以咨询无癌家园医学部申请参与CAR-T实体肿瘤的临床试验。
CAR-T细胞免疫疗法的横空出世使广大肿瘤患者看到了希望,以CAR-T疗法为代表的细胞免疫治疗将是未来5~10年全球生物制药行业最热门的领域。小编相信在不久的将来,越来越多的临床试验数据将会不断涌现,CAR-T疗法不仅会在血液肿瘤领域大放异彩,在实体瘤方面也会日益彰显其蕴藏的实力!
参考文献
1.https://autolus.gcs-web.com/news-releases/news-release-details/autolus-therapeutics-presents-additional-data-auto3-dlbcl-0
2.ASCO2020-abstracts.PDF.
3.https://ascopubs.org/doi/abs/10.1200/JCO.2020.38.15_suppl.8505
4.https://servier.com/wp-content/uploads/2020/05/PR_Allogene-ASCO.pdf

































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城