粪土是金|一文搞懂什么是粪菌移植
文章导读
粪便微生物群移植(FMT)是新型并且非常有前途的一种治疗方案,主要治疗艰难梭状芽胞杆菌感染(CD)。
因需要将健康人的排泄物转移到患者肠道中,粪便移植需要非常严格和安全的管理流程。本文总结最新专家共识供大家共同参考。
1.初筛患有以下疾病不能入选FMT捐赠者
(1)传染病
▸明确的艾滋病病毒、乙肝病毒、丙肝病毒、梅毒、人类T淋巴细胞白血病病毒I和II、疟疾、锥虫、结核杆菌感染或接触史;
▸明确的全身感染尚未控制;
▸吸毒;
▸不洁性行为;
▸组织/器官移植史;
▸输血史(<12个月);
▸针刺受伤史(<6个月);
▸纹身、穿体洞、穿耳孔、针灸史(<6个月);
▸医疗卫生条件差;
▸存在朊病毒传染风险;
▸近期感染寄生虫、轮状病毒、兰伯氏贾第虫及其他胃肠道微生物;
▸近期(<6个月)在热带、传染病高风险或旅行者腹泻国家旅游;
▸近期(<6个月)接种减毒活疫苗,可能存在传染风险;
▸从事医务工作(需排除传播多重耐药微生物风险);
▸从事接触动物的工作(需排除传播人畜共患病风险)。
(2)胃肠道、代谢和神经系统疾病
▸肠易激综合征、炎症性肠病、慢性功能性便秘、乳糜泻和其他慢性胃肠道病史;
▸慢性系统性自身免疫病胃肠道受累史;
▸高风险胃肠道癌症或息肉病或病史;
▸近期出现腹泻、便血;
▸神经/神经退行性疾病史;
▸精神疾病史;
▸超重和肥胖[体重指数(BMI)]>25。
(3)使用影响肠道微生物群的药物
▸近期(<3个月)抗生素、免疫抑制剂、化疗药物使用史;
▸长期使用质子泵抑制剂。
2.FMT当天检查出以下疾病不能入选捐赠者
▸新出现的胃肠道症状和体征,如腹泻、恶心、呕吐、腹痛、黄疸;
▸新出现的一般症状和体征,如发热、咽痛,淋巴结肿大;
▸最近一次FMT检查前使用抗生素或其他可能影响肠道微生物群的药物,有新的性伴侣或出国旅行;
▸最近摄入可能对接受FMI患者有害的物质;
▸在热带地区旅行,接触过其他人血液(伤口、穿体洞、纹身)及高风险性行为;
▸FMT前4周内捐赠者及周围人(包括儿童)出现腹泻(≥3次/d稀便或水样便)。
3.血液和粪便测试检查排除捐赠者存在任何潜在的传染病
(1)一般血液检测
▸巨细胞病毒;
▸EB病毒;
▸甲肝病毒;
▸乙肝病毒;
▸丙肝病毒;
▸戊肝病毒;
▸梅毒螺旋体;
▸HIV-1和HIV-2病毒;
▸溶组织内阿米巴原虫;
▸血细胞计数及分类;
▸C反应蛋白和血沉;
▸血清白蛋白;
▸血清肌酐和电解质;
▸血清转氨酶、胆红素、谷氨酰基转肽酶华和碱性磷酸酶。
(2)特殊血液检查
▸T淋巴细胞病毒Ⅰ和Ⅱ型抗体;
▸粪类圆线虫。
(3)一般粪便检查
▸CD;
▸肠道病原菌,如沙门氏菌、志贺菌属;
▸弯曲杆菌,大肠埃希菌,鼠疫杆菌,耐万古霉素肠球菌,耐甲氧西林金黄色葡萄球菌,革兰染色阴性多重耐药菌;
▸诺如病毒;
▸兰氏贾第鞭毛虫和隐孢子虫抗原和/或抗酸染色;
▸原生动物(包括致病性人酵母菌)和寄生虫;
▸粪便潜血试验。
(4)特殊粪便检查
▸霍乱弧菌和李斯特菌;
▸等孢子球虫和微孢子虫抗原和/或抗酸染色;
▸钙卫蛋白;
▸幽门螺杆菌抗原;
▸轮状病毒。
4.制备新鲜和冷冻粪便材料
(1)新鲜粪便材料
▸新鲜粪便为排泄6h内粪便;
▸为保护厌氧菌,粪便存储和准备过程应尽量简单;
▸粪便样本应存储于室温环境(20-30℃);
▸尽量厌氧存储和处理;
▸至少使用30g粪便;
▸将粪便置于生理盐水中搅拌后筛掉,留取混悬液;
▸防止肠道细菌形成孢子。
(2)冷冻粪便材料
▸至少需要30g粪便和150ml生理盐水;
▸制作粪便混悬液方法同(1);
▸混悬液冷冻前应添加甘油,使其浓度为10%;
▸混悬液应存储在-80℃无氧环境中;
▸FMT当天混悬液在37℃水浴下解冻;
▸解冻后可根据所需量添加生理盐水;
▸解冻后6h内灌注;
▸应避免重复解冻和冷冻。
5.FMT适应证(表)
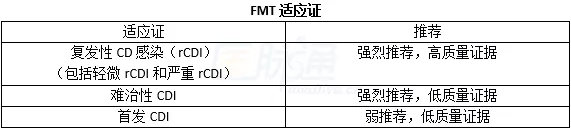
6.FMI治疗流程
(1)抗菌素:rCDI患者应在FMT前应用万古霉素或非达霉素至少3d,FMT前12-48h停用(强烈推荐,中等质量证据)。
(2)灌肠:rCDI患者在FMT前予聚乙二醇灌肠,FMT通过上消化道途径或结肠镜灌注(弱推荐,低质量证据)。
(3)经结肠镜FMT:通常将混悬液注入右半结肠,但对严重结肠炎患者,混悬液应注入左半结肠(强烈推荐,高质量证据)。研究发现灌注由20-100g粪便制成的200-500ml混悬液是安全的。
(4)经灌肠液FMT:应保持灌肠液在肠道内至少30min,患者呈仰卧位以减少便意(强烈推荐,低质量证据)。
(5)经上消化道FMT:通过上消化道FMT可以执行。粪便悬浮液可以通过胃镜、胃管、鼻空肠管或胃造瘘管灌注。灌注后患者需保持45℃半卧位4h防止反流(强烈推荐,高质量证据)。
(6)安全性:各种途径FMT即使对于免疫力低下或危重症患依然安全,最好选择灌肠液灌注(强烈推荐,低质量证据)。
(7)重复灌注:在初次治疗失败或CDI复发后可重复灌注(强烈推荐,高质量证据)。
(8)观察短期不良反应:如腹泻、腹痛、嗳气、便秘、发热等(弱推荐,低质量证据)。
(9)观察长期不良反应:目前尚无足够数据(弱推荐,低质量证据)。
(10)观察疗效:应随访至少8周(强烈推荐,低质量证据)。
参考文献
1. Cammarota G, Ianiro G, Tilg H, et al. European consensus conference on faecal microbiota transplantation in clinical practice. Gut 2017.
2. van Nood E, Vrieze A, Nieuwdorp M, et al. Duodenal infusion of donor feces for recurrent Clostridium difficile. N Engl J Med 2013;368:407–15.
3. Cammarota G, Masucci L, Ianiro G, et al. Randomised clinical trial: faecal microbiota transplantation by colonoscopy vs. vancomycin for the treatment of recurrent Clostridium difficile infection. Aliment Pharmacol Ther 2015;41:835–43.
4. Lee CH, Steiner T, Petrof EO, et al. Frozen vs fresh fecal microbiota transplantation and clinical resolution of diarrhea in patients with recurrent Clostridium difficile infection: a randomized clinical trial. JAMA 2016;315:142–9.
5. Cammarota G, Ianiro G, Gasbarrini A. Fecal microbiota transplantation for the treatment of Clostridium difficile infection: a systematic review. J Clin Gastroenterol 2014;48:693–702.
6. Kassam Z, Lee CH, Yuan Y, et al. Fecal microbiota transplantation for Clostridium difficile infection: systematic review and meta-analysis. Am J Gastroenterol 2013;108:500–8.
7. Drekonja D, Reich J, Gezahegn S, et al. Fecal microbiota transplantation for Clostridium difficile infection: a systematic review. Ann Intern Med 2015;162:630–8.
8. Mattila E, Uusitalo-Seppälä R, Wuorela M, et al. Fecal transplantation, through colonoscopy, is effective therapy for recurrent Clostridium difficile infection. Gastroenterology 2012;142:490–6.
9. Lessa FC, Mu Y, Bamberg WM, et al. Burden of Clostridium difficile infection in the United States. N Engl J Med 2015;372:825–34.
10. Varier RU, Biltaji E, Smith KJ, et al. Cost-effectiveness analysis of fecal microbiota transplantation for recurrent C. difficile infection. Infect Control Hosp Epidemiol 2015;36:438–44.
本文由作者投稿,转载请务必注明作者及来源。
作者:天津市胸科医院 小可真;来源:医脉通


































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城