胃癌新药,抗体偶联(ADC)药物Enhertu(DS-8201、Deruxtecan)获FDA优先审查资格
2020年10月28日,阿斯利康与第一三共株式会社联合发布公告称,FDA已经接受了其共同研发的ADC药物Enhertu(Trastuzumab Deruxtecan,曾用名DS-8201)的补充生物制剂许可申请,并授予其优先审查资格,用于治疗HER2阳性的胃及胃食管交界处腺癌患者。
该批准基于Ⅱ期的DESTINY-Gastric01试验结果,其结果显示,与化疗相比,Enhertu治疗曲妥珠单抗治疗后进展的HER2阳性胃及胃食管交界处腺癌患者,获得了更高的缓解率。
缓解率接近4倍,中位总生存期12.5个月
与化疗相比,Enhertu在整体缓解率、无进展生存、总生存期和生存率方面均展现出了显著的优势。
接受Enhertu治疗的患者,整体缓解率为51.3%,中位无进展生存期为5.6个月,中位总生存期为12.5个月;接受化疗的患者,整体缓解率为14.3%,中位无进展生存期3.5个月,中位总生存期8.4个月。
在无进展生存率方面,Enhertu治疗患者的6个月无进展生存率为20.6%,1年无进展生存率为29.9%;接受化疗的患者仅为20.6%和0%。
在缓解持续时间方面,Enhertu治疗的中位缓解持续时间达到了11.3个月,化疗的中位缓解持续时间仅为3.9个月。
最常见不良事件为嗜中性粒细胞数量减少
在不良反应方面,Enhertu治疗和化疗的患者最常见的不良事件均为嗜中性粒细胞减少(51% vs 24%),贫血(38% vs 23%)和白细胞计数减少(21% vs 11%)。
在接受Enhertu治疗的患者中,15.2%的患者因无法耐受而导致中止治疗,这一比例在接受化疗的患者中为6.5%;剂量限值性毒性在Enhertu治疗的患者中发生率为32.0%,在化疗患者中为33.9%。
接受Enhertu治疗,医生应密切关注患者的症状表现,一旦发生不良事件,及时进行处理或调整用药剂量。
曾获突破性治疗指定与孤儿药称号
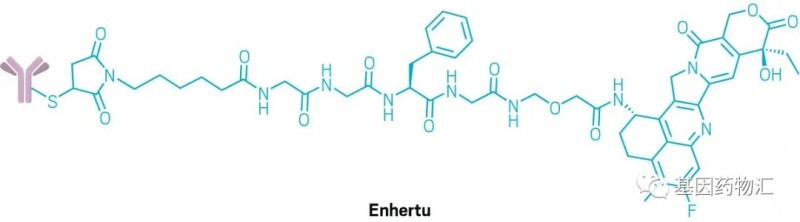
Enhertu(DS-8201)是一款HER2导向的抗体-药物偶联物(ADC),已经在美国和日本获批用于治疗不可切除或转移性HER2阳性乳腺癌成年患者。
2020年5月时,Enhertu曾获得FDA突破性治疗指定称号,用于治疗曾接受过2种或以上治疗方案的,不可切除或转移性HER2阳性胃及胃食管交界处腺癌。在这一适应症上,Enhertu还曾获得过孤儿药称号。
2020年9月,Enhertu在日本获批了胃及胃食管交界处腺癌的适应症。
胃癌是全球第五大最常见的癌症,也是癌症死亡的第三大原因。转移性胃癌患者的5年生存率不足5%,为恶性程度最高的癌种之一。
约20%的胃癌存在HER2突变,自靶向药物治疗问世以来,HER2阳性的晚期或转移性胃癌的一线治疗方案为曲妥珠单抗联合化疗的方案,疗效比强于传统化疗、但对于在一线治疗中进展的转移性胃癌患者,并没有其它获批的靶向药物可用。
第三一共制药的肿瘤学执行副总裁兼全球负责人在新闻稿中总结道:“DESTINY-Gastric01试验的结果是突破性的,为经治的HER2阳性转移性胃癌患者带来了全新的希望。”
小汇有话说:胃癌治疗蓬勃发展,新药涌现
我国是胃癌最高发的国家之一,每年的胃癌患者数量远远超过其它国家,晚期患者5年生存率不足20%,生存情况不容乐观。
作为患病人数最多、恶性程度最高的几种癌症之一,长期以来胃癌一直受到了医疗界的重点关注。除了已经获批的曲妥珠单抗及抗血管生成抑制剂阿帕替尼(国内已获批)和雷莫芦单抗(国外获批)等药物以外,还有许多重磅在研新药。
如针对Claudin 18.2靶点的新药Zolbetuximab,Claudin 18.2是一个近期大热的消化系统肿瘤新靶点,约在60%的胃癌中表达。采用Zolbetuximab+CAPOX化疗方案治疗局部晚期或转移性胃癌患者,中位无进展生存期为7.9个月,中位总生存期13.2个月;而仅采用CAPOX化疗方案治疗的患者,中位无进展生存期为4.8个月,中位总生存期为8.4个月。
目前,Zolbetuximab的Ⅲ期临床试验正在开展,面向全国范围内招募局部晚期不可切除或转移性胃及胃食管交界处腺癌患者,符合标准、同时有意接受新药治疗的患者可以联系医学部(400-666-7998),或将病例资料发送至招募中心邮箱(doctorjona0404@gmail.com)进行申请。
又如国内药企研发的雷莫芦单抗“Me-Too”药物金妥昔单抗,疗效也相似,同属于抗血管生成类药物。金妥昔单抗的临床试验寻找的患者为既往接受过一线化疗,且在治疗期间或治疗结束后3个月内疾病进展的晚期或转移性胃或胃食管结合部腺癌患者,也就是说,曾经接受过化疗的患者同样有机会使用这款新药!符合标准的患者可以按照上述联系方式进行申请。
医学技术的发展是一个“格物致知”的过程。研究者们不断深入地探索,剖析原理,进而探寻更加精准的治疗方案。相信在不远的未来,一定会有更多、更有效的治疗药物与方案问世,能够针对患者的病情,更加个性化、更加精准、更加有效地施治。
治疗癌症的路上,我们从未停止前行。


































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城