非小细胞肺癌新药波齐替尼(Poziotinib)两种不同量用药方案论证临床试验安全性和临床试验的意义
我们都知道,临床试验主要用于评估一款新药的疗效和安全性等指标,对于新药的上市具有决定性的意义。但近期,一项对于非小细胞肺癌患者的临床试验早期评估结果显示,选择每日一次较大剂量用药,或每日两次较小剂量用药的方案,在每天摄入药物总剂量一致的情况下,对于安全性有着巨大的影响。
这是一项针对EGFR及HER2外显子20插入(ex20ins)突变型非小细胞肺癌患者的临床试验项目,由研究者在2021年欧洲医学肿瘤学会靶向疗法虚拟大会上公开,使用的治疗药物是一款在研新药波齐替尼(Poziotinib)。
6/8 mg×2 vs 12/16 mg×1
ZENITH20试验(NCT03318939)共分为7个试验组,研究者分析了第3组和第5组患者的治疗效果。其中第3组分析了EGFR ex20ins患者接受波齐替尼治疗的缓解率、疾病控制率、缓解时间及安全性和耐受性,第5组为剂量探索试验组,分析了患者接受每天两次6、8 mg给药,或每天一次10、12、16 mg给药的效果。
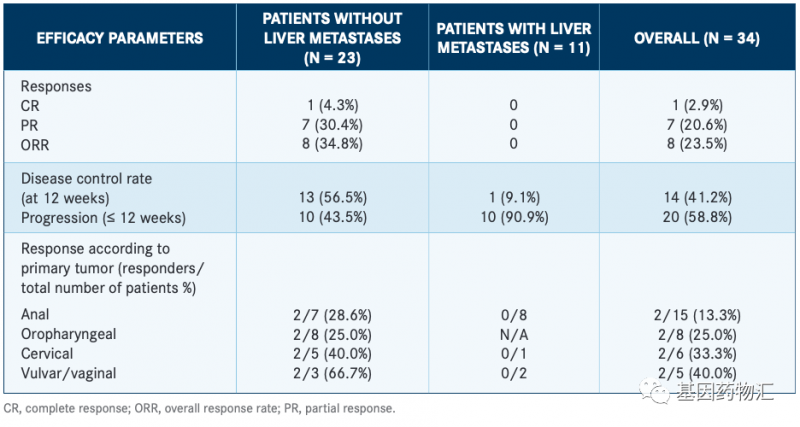
第3组结果显示,患者的整体缓解率为27.8%,疾病控制率为86.1%,中位无进展生存期为7.2个月;15%的患者仍在接受治疗。
整体来说,91%的患者在接受治疗后肿瘤病灶体积缩小,缩小百分比的中位数为25.5%。
第5组结果显示,每日两次接受6、8 mg剂量药物治疗的患者中,分别有50%和63%的患者治疗中断,38%和50%的患者因不良事件等原因降低了剂量;而在每日一次接受12、18 mg剂量药物治疗的患者中,这两个比例分别为87%和82%以及57%和59%。
尽管这一组的招募尚未结束,试验结果仍处于初步分析阶段,但已经可以看出明显的差异。研究者指出,使用每日两次低剂量用药的方案,患者的不良反应发生率显著降低了。
接受每日两次6 mg药物治疗的患者,治疗相关不良反应发生率为19%,每日两次8 mg的患者为31%,每日一次12 mg的患者为39%,每日一次16 mg的患者为45%;这几个剂量组的患者,3级或以上严重不良事件发生率分别为19%、19%、35%和36%。
临床试验有多重要?每个细节都可能决定疗效!
尽管此次公开的只是初期研究结果,但我们已经可以从中看出一些端倪。两类方案,对于患者来说,每日用药的总量是一致的,却因为改变了用药的单次剂量和用药的频次,安全性以及患者的耐受性差别非常明显。
在无需降低患者每日用药总剂量的情况下,将用药的频次改为2次,就能显著提升患者的耐受性,让更多患者有机会完成治疗了!
这提示我们,治疗中的任何一点细节都可能改变患者的最终结局,因此临床试验对于一款药物的正式上市具有决定性的意义。研究者表示,ZENITH20试验正在积极招募患者,数据日趋成熟,预计在进一步的研究中详细评估剂量变化对于治疗效果的影响。
"难治"亚型也有"克星",更多临床试验正在招募中
EGFR ex20ins突变亚型是非小细胞肺癌当中“凶名赫赫”的“难治型”,对于各类EGFR抑制剂不敏感,患者接受常规方案治疗的生存期远远短于其它EGFR亚型,因此其新药研发一直广受研究者与患者的重视。
除了此次报告中的波齐替尼,针对EGFR ex20ins这一靶标还有许多靶向治疗药物正在接受临床试验的“考验”,其中一部分试验也在招募患者。存在这一突变的患者,可以联系全球肿瘤医生网医学部(400-666-7998)了解试验详情,或进行入组评估。







































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城