非小细胞肺癌肺癌脑转移的治疗方法有哪些
脑转移是非小细胞肺癌肺癌发展到中晚期,最重要的表现与标志之一。考虑到脑这一部位的特殊性,全身治疗+局部治疗是脑转移治疗的基本框架,许多经典的案例也证实了这一点。
这一次,我们为大家总结了非小细胞肺癌脑转移最主要的一些治疗手段。从传统治疗“三驾马车”,到精准治疗时代的“靶向+免疫”,以及一些新兴的物理治疗“黑科技”,希望能够帮助到有需求的患者们。
传统治疗
在靶向治疗、免疫治疗等癌症精准治疗手段诞生之前,癌症治疗的“三驾马车”都曾经被用于非小细胞肺癌脑转移的治疗。这三类治疗手段各有“擅长领域”,但同样,也分别存在着一些无法治疗的“盲区”。不过总得来说,在精准治疗普及之前,这“三驾马车”为无数脑转移患者带来了希望,延长了生命。
1、手术
手术在非小细胞肺癌脑转移的治疗中应用比较少,仅局限于少数孤立性脑转移、且病灶位于非重要功能区的、身体状态与疾病控制均良好的患者。绝大多数脑转移患者完全无法满足手术苛刻的要求。
2、化疗
从药物本身来说,化疗药物通常很难通过血脑屏障;但由于发生脑转移时血脑屏障通常已经被癌细胞破坏,所以化疗药物也能够通过这些被破坏的区域进入颅脑内,发挥一定的疗效。
3、放疗
可以说,放疗是非小细胞肺癌脑转移以往最主要的治疗与控制手段。立体定向放疗(SRS)可以集中放射剂量,用于快速控制或消除局部的转移病灶;全脑放疗(WBRT)则是将剂量均匀分布,一方面缓解症状,一方面预防新病灶的产生。
非小细胞肺癌诊疗指南上也明确了放疗(以及手术等局部治疗手段)的使用时机与适用患者群体。
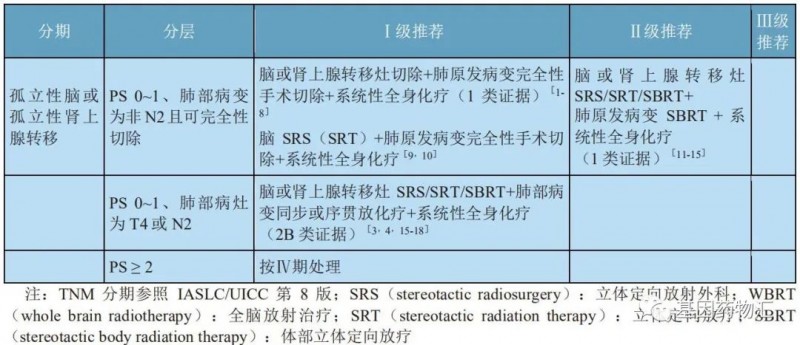
孤立脑或肾上腺转移非小细胞肺癌的治疗
对于非小细胞肺癌患者,在患者有脑部症状的情况下,如果脑部转移病灶数量较少(≤3个),则可以考虑手术切除方案、局部放疗(立体定向放疗)联合全脑放疗方案;如果脑部转移病灶数量较多(>3个),则基本不考虑手术治疗,主要采用局部放疗联合全脑放疗方案。
靶向治疗
如果患者没有严重的占位,或者脑疝的风险,或者其它严重的症状表现,那么对于脑转移的治疗来说,是否存在致癌驱动突变是非常重要的一个考量因素。
携带EGFR突变或ALK重排的患者发生脑转移的风险更大,可以达到50%~60%;ROS1阳性的风险稍微小一些,但是这种亚型也比较少。如果患者恰好是(包括但不限于上述三类)驱动基因突变的类型,那么很多新一代靶向治疗药物的全身治疗也能够取得不错的疗效。通常情况下,对于这些患者来说,全身治疗优于局部治疗。
1、EGFR
EGFR抑制剂,“上帝送给中国人的礼物”,重要性自然不必说。
我们曾经在之前的文章中提到的一个经典案例,就是由第三代EGFR抑制剂奥希替尼所创造的。患者治疗前,颅脑MRI检查提示,她头颅中大大小小的转移病灶数量超过20个。但在接受了仅仅5周的奥希替尼治疗之后,患者颅内的病灶,完全消失!
除了奥希替尼,其它EGFR抑制剂治疗脑转移病灶的疗效也非常出色。第一、二代EGFR抑制剂(吉非替尼、厄洛替尼、阿法替尼等),治疗颅内病灶的缓解率在60%~70%;第三代EGFR抑制剂(奥希替尼、阿美替尼、伏美替尼等),治疗第一二代药物耐药的患者,颅内病灶缓解率仍然高达60%~70%,控制率更是接近100%。
这说明,在某些特殊的情况下(比如患者可能很难耐受放疗,或颅内转移病灶数量过多等),可以考虑先使用药物治疗。如果患者对于药物的响应良好,很可能靶向药物的治疗能够为脑部放疗提供条件,甚至,部分患者有希望直接凭借药物治疗完全消除病灶。
2、ROS1/ALK
ROS1和ALK,非小细胞肺癌的两大“钻石突变”,对于整个治疗过程的价值更加明显。
许多驱动基因突变导致的肺癌,都是脑转移风险比较高的类型。因EGFR突变导致的非小细胞肺癌,发生脑转移的风险高达44%~63%;ROS1或者ALK突变的患者也有约30%~40%的风险。47%的ROS1阳性患者,以及33%的ALK阳性患者,首个、也是唯一一个发生进展的部位,就是脑。
我们曾经为大家分析过几个使用克唑替尼单药治疗,但逐渐发生为脑转移的患者。整体来说,这部分患者接受克唑替尼治疗,除了颅脑病灶以外的其它靶病灶控制都相当不错。但不论是初始存在脑转移的患者还是不存在脑转移的患者,最终癌细胞都会逐渐地向颅脑侵袭——这是一个克唑替尼“够不到”的地方,是这种方案的“致命弱点”,于是癌细胞非常“狡猾”地躲向了这里。
第三代药物劳拉替尼弥补了这一治疗上的“短板”。同时,另一款与克唑替尼同为第一代ROS1/ALK抑制剂的药物,我们熟知的ROS1/NTRK抑制剂恩曲替尼,也为脑转移患者的一线治疗,提供了有价值的解决方案。
临床试验当中,克唑替尼的颅内病灶缓解率大概是百分之十几,恩曲替尼的缓解率却高达79.2%!同时,脑转移患者的缓解持续时间也非常稳定,55%的患者缓解持续超过12个月。
3、MET
MET外显子14跳跃突变,简称MET ex14跳跃,患者发生脑转移的风险同样不低,大约在20%~40%,基本接近非小细胞肺癌脑转移的平均概率。
这是一个近几年热度正高的突变类型。一方面是因为几款近期上市的新药,让这类突变正式成为治疗性的靶标;另一方面则是庞大的患者需求。除了作为原发性致癌突变以外,MET突变还可能是EGFR、ROS1等多种靶向药物的耐药突变。
超过20%的EGFR突变型非小细胞肺癌患者因继发的MET异常而产生了耐药。一些研究显示,存在MET 14外显子跳跃突变的细胞,对于奥希替尼的敏感性降低了大约20倍,反馈于治疗当中,疗效自然显著降低,甚至导致耐药。
那么,MET突变的患者,如果发生了脑转移,接受靶向治疗的效果如何呢?
在特泊替尼(Tepotinib)的Ⅱ期VISION研究中显示,脑转移患者的颅内病灶缓解率为71.4%,虽然样本量稍微小了一点,但是当前的数据非常理想!
另外一项今年公布数据的临床试验中,一线接受卡马替尼治疗的患者,颅内病灶缓解率高达85.0%;而接受免疫检查点抑制剂治疗的患者中仅有1例实现颅内病灶缓解,缓解率为11.1%。
4、RET
RET同样是近几年热门的靶点之一,几款经典RET抑制剂对于脑转移病灶的治疗效果都比较理想。
其中,塞尔帕替尼(Selpercatinib,LOXO-292)治疗的颅内病灶缓解率高达91%,普雷西替尼(Pralsetinib,BLU-667)的颅内病灶缓解率也有56%。
5、KRAS
关于KRAS突变,大家可以看我们以前的文章《从“不可成药”到“多方围剿”,对抗KRAS突变的那些事儿》。
在KRAS G12C突变的脑转移患者中,Sotorasib(AMG-510)的颅内病灶缓解率为25%。
免疫治疗
免疫检查点抑制剂的诞生,成为了靶向治疗非常好的补充。一项统计学分析结果显示,PD-1抑制剂单药治疗脑转移的非小细胞肺癌患者,颅内病灶的缓解率为16.4%,控制率45%。虽然与靶向治疗动辄60%~70%的超高缓解率相比仍有很大的差距,但已经不算太低,是缺乏驱动基因突变、无法使用靶向治疗的患者不错的选择。
不过,值得注意的是,当免疫治疗与放疗联合应用的时候,发挥出的疗效将更加显著。
1、免疫+放疗,跨界"割"王
放疗的过程中,放射线会损伤癌细胞的DNA,进而导致癌细胞的死亡。目前,越来越多的研究证实,放疗与免疫治疗存在一定的协同作用,也就是说,当这两种疗法共同使用的时候,效果会比单独某一种疗法要更好。
在PACIFIC研究当中,验证了同步放化疗后序贯免疫治疗局部晚期肺癌的效果,患者的中位总生存期长达47.5个月,中位无进展生存期17.2个月;而不使用免疫治疗的患者,中位总生存期仅有29.1个月,中位无进展生存期5.6个月。
此外,放疗之后还可能出现特殊的“远隔效应”,即在患者接受了针对局部病灶的放射线照射之后,靶区之外的病灶、即没有接受过放射线照射的同源病灶,也会在结束治疗后的一段时间之后缩小甚至消失的现象。
这种现象产生的根源在于人体免疫力。在癌细胞因放射线照射死亡后,会裂解释放出一些原本被隐藏起来的、能被人体免疫细胞识别的“标志物”;而在照射中没有死亡的癌细胞也会发生一些特殊的变化,更容易被免疫细胞(尤其是其中T细胞)识别并攻击,成为免疫细胞“练手”的“活靶子”。
一项2015年发表于《柳叶刀》杂志上的研究发现,在晚期实体瘤患者接受局部放疗联合免疫治疗之后,多达27%的患者出现了远隔效应。而产生了远隔效应的患者,中位总生存期为20.98个月;没有产生远隔效应的患者,中位总生存期仅有8.33个月,两者之间差异非常显著。
物理治疗新"黑科技"
除了这些写在指南上的常规治疗手段,还有一些比较新兴的手段,或在常规手段之上有一些提升,或可以填补一些尚属空缺的领域,例如质子疗法和电场疗法。
1、质子疗法:从"粒子"提升放疗疗效
质子疗法属于放疗,是一种采用质子束取代目前临床上最常用的光子束(X射线)进行放射治疗的疗法。
质子释放的能量是远远大于普通放疗中所使用的光子的,光子放射的能量为4~18 MeV,质子放射的能量却可以达到70~230 MeV。
除能量强度外,由于粒子的重量不同,两种射线束还具有不同的特性。质子是相对较重的带正电的粒子,它们会在击中目标时停止。而X射线由光子组成,光子是几乎没有质量的粒子,因此它们会一直穿过身体,包括健康的组织。
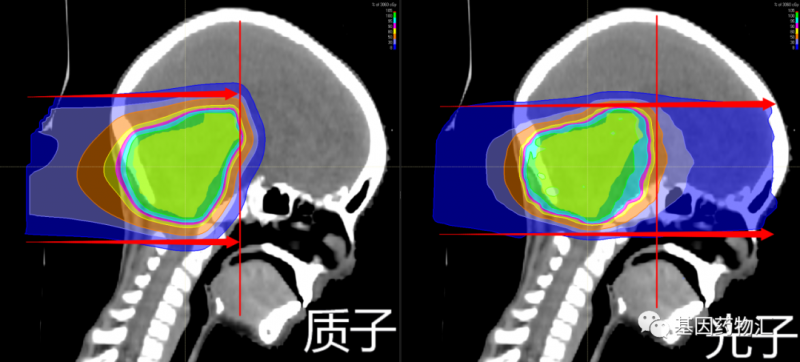
总的来说,质子疗法就像是常规放疗的“硬件升级版”,而三维、适形、调强等手段就像是放疗的“软件升级”。
基于质子和质子束本身的特点,比起传统的光子放疗,质子疗法具有一些独特的优势:放射剂量更集中于病灶部位、不良反应更少、安全性更好、二次肿瘤发生率更低、治疗过程中痛苦更少等等。这些特点都很有利于脑转移病灶的治疗。
2、电场疗法:正在崛起的新"抗癌黑科技"
电场疗法是一种全新的、物理性的抗癌手段。其原理简单来说,电场疗法是通过一些体外的设备,在我们希望处理的病灶部位创造一个电场,并通过电场力来影响癌细胞的分裂过程,让它在某个特定的过程当中停滞、最终死亡的治疗手段。
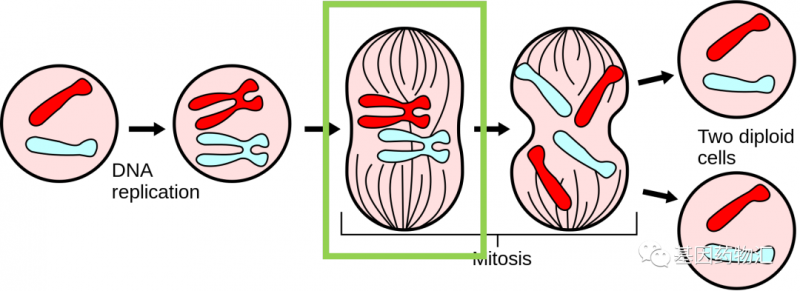
图为细胞有丝分裂正常过程示意图。绿色方框标记的位置,即电场疗法主要发挥效果的时间段。图中的黑色细线即纺锤丝,而纺锤丝是有电极性的,一端带正电、一端带负电,正常情况下将在细胞内环境的影响下朝向正确的方向。但在外界电场的作用下,纺锤丝进入了另一个完全不符合分裂期要求的环境里,被迫不断地随着电场掉转方向,无法维持正常结构,最终崩散。而染色体无法正常分离的时候,癌细胞也会走向死亡。
由于这样的治疗原理,电场疗法也具备了其它疗法所不具备的特殊性:这种疗法无创、副作用几乎只来源于设备与皮肤长时间接触或贴敷带来的皮肤不适或炎症;除此以外,电场疗法不会像各类药物治疗一样发生“耐药”,只要移除设备或断电就可以完全去除其对机体的影响。
综合来说,电场疗法是一类副作用小、疗效温和(并非如手术切除一样“立竿见影”实现“治愈”)但可以长期治疗或配合标准治疗一起使用的抗癌手段。
而电场疗法的副作用还与设备的选择有关:举例来说,美国研发的电场疗法主要依靠粘贴附着于患者身体,因此长期佩戴会有皮肤不适;而日本研发的电场疗法设备主要通过穿戴来附着于患者身体,皮肤副作用就更少。两者之间的临床试验数据也有差别,大家可以详细了解之后根据自身情况选择。
前段时间,我们为大家介绍了今年的ASCO大会上的一项新闻,电场疗法临床试验的新数据。在这项试验中,研究者将电场疗法加入非小细胞肺癌的标准治疗(免疫治疗与化疗)当中,结果令人振奋——患者的生存期延长近半(13.2个月 vs 9.9个月),且其中接受的标准治疗方案为免疫检查点抑制剂的患者生存期几乎翻倍(18.5个月 vs 10.6个月)。
对于非小细胞肺癌,尤其是缺乏驱动基因突变的非小细胞肺癌来说,免疫检查点抑制剂与化疗(多西他赛)是非常重要的标准治疗选择。在不改变标准治疗方案的前提下,仅仅是多增加一种治疗,疗效就能得到这么明显的提升,很多患者都表现出了兴趣。
总得来说,出现了脑转移、或脑转移风险大的患者,在治疗的时候应当注意这三点:
①根据患者的体力情况、转移病灶数量与部位、驱动基因突变情况等进行综合分析,选对治疗方案,并根据患者疾病的变化及时调整方案,更有针对性地抗癌;
②每当病情发生变化时,及时通过基因检测与影像学检查,准确把握当前的疾病特点,从而精准选择治疗方案;
③积极参与临床试验也是患者最终获益的根源之一。当现有的、已经获批上市的药物难以满足患者治疗需求的时候,临床试验将成为扭转困境的最有力帮手。

































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城