抗癌疫苗消灭残留癌细胞,3年零复发,终结肺癌、肾癌、肝癌、肠癌等卷土重来可能
对癌症患者而言,治疗后的每一次复查都如同一场“考验”,而癌症复发或转移堪称治疗后最令人担忧的“雷区”,始终揪着无数患者的心。即便手术成功,癌症仍可能因体内残留的少量癌细胞而卷土重来。面对这种反复出现的威胁,我们真的只能束手无策吗?
最新研究给出了新的希望:针对这些残留癌细胞研发的癌症疫苗,或许能有效阻止复发或转移。全球顶尖期刊《Nature》报道的一项新型癌症疫苗已通过功效验证,它正以前所未有的方式,为改写抗癌结局带来可能!
《Nature》力证:新抗原疫苗发"癌细胞通缉令",肾癌3年零复发,黑色素瘤4.6年全存活
近年研究发现,新抗原源于肿瘤的特异性突变,是抗肿瘤免疫的核心靶点,在激发机体抗肿瘤免疫中扮演着关键角色。而个性化癌症疫苗(PCV)正是基于新抗原研发的创新疗法:它能精准识别患者的癌症特征,诱导免疫系统对癌细胞的特异性表位产生免疫反应,如同向免疫系统发放“癌细胞通缉令”,助力其精准锁定并攻击癌细胞。
个性化疫苗3周激活免疫,肾癌患者3年零复发
2025年2月,国际顶尖学术期刊《Nature》报道了一项1期临床研究(NCT02950766)的惊艳数据——该研究针对9例晚期透明细胞肾细胞癌(RCC)患者(高风险且已接受完全切除手术),应用靶向新抗原的个性化癌症疫苗(PCV)展开治疗。
研究结果令人振奋:个性化癌症疫苗成功激发了患者体内的抗肿瘤免疫力。在中位随访40.2个月(约3.3年)期间,9名患者均未出现RCC复发,且持续保持无癌状态。更值得关注的是,疫苗仅用三周便诱发了显著免疫反应——9例患者中有7例检测出针对自体肿瘤的T细胞反应性,其T细胞数量更是飙升166倍。这种持久强劲的免疫应答,充分凸显了PCV作为肾细胞癌有效辅助治疗手段的巨大潜力。
▼Kaplan-Meier生存曲线图
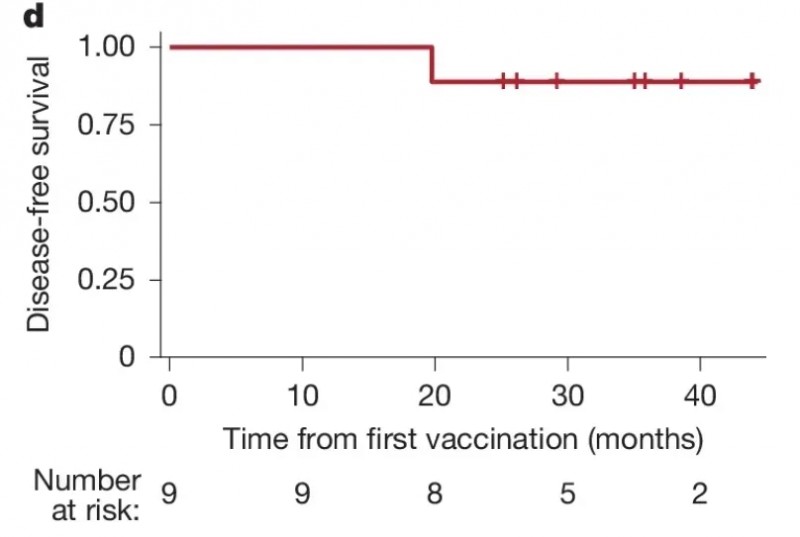
▲图源“nature”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
新抗原NeoVax疫苗续写抗癌传奇:黑色素瘤高危患者4.6年全存活,长期无进展
这并非新抗原疫苗首次展现疗效。早在2021年,《Nature》就曾报道过一项“应用NeoVax新抗原疫苗(每位患者最多可靶向20种个体化肿瘤新抗原),治疗黑色素瘤”的临床研究(NCT01970358)。共纳入8例IIIB/C期或IVM1b期高危黑色素瘤患者,并为其接种疫苗。
结果显示:中位随访55个月(约4.6年)时,所有患者均存活,其中6例未出现任何肿瘤进展迹象。值得注意的是,患者2和患者3在接种疫苗后,分别持续4.5年和4年检测到CD4⁺T细胞对已鉴定的非疫苗新抗原的应答。
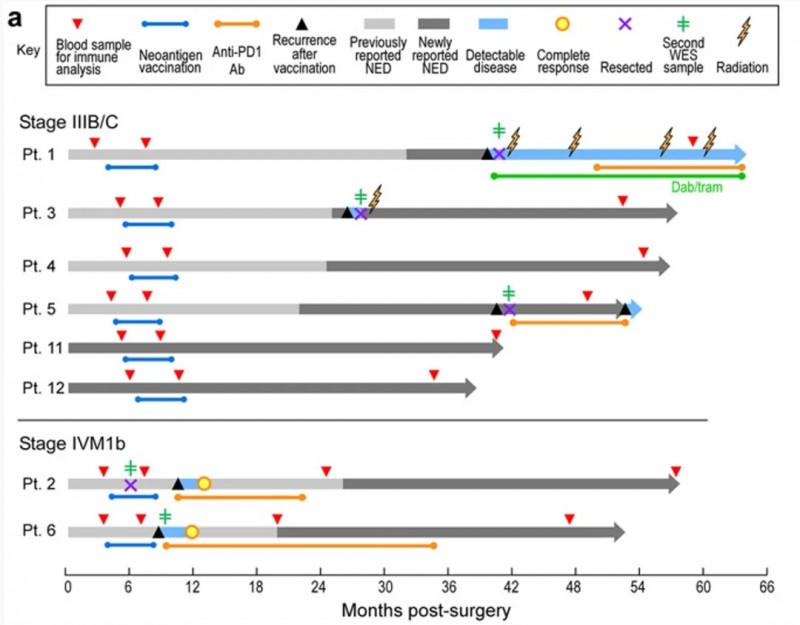
▲图源“nature”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
中国患者如何寻求癌症疫苗帮助
目前,癌症疫苗中临床疗效及预防复发效果较突出的是树突状细胞疫苗、mRNA癌症疫苗、古巴肺癌疫、个性化新抗原疫苗等。
1、树突状细胞(DC)疫苗:在日本、德国等,用于临床辅助治疗多种癌症,包括皮肤癌、肝癌、肺癌、肾癌、乳腺癌等,是癌症患者的新希望!
2、mRNA癌症疫苗:正在针对肺鳞癌、肝癌、结直肠癌、黑色素瘤、食道癌、三阴性乳腺癌、头颈部肿瘤等多款恶性实体瘤,开展临床研究。
3、古巴肺癌疫苗(CIMAvax-EGF):中国患者现无需出国,可通过医学部,向古巴医疗部门申请肺癌疫苗,以延长生存期,提高生活质量!
想寻求国内外癌症疫苗或其他治疗新技术帮助的患者,可先将治疗经历、病理报告、出院小结等资料,提交到医学部,进行初步评估或了解详细的入排标准。
587天无复发/无转移!树突状细胞疫苗与厄洛替尼为晚期肺腺癌按下"暂停键"
树突状细胞(dendriticcell,DC)作为关键的抗原提呈细胞,核心功能是激活机体抗癌免疫力,引导免疫系统精准摧毁癌细胞。
近期《医学病例报告杂志》刊载的一则病例令人振奋:一位无法手术的晚期肺癌患者,在接受树突状细胞疫苗与厄洛替尼联合治疗后,长达587天(约1.6年)期间,未出现任何复发或转移的迹象。
这位63岁的患者确诊为Ⅲb期(T2aN3M0)EGFR突变肺腺癌,未接受过化疗,且无ALK表达、PD-L1表达不足1%,因病情无法进行手术切除。随后,患者入组接受厄洛替尼联合WT1/MUC1-DC疫苗(经MHCII类限制性WT1肽和粘蛋白1肽冲击的树突状细胞)治疗。
治疗结果显示:通过CT及氟脱氧葡萄糖(FDG)-正电子发射断层扫描(PET)/计算机断层扫描(CT)监测,治疗前患者左下肺叶存在35mm×30mm的病灶;联合治疗237天后,肿瘤缩小至12mm,体积显著缩减65.7%;治疗321天时(已完成10次DC疫苗接种),计算机断层扫描未再检测到肿瘤,患者临床表现明显改善。更令人惊喜的是,截至统计时,这种肿瘤消失的状态已持续至少587天,期间未出现任何复发或转移迹象。
▼该患者DC疫苗联合治疗前、治疗后CT和PET/CT对比
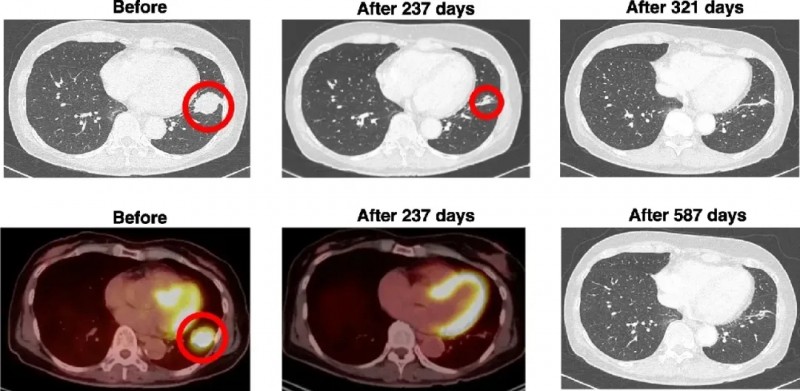
▲图源“BMC”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
BNT122 mRNA疫苗携20种新抗原,攻破实体瘤壁垒!多癌种响应率超30%,肾癌缩小10倍、直肠癌生存期超3年
BNT122(自基因cevumeran、RO7198457)是一款创新性个体化新抗原mRNA疫苗,其独特优势在于可依据每位患者肿瘤组织的特异性体细胞突变数据精准设计,通过刺激机体产生针对多达20种新抗原的T细胞反应,最终降低肿瘤复发风险、延长患者生存时间。
国际期刊《NatureMedicine》报道了该疫苗在1期GO39733临床研究(NCT03289962)中的振奋数据:研究共纳入213例局部晚期、转移性或复发性且无法治愈的恶性实体瘤患者。
结果显示:不同癌种均呈现积极响应:其中黑色素瘤(n=9)客观缓解率(ORR)达33.3%,非小细胞肺癌(NSCLC,n=10)ORR为10.0%,肾细胞癌(RCC,n=12)ORR为33.3%,尿路上皮癌(UC;n=11)ORR为18.2%。其中两例患者的治疗效果尤为亮眼:
其中一位肾癌患者(38号患者),入组前已接受包括纳武单抗在内的4种全身治疗,研究初期病情曾进展,后续却达到部分缓解(PR):其胸膜靶病变的最长直径总和(SLD)基线时为108mm,经癌症疫苗治疗13个月后缩小至10mm(详见下图),肿瘤显著缩小近10倍!
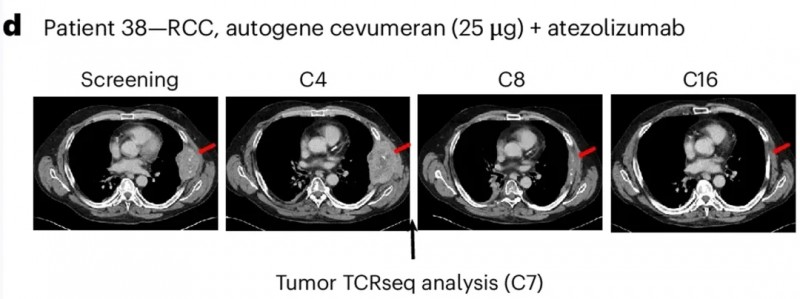
▲图源“nature”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
另一位微卫星稳定且PD-L1低表达的直肠癌患者(21号患者):经两线治疗后肺部仍有1.1cm靶病灶及非靶病灶。在接受9剂阿替利珠单抗+BNT122疫苗联合治疗后,患者奇迹般实现完全缓解(CR),缓解持续时间达8.2个月;截至数据统计时,其生存期已超过3年(40.7个月)(详见下图)。
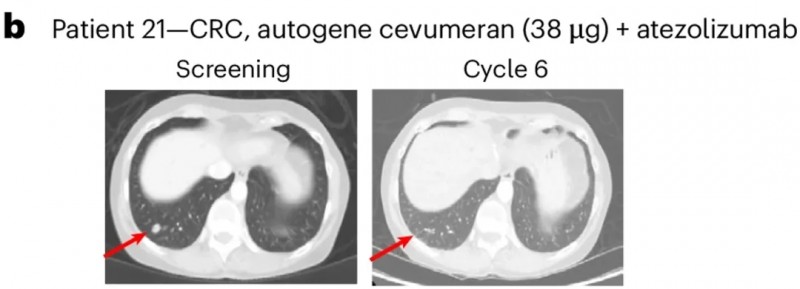
▲图源“nature”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
个性化DC疫苗+T细胞疗法筑牢肝癌防复发防线!50%患者2年无复发,71.4%免疫应答者零复发,生存期显著延长
《癌症免疫学研究》发表的一项II期临床研究(NCT03067493),首次探索了“个性化新抗原DC疫苗联合新抗原激活T细胞疗法,在肝癌术后防复发中的应用价值”。该研究共入组10例接受根治性手术或射频消融(RFA)的肝细胞癌(HCC)患者,术后均接受DC疫苗+个体化新抗原免疫细胞联合治疗。
结果显示:50%(5例)患者在治愈性治疗后2年内,肿瘤未出现复发(详见下图A),中位无复发生存期(DFS)长达18.3个月(95%CI:4.9-NA,详见下图B),较传统术后治疗显著延长。
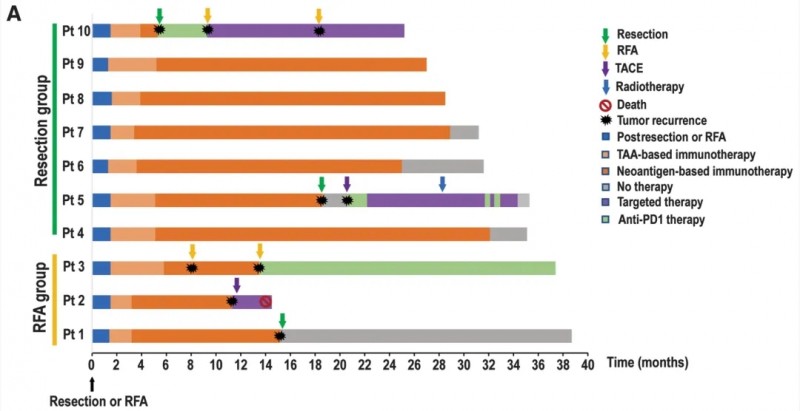
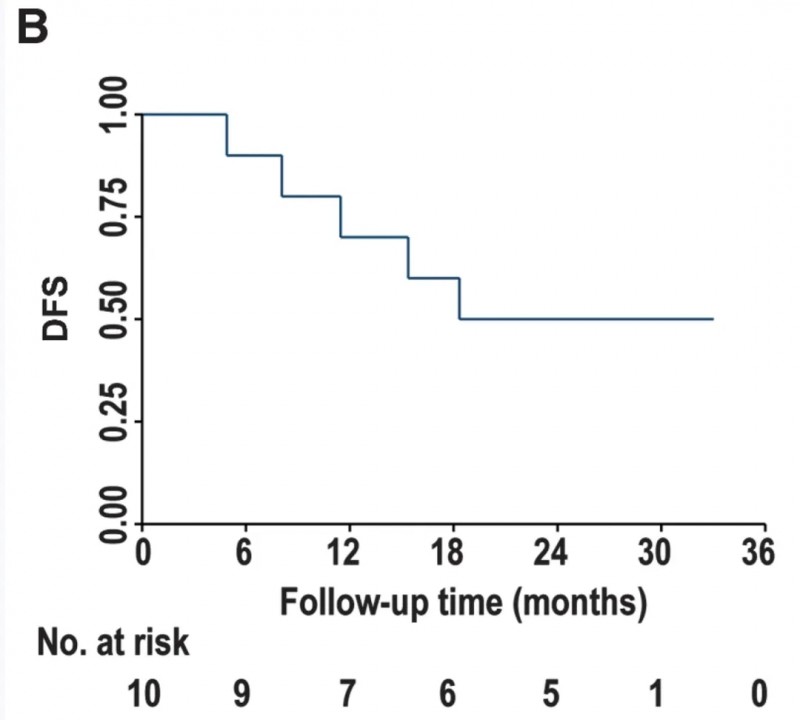
▲图源“nature”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
更重要的是,免疫应答与生存预后呈现强关联——有免疫应答患者的DFS显著长于无应答者(P=0.012),其中71.4%的免疫应答者在2年内保持无复发,而无免疫应答患者则全部复发(详见下图C)。
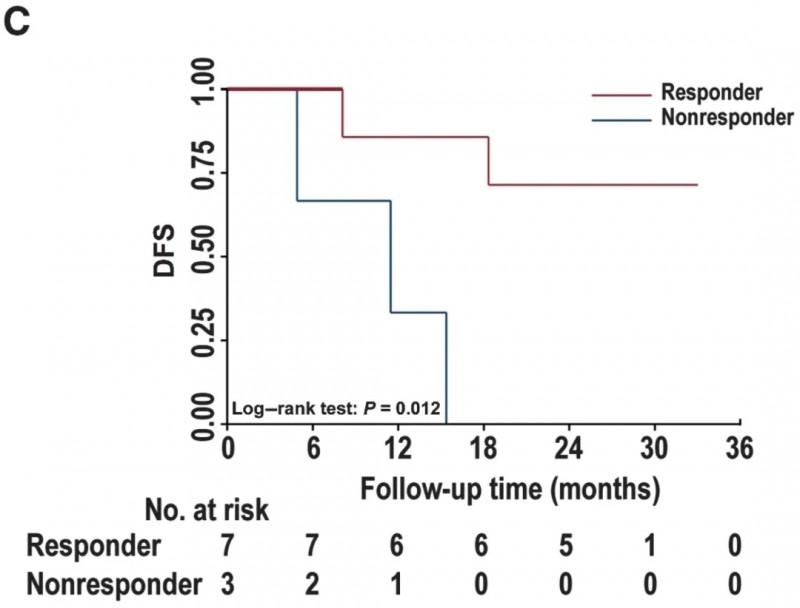
▲图源“nature”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
小编寄语
癌症疫苗历经数十年发展,已从基础研究逐步迈向临床应用,近年来更实现突破性进展——针对残留癌细胞的癌症疫苗,有望成为阻止癌症复发或转移的手段之一。
但小编仍然要提醒广大癌友,癌症作为一种高度突变的复杂疾病,单一治疗手段难以实现理想疗效。当前更优的治疗策略是:在权威医院的传统治疗(如手术、放化疗等)基础上,结合患者病情、个体特征、突变靶点及经济状况,联合靶向药、免疫细胞治疗(如CAR-T、TCR-T、TIL细胞疗法)、癌症疫苗、质子治疗、电场疗法等新型手段,从而巩固传统治疗效果、降低复发风险、提升生存质量、并延长生存期。
“打一针就能治疗癌症”的愿景虽仍需探索,但好消息是,我国目前正开展多款癌症疫苗的临床研究。对此感兴趣的病友,可将治疗经历、近期病理及影像学检查结果等,提交至医学部,进行初步评估或申请国内外抗癌专家会诊。
参考资料
[1]Braun DA,et al.A neoantigen vaccine generates antitumour immunity in renal cell carcinoma. Nature. 2025 Mar;639(8054):474-482.
https://www.nature.com/articles/s41586-024-08507-5
[2]Hu Z,et al.Personal neoantigen vaccines induce persistent memory T cell responses and epitope spreading in patients with melanoma. Nat Med. 2021 Mar;27(3):515-525.
https://pmc.ncbi.nlm.nih.gov/articles/PMC8273876/
[3]Kosumi T,et al.Dendritic cell vaccination in combination with erlotinib in a patient with inoperable lung adenocarcinoma: a case report[J]. Journal of Medical Case Reports, 2024, 18(1): 88.
https://jmedicalcasereports.biomedcentral.com/articles/10.1186/s13256-024-04363-z
[4]Lopez J,et al.Autogene cevumeran with or without atezolizumab in advanced solid tumors: a phase 1 trial[J]. Nature Medicine, 2025: 1-13.
https://www.nature.com/articles/s41591-024-03334-7
[5]Peng S,et al.Combination neoantigen-based dendritic cell vaccination and adoptive T-cell transfer induces antitumor responses against recurrence of hepatocellular carcinoma[J]. Cancer immunology research, 2022, 10(6): 728-744.
https://aacrjournals.org/cancerimmunolres/article/10/6/728/699035/Combination-Neoantigen-Based-Dendritic-Cell

































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城