肠癌化疗失败别放弃,树突状细胞(DC)疫苗治疗肠癌双线突围,生存期翻倍+54个月无进展
免疫检查点阻断(ICB)对微卫星不稳定(MSI)高转移性结直肠癌(mCRC)有效,但对微卫星稳定(MSS)患者收效甚微。而近年研究发现,自体树突状细胞(ADC)癌症疫苗可补充ICB,二者联合或产生协同效应:疫苗能刺激肿瘤抗原特异性细胞毒性T淋巴细胞,特异性识别清除癌细胞,将“冷”肿瘤转化为“热”肿瘤。
基于此,研究团队开展了一项I/II期多中心试验(含转化子研究),数据同步发表于《癌症免疫学/免疫疗法》,不仅首次揭示了治疗后代谢重新布线的机制,还证实Avelumab(抗PD-L1)联合ADC疫苗的组合安全且耐受性良好。
这一突破打破了MSS型mCRC治疗僵局,为经多线治疗的患者带来生存希望,也为这类“难治性”肿瘤免疫治疗开辟新路径!
自体树突状细胞(ADC)疫苗联合PD-L1抑制剂Avelumab,让MSS转移性结直肠癌生存期翻倍,中位OS达12.2个月
MSS mCRC肿瘤突变负担低,ICB单药最佳总体反应(BOR)不足5%,中位无进展生存期(PFS)2.2个月、总生存期5个月,6个月无进展生存率低于20%,治疗陷入瓶颈。
《癌症免疫学/免疫疗法》报道的这项单组I/II期多中心研究(含转化子研究),旨在评估Avelumab(抗PD-L1)联合自体树突状细胞(ADC)疫苗,对经至少2线化疗的微卫星稳定(MSS)转移性结直肠癌患者的疗效与安全性。该研究共筛选28例年龄≥18岁、组织学确诊MSS结直肠腺癌的患者,最终18例可评估治疗反应。
结果显示:4例患者病情稳定(22%),中位无进展生存期(PFS)为3.1个月(2.1–5.3个月),中位总生存期(OS)为12.2个月(3.2–23.2个月)。
总之,该联合疗法12.2个月的中位总生存期(OS),优于抗PD-1单药疗法的5个月及Avelumab与其他获批药物联合方案的10-11个月。其安全性良好但临床活性适中,且首次揭示了治疗后的代谢重新布线现象,这可能代表免疫疗法诱导的新型肿瘤脆弱性。
▲截图源自“springer”
DC疫苗+CAT联合疗法打破晚期十二指肠癌宿命,腹水清零并创造54个月无进展奇迹
除了前文报道的“自体树突状细胞(ADC)疫苗联合PD-L1抑制剂Avelumab治疗MSS转移性结直肠癌”的临床研究外,全球知名期刊《Cureus》还报道过一则震撼案例——WT1/MUC1-DC联合CD3激活T淋巴细胞(CAT)的过继细胞疗法(ACT),成功让晚期十二指肠癌患者肿瘤52个月无进展!
该患者为一位72岁男性,确诊为IV期原发性十二指肠腺癌(T3N2M1),伴远端淋巴结转移。他先接受胃空肠旁路手术,术后行S-1(口服嘧啶氟化物衍生药物)+奥沙利铂化疗,肿瘤虽有缩小但后续出现腹膜播散。二线伊立替康化疗启动后第二个月,腹膜播散、恶性腹水及恶病质迅速恶化,腹部CT显示大量恶性腹水及十二指肠周围大网膜脏脂肪征,化疗失败且无合适后续治疗方案,患者最终入组,并于2020年1月正式开始接受WT1/MUC1-DC(WT1和MUC1肽脉冲树突状细胞)+CAT疗法治疗。
治疗效果十分显著:治疗前腹部CT可见十二指肠周围明显扩张的大网膜(详见下图A箭头所示)、大量恶性腹水(详见下图B、C)。
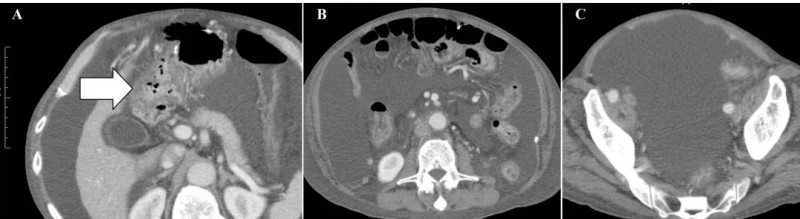
▲图源“Cureus”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
而在完成第6次治疗后,患者症状大幅改善。最终在第8次治疗后1个月,恶性腹水完全消失,腹胀、腿部水肿消退,食欲恢复,原发病灶与转移性淋巴结持续缩小,腹膜播散的影像学特征已不明显——腹腔内脂肪性粘稠组织大网膜消失(详见下图A),腹水消退(详见下图B),仅右侧腹股沟疝因之前大量腹水导致的腹压仍持续存在(详见下图C)。
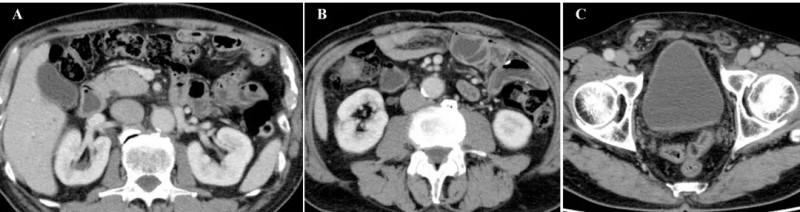
▲图源“Cureus”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
值得关注的是,在整个治疗过程中,患者未出现治疗相关严重副作用,且恢复正常活动。此后每数月接受该方案维持治疗,截至目前,首次给药后至少54个月内未再出现恶性腹水,肿瘤长期无进展!
小编寄语
树突状细胞(DC)作为体内唯一能激活初始T细胞的抗原提呈细胞,在免疫反应中占据核心地位。目前,DC疫苗虽多数仍处于早期临床试验阶段,但已在部分国家正式应用于临床。对于早期肿瘤患者,术后采用DC疫苗联合放化疗的辅助治疗方案,可通过清除残留癌细胞、形成免疫记忆,降低复发转移风险。
树突状疫苗在日本、德国等,用于临床辅助治疗多种癌症,包括皮肤癌、肝癌、肺癌、肾癌、乳腺癌等,是癌症患者的新希望!值得欣慰的是,如今我国也有多款癌症疫苗正在开展临床研究,这也意味着中国患者也有机会寻求这款抗癌新技术的帮助!
对目前治疗方案不满意,或想寻求树突状细胞疫苗等抗癌新技术帮助的患者,可将近期病理报告、影像学检查资料、治疗经历等,提交至医学部,进行初步评估。
参考资料
[1]Español-Rego M,et al.A Phase I-II multicenter trial with Avelumab plus autologous dendritic cell vaccine in pre-treated mismatch repair-proficient (MSS) metastatic colorectal cancer patients; GEMCAD 1602 study[J]. Cancer Immunology, Immunotherapy, 2023, 72(4): 827-840.
https://link.springer.com/article/10.1007/s00262-022-03283-5
[2]Yagawa Y,et al.Peritoneal Dissemination and Malignant Ascites in Duodenal Cancer Successfully Treated With Adoptive Cell Therapy Using WT1-and MUC1-Pulsed Dendritic Cells and Activated T Cells With No Adverse Effects: A Case Report[J]. Cureus, 2024, 16(11).
https://www.cureus.com/articles/308954-peritoneal-dissemination-and-malignant-ascites-in-duodenal-cancer-successfully-treated-with-adoptive-cell-therapy-using-wt1--and-muc1-pulsed-dendritic-cells-and-activated-t-cells-with-no-adverse-effects-a-case-report#!/

































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城