免疫治疗肿瘤效果好吗?2万+患者印证,主动出击才是王道,早期免疫疗法联合重塑多癌种预后
在不少癌症患者及家属的传统认知中,免疫疗法常被视为“最后一根救命稻草”——只有当化疗、放疗、靶向治疗等均宣告无效,患者与家属陷入山穷水尽之时,才会抱着“死马当活马医”的心态尝试这一疗法。
然而,近年来越来越多的大数据研究正在颠覆这一认知:免疫疗法并非只能用于“最后一搏”。事实上,若在癌症治疗的更早阶段介入,不仅能让患者获得更大获益,带来长期生存的更多可能!
打破“最后一搏”偏见!免疫疗法不只是“救命稻草”,早期使用更胜一筹
长期以来,临床实践中存在一种惯性思维:免疫疗法作为“后线治疗”更稳妥。这一观念的形成有其历史原因——免疫疗法发展初期,作为一项革命性的新技术,它最初获批的临床试验,大多针对的是传统治疗失败、已无药可用的晚期患者。在这种“绝境”下,免疫疗法依然能让一部分患者获得惊人疗效,这本身就证明了其强大的潜力。
但问题也随之而来:当患者在历经多轮治疗后,身体机能和免疫系统已被严重削弱,肿瘤负荷巨大,且可能产生了高度的异质性。此时,再强大的“免疫军队”也可能面临一个“烂摊子”——疲惫的T细胞、抑制性的肿瘤微环境,这些都大大限制了免疫疗法的效果。因此,随着循证医学证据的积累,这种“免疫疗法是最后一搏”的认知正在被彻底改写。
为何“先发制人”更有效
早期使用免疫疗法的优势,核心源于肿瘤微环境与患者免疫状态的“时间窗口”效应,具体体现在三方面:
1、肿瘤与微环境更易被攻克:早期肿瘤细胞数量少、异质性低,尚未形成强免疫抑制微环境,免疫细胞更易穿透肿瘤组织,高效清除癌细胞。
2、患者免疫系统状态更佳:治疗早期患者全身状况好,T细胞等免疫细胞数量足、功能健全,未被多次化疗耗竭,此时引入免疫疗法能更精准识别并攻击癌细胞,还易产生持久免疫记忆。
3、阻断逃逸+放大协同效应:早期介入可在肿瘤“免疫逃逸机制”成熟前将其阻断;同时,免疫疗法与手术、放疗等手段早期结合,能借助后者释放的肿瘤抗原“指引方向”,让免疫应答更具广度和深度,实现“1+1>2”的协同效果。
下图展示了美国国立研究所及剑桥大学团队,通过晶格层光显微镜技术拍摄到的场景:红色的T 细胞正与蓝色的癌细胞展开 “殊死搏斗”。
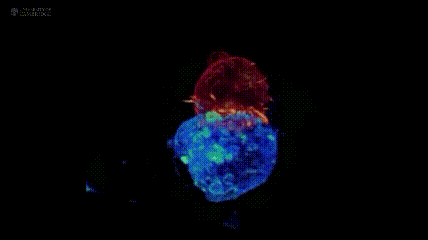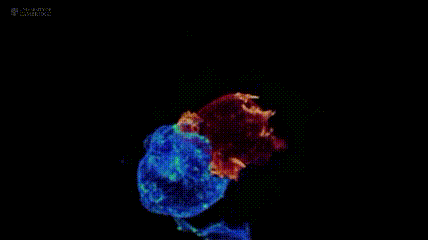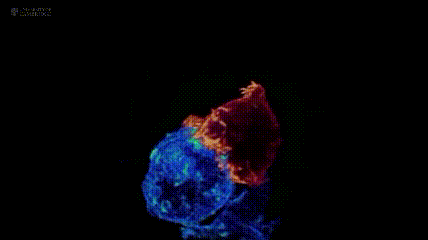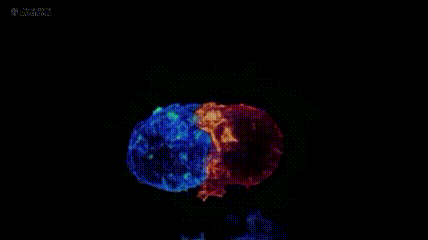
超2万患者生存曲线给出答案:免疫疗法早期介入激活抗癌最强战力
比如《JAMA肿瘤学》发表的一篇综述,分析了25项非小细胞肺癌临床试验的大数据(涉及超2万名患者),发现免疫疗法与靶向治疗的使用时机不同,生存曲线差异显著。
数据显示:免疫疗法组与化疗组的总生存期(OS)中位数分别为12个月和9个月(HR=0.69;95%CI:0.63-0.75),OS曲线在3个月后开始分离,且12、18、24个月时仍保持分离(详见下图)。
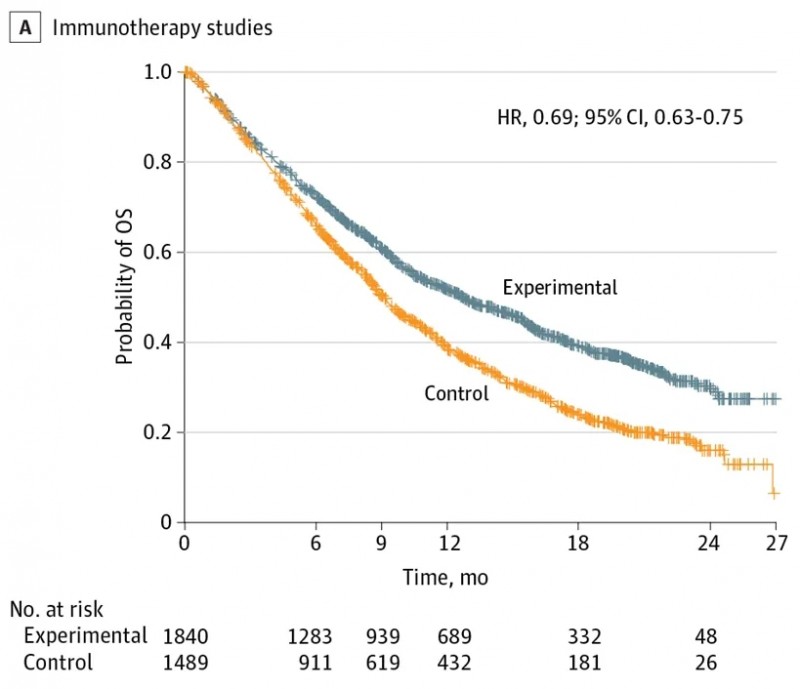
▲图源“JAMA”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
而靶向治疗组与对照组的OS曲线未出现分离,前者中位生存期为27个月(HR=0.98;95%CI:0.80-1.19,详见下图),这与化疗组向靶向治疗组交叉率高、疾病进展后生存期较长有关。
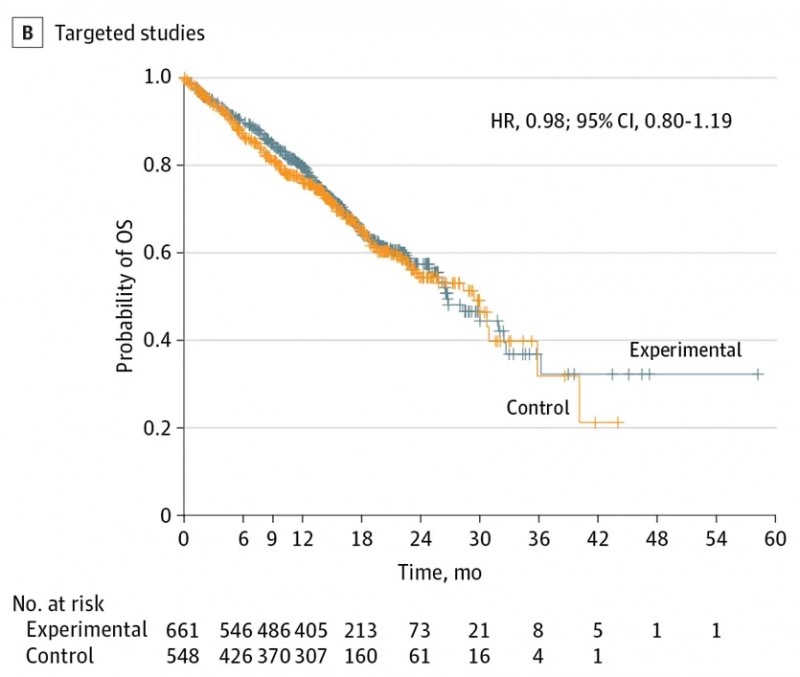
▲图源“JAMA”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:图中试验组(蓝色线)为“早期使用免疫疗法”,对照组(橘色线)为“后线使用免疫疗法”。
免疫疗法的“四大王牌”,从抑制剂/免疫细胞到癌症疫苗,精准攻坚各类肿瘤
常见的免疫疗法主要分为四大核心类型,覆盖临床常用与前沿应用方向(详见下表):
1、免疫检查点抑制剂(ICI):目前临床应用最广泛的免疫疗法。原理是解除肿瘤细胞对免疫细胞的“抑制刹车”,让T细胞等免疫细胞重新激活,精准攻击癌细胞。常见靶点包括PD-1、PD-L1、CTLA-4等,适用于多种实体瘤和血液肿瘤。
2、细胞因子治疗:通过注射免疫调节因子,调节机体免疫反应强度,增强免疫细胞的抗癌活性。常见药物包括白细胞介素、干扰素等,常与其他疗法联合使用,提升整体治疗效果。
3、过继性免疫细胞疗法:通过改造患者自身免疫细胞来增强抗癌能力的疗法。主要包括CAR-T细胞治疗(改造T细胞使其精准识别肿瘤抗原)、TCR-T细胞治疗(优化T细胞受体结合肿瘤抗原)、TIL细胞、NK细胞、CAR-NK细胞、γδT细胞疗法等,适用于多种血液肿瘤、部分实体瘤(如肺癌、脑瘤、肝癌、胰腺癌、胃癌、肠癌、黑色素瘤等)。
4、癌症疫苗:通过接种疫苗激活患者自身免疫系统的“记忆功能”,让免疫系统主动识别并清除肿瘤细胞。分为预防性疫苗(如HPV疫苗,预防相关癌症发生)、治疗性疫苗(针对已发生的肿瘤,如DC细胞疫苗、mRNA疫苗、古巴肺癌疫苗等),需结合肿瘤抗原特征定制。
▼常见免疫疗法的核心信息对比表
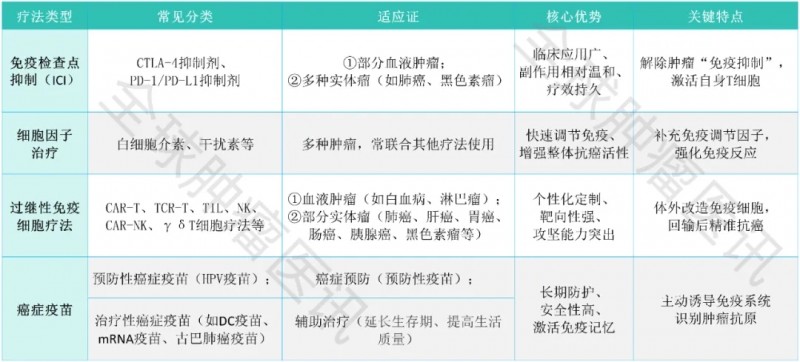
1+1>2!免疫疗法联手传统治疗,为患者筑牢长期生存防线
近年来,多项临床试验与真实世界研究,为免疫疗法的早期应用提供了坚实数据支撑,覆盖肺癌、黑色素瘤、胃癌等多个高发癌种。此外,它还能与传统治疗联合使用,高效清除残余肿瘤细胞,进而显著延长患者生存期,发挥“1+1>2” 的协同治疗优势。
术后联用CAR-NK细胞疗法!助复发性胶质母细胞瘤患者创近3年生存奇迹
全球知名期刊《神经肿瘤学(Neuro-Oncology)》近期发表了一项Ⅰ期临床试验数据,聚焦CAR-NK细胞治疗复发性HER2阳性胶质母细胞瘤(GB)。9例可评估疗效的患者,在复发手术期间接受了手术腔边缘注射CAR-NK细胞治疗。
结果显示:9例入组患者的中位总生存期(OS)达31周,中位无进展生存期(PFS)为7周;其中2例出现假性进展的患者,OS分别长达98周和135周,PFS均为37周(详见下图)。
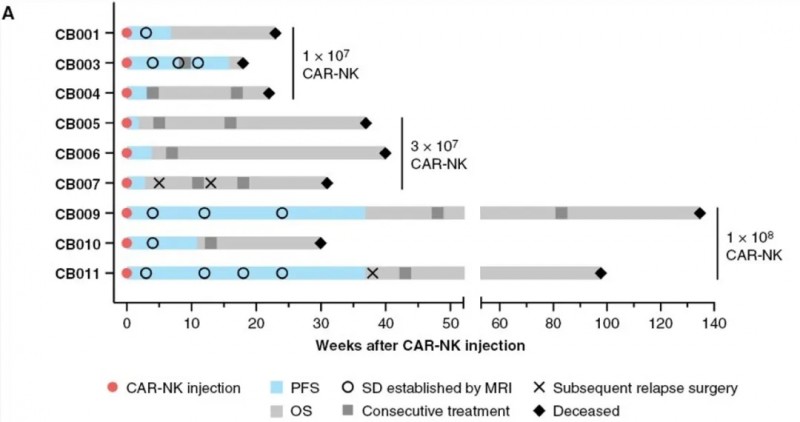
▲图源“Neuro-Oncology”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
此外,56%的患者在复发手术联合7~37周CAR-NK治疗后达到病情稳定(SD)。值得注意的是,2例患者在注射部位出现假性进展,提示存在治疗诱导的免疫反应。MRI检查显示,CAR-NK注射后第12周,患者切除边缘附近出现斑点状对比增强,且该现象在后续几周内自行消失,推测与诱导的免疫反应相关,无需额外治疗(详见下图)。
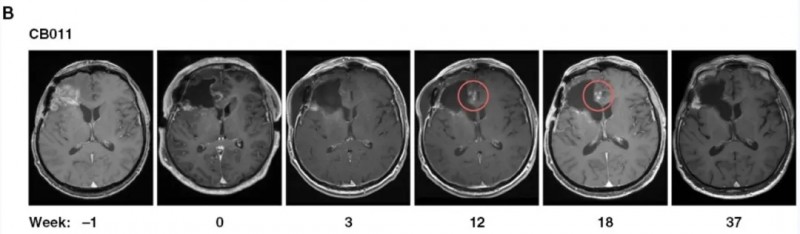
▲图源“Neuro-Oncology”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
NK细胞联合曲妥珠单抗,让耐药晚期HER2阳性乳腺癌实现长期病情稳定
《临床癌症研究》曾报道一项“自体NK细胞联合曲妥珠单抗治疗HER2阳性乳腺癌”的Ⅰ期临床试验振奋数据。该研究共纳入19例18~75岁、对标准治疗耐药的HER2阳性晚期乳腺癌患者,均接受这一联合治疗方案。
结果显示:6例患者达到病情稳定(SD),缓解持续时间均≥6个月(范围6~12个月)。
值得关注的是,其中1例55岁转移性激素受体阳性+HER2阳性乳腺癌患者还实现了部分缓解(PR):该患者既往已接受抗HER2治疗、激素疗法及多种化疗,经连续2个周期联合治疗后达PR,且这一状态持续至第8周期(详见下图)。此外,该患者的肿瘤标志物CA-153水平显著下降,治疗前为146.8,治疗第5周期降至75.4,治疗结束时仍稳定在76.6。

▲图源“AACR”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
TIL细胞联合PD-1疗法,精准狙击复发性宫颈癌,10周完全缓解
全球知名期刊《BMJ Journals》曾报道一则振奋人心的案例(临床试验编号:NCT04766320):一名复发性宫颈癌患者经TIL细胞治疗后实现完全缓解(CR)。
该患者为52岁女性,2019年5月确诊IB3r期宫颈癌,随即接受根治性子宫切除术联合盆腔淋巴结清扫术。术后病理分期升级为IIIC1p期(盆腔淋巴结受累),后续完成4个周期紫杉醇脂质体联合奥沙利铂化疗。17个月后,核磁共振成像(MRI)提示膀胱复发,患者接受部分膀胱切除术,术后继续辅助化疗,同时留存肿瘤切除物用于制备TIL细胞。入组本研究后,患者依次接受环磷酰胺静脉输注、TIL细胞回输及PD-1抗体治疗。
疗效数据十分亮眼:TIL细胞输注6周(42天)后,T1WI影像显示病灶显著缩小(黄色箭头标注),首次临床评估提示患者无发热、体重减轻等异常症状,体格检查未触及浅表淋巴结肿大;依据RECISTv1.1标准,输注10周后正式确认患者达到完全缓解(CR,详见下图)。

▲图源“BMJ journals”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
WT1-DC联合化疗为晚期肺癌患者续命,病灶近乎消失+PFS超1.5年
《Cureus》杂志近期报道了一例肺癌治疗突破性案例:一名69岁男性患者确诊为右肺中叶IV期鳞状细胞癌,确诊时已发生多发性骨、肝及双侧肾上腺转移,且因身体状况无法耐受手术与放疗。此后患者采用WT1树突状细胞疫苗(WT1-DC)+卡铂AUC6+紫杉醇的化疗方案联合治疗。
治疗成效十分显著:患者无进展生存期(PFS)超577天,期间体能状态良好,可正常生活。其癌胚抗原(CEA)曾一度持续上升,后续经雷莫芦单抗+多西他赛联合治疗后降至5.9。影像检查显示,治疗前PET-CT提示全身广泛转移;治疗第479天复查时,仅右肺(直径1.0cm)及肝脏(直径1.7cm)残留两处转移灶,其余病灶均明显改善。此外,胸部CT结果显示,治疗第114天肺部原发病灶已近乎消失;第213天虽出现局部复发,但第338天时,原发及复发病灶均显著缩小。
▼该患者WT1-DC治疗前后全身PET-CT对比

▲图源“Cureus”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
▼该患者WT1-DC治疗前后胸部CT图像对比

▲图源“Cureus”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
临床启示:免疫疗法需“早规划、早评估”,开启“主动抗癌”模式
免疫疗法的核心价值已从“挽救晚期”转向“早期干预”——在肿瘤尚未深度抑制免疫系统、患者身体机能完好的阶段激活免疫应答,既能实现对肿瘤的精准打击,更能达成长期控制目标。这要求我们对免疫疗法建立正确认知,做到早规划、早评估。
免疫疗法“前后夹击”:术前狙击+术后防复发,开启双线抗癌模式
1、术前新辅助:抗癌“奇兵”显威力:手术前开展新辅助免疫治疗,不仅能缩小肿瘤、降低手术难度,更能提前激活全身性免疫应答,清除潜在转移灶。研究显示,接受该治疗的患者,病理学完全缓解率(pCR,即手术切除组织中无癌细胞)大幅提升,长期预后更优。
2、术后辅助:防复发“防线”再加固:对于III期非小细胞肺癌等术后高复发风险患者,术后辅助免疫治疗可显著降低肿瘤复发与死亡风险。它能在体内存在微小残留病灶时,调动免疫系统开展“全面清扫”,将复发苗头扼杀在摇篮里,真正实现从“治已病”到“防复发”的跨越。
免疫疗法需“早规划、早评估”
1、术前评估是前提:通过PD-L1检测、TMB(肿瘤突变负荷)、MSI-H/dMMR等生物标志物检测,精准筛选最适合早期免疫治疗的患者,为后续治疗铺路。
2、个体化方案是核心:结合肿瘤分期、病理类型及患者身体状况,灵活选择“新辅助免疫”“辅助免疫”或“免疫联合治疗”模式,实现针对性治疗。
3、长期随访是保障:免疫治疗的获益具有长效性,需通过定期影像学检查、免疫功能评估,及时发现并处理免疫相关肺炎、结肠炎等潜在不良反应。
小编寄语
免疫疗法的“早期价值”被揭示,不仅是治疗手段的革新,更是癌症治疗理念的升级。它告诉我们:癌症治疗不应等到“走投无路”才尝试新方法,而是要在疾病进程的更早阶段,利用科学证据为患者选择最优方案。随着更多临床研究的开展和治疗技术的进步,相信免疫疗法将在早期癌症治疗中发挥更大作用,为更多患者带去长期生存的希望。
但也想提醒广大癌友:癌症作为一种高度异质性、极具侵袭性的疾病,目前仅靠单一疗法往往难以达到理想治疗效果。因此,建议癌症患者尤其是早期患者,既要积极配合医生完成规范治疗,治疗后也不可掉以轻心,需遵医嘱定期复诊,同时通过饮食调理、生活方式优化、免疫功能维护等方式,最大程度降低术后复发或转移风险。若不幸出现复发或转移,更要做到早发现、早干预,积极对接国内外新型抗癌技术,与癌抗争,永不言弃。
若对当前治疗方案存疑,或希望获取国内外抗癌新药、新技术支持,患者可将近期影像报告、病理检查结果、治疗经历等资料,提交至医学部,由专业团队详细评估病情,或协助申请国内外抗癌专家会诊,寻求抗癌新药/新技术的帮助。
参考资料
[1]Blumenthal G M,et al.Milestone analyses of immune checkpoint inhibitors, targeted therapy, and conventional therapy in metastatic non–small cell lung cancer trials: A meta-analysis[J]. JAMA oncology, 2017, 3(8): e171029-e171029.
https://jamanetwork.com/journals/jamaoncology/fullarticle/2632112
[2]Burger M C,et al.Intracranial injection of natural killer cells engineered with a HER2-targeted chimeric antigen receptor in patients with recurrent glioblastoma[J]. Neuro-oncology, 2023, 25(11): 2058-2071.
https://academic.oup.com/neuro-oncology/article/25/11/2058/7155851?login=false
[3]Guo J, Luo N, Ai G, et al. Eradicating tumor in a recurrent cervical cancer patient with autologous tumor-infiltrating lymphocytes and a modified lymphodepleting regimen[J]. Journal for Immunotherapy of Cancer, 2022, 10(2).
https://jitc.bmj.com/content/10/2/e003887
[4]Yagawa Y,et al.Peritoneal Dissemination and Malignant Ascites in Duodenal Cancer Successfully Treated With Adoptive Cell Therapy Using WT1-and MUC1-Pulsed Dendritic Cells and Activated T Cells With No Adverse Effects: A Case Report[J]. Cureus, 2024, 16(11).
https://www.cureus.com/articles/308954-peritoneal-dissemination-and-malignant-ascites-in-duodenal-cancer-successfully-treated-with-adoptive-cell-therapy-using-wt1--and-muc1-pulsed-dendritic-cells-and-activated-t-cells-with-no-adverse-effects-a-case-report#!/

































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城