100%控瘤+4年无癌生存!国研TIL细胞疗法亮相2025 ESMO+关键Ⅱ期获批!攻克肺癌/肝癌/肉瘤等
2025年11月17日,华赛伯曼研发的国研新型TIL疗法FAST-TIL(HS-IT101)获国家药监局药审中心(CDE)批准开展晚期黑色素瘤关键II期临床试验,成为国研TIL疗法领域的重大里程碑!
此前2025 ESMO年会上,该疗法I期黑色素瘤突破性临床数据一经公布便引发广泛关注:多名患者实现持续疾病缓解(CR/PR),数据截止时中位随访超5个月,位无进展生存期(mPFS)仍未达到,疾病控制率更是高达100%!这一兼具里程碑意义与亮眼疗效的突破,彰显了国研免疫疗法的硬核实力,更为晚期患者带来了新的希望与选择!

▲图源“华赛伯曼官微”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
ORR最高66.7%+DCR 100%!国研FAST-TIL凭硬核疗效闪耀欧洲肿瘤盛会,助改写晚期黑色素瘤治疗格局
2025年9月《肿瘤学年鉴》报道了“自体肿瘤浸润淋巴细胞FAST-TIL(HS-IT101)联合低剂量IL-2,治疗晚期实体瘤”的I期临床试验(NCT06342336),并公布了黑色素瘤亚组分析数据。截至2025年2月,该亚组共纳入8例对免疫检查点抑制剂(ICI)耐药的晚期黑色素瘤患者(5男、3女),含1例皮肤型、5例肢端型及2例黏膜型;患者先接受低剂量非清髓性预处理(LD-NMA,2例)或中剂量方案(MD-NMA,6例),再行TIL细胞输注+皮下注射IL-2治疗。
结果显示:总客观缓解率(ORR)达50%(4/8),其中MD-NMA组ORR高达66.7%(4/6),含1例完全缓解(CR)、3例部分缓解(PR)。

▲截图源自“ESMO”
随着随访延长,临床数据持续更新。2025年10月17-21日欧洲肿瘤内科学会(ESMO)年会上,该疗法I期黑色素瘤临床试验数据首次全球公布,展现出亮眼疗效。
结果显示:截至2025年10月,10例完成治疗及至少一次肿瘤评估的受试者中,4例确认疾病缓解,包括1例达到完全缓解(CR)、3例达到部分缓解(PR),初始客观缓解率(ORR),疾病控制率(DCR)达100%,显著优于美国已上市同类产品AMTAGVI(ORR31.4%、中位无进展生存期mPFS 4.2个月);中位随访5个月时,mPFS仍未达到。此外,在安全性方面,所有入组患者均未发生ICU入住或死亡事件,TIL治疗相关不良反应短期内均已恢复,表现出良好的安全性。
▼黑色素瘤受试者FAST-TIL(HS-IT101)治疗后靶病灶总和(SOD)变化
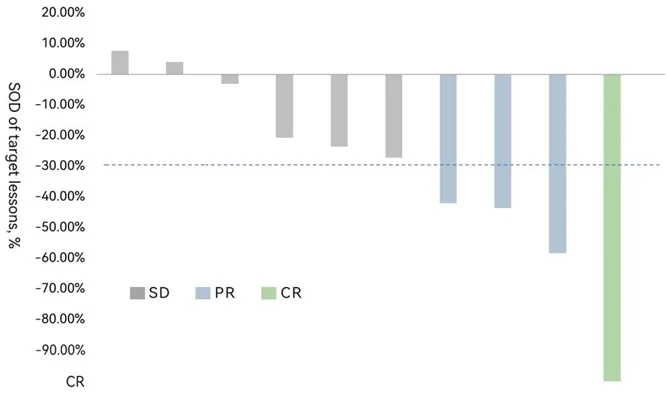
▲图源“华赛伯曼官微”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
综上,FAST-TIL(HS-IT101)通过多项关键性创新,有效破解了当前TIL细胞治疗取材难、风险高、价格高的临床痛点,其注册临床数据充分验证了技术突破的核心临床价值。
TIL细胞联合抗PD-1疗法,为化疗耐药/转移性骨肉瘤带来"治愈"级希望,80%病情受控,1年总生存率突破60%
骨肉瘤是最常见的恶性骨肿瘤之一,主要影响儿童和青少年,发病高峰年龄约20岁。目前,约70%的非转移性骨肉瘤患者经综合治疗后可长期生存,但转移性患者病灶进展迅速且易对化疗耐药,因此迫切需要寻求针对这类患者(尤其化疗耐药人群)的新型治疗策略,以改善预后。
近年研究表明,TIL疗法或为骨肉瘤治疗的有效方向:从骨肉瘤中提取的TILs可穿透肿瘤微环境,对同种异体肿瘤细胞产生细胞毒性;同时,抗PD-1疗法的疗效依赖肿瘤微环境中的TILs,因此两者联合或对转移性骨肉瘤具有潜在抗肿瘤作用。基于此,《免疫学研究杂志》报道了一项相关临床研究,旨在探索过继性TIL联合抗PD-1疗法(纳武利尤单抗)对化疗耐药转移性骨肉瘤患者的预后改善效果,该研究共纳入60例患者,并给予联合治疗。
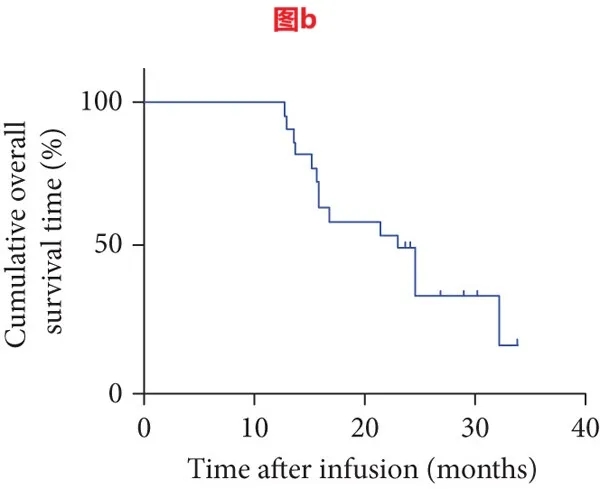
结果显示:患者整体客观缓解率(ORR)达36.67%(22/60),其中2例奇迹般获得完全缓解(CR)、20例获部分缓解(PR),疾病控制率(DCR)高达80%(48/60);截至2020年2月最后一次随访,10例患者仍存活,中位无进展生存期(mPFS)为5.75个月(详见下图a),中位总生存期(mOS)为13.6个月(详见下图b),1年无进展生存(PFS)率为25%(95%CI:13%,37%),1年总生存(OS)率更是高达60%(95%CI:50%,72%)。
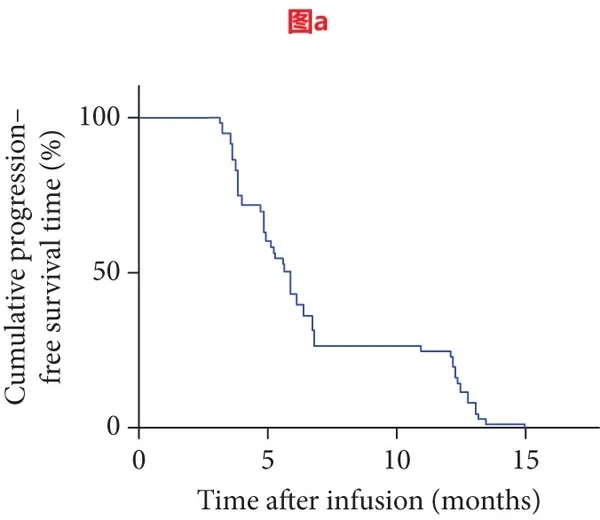
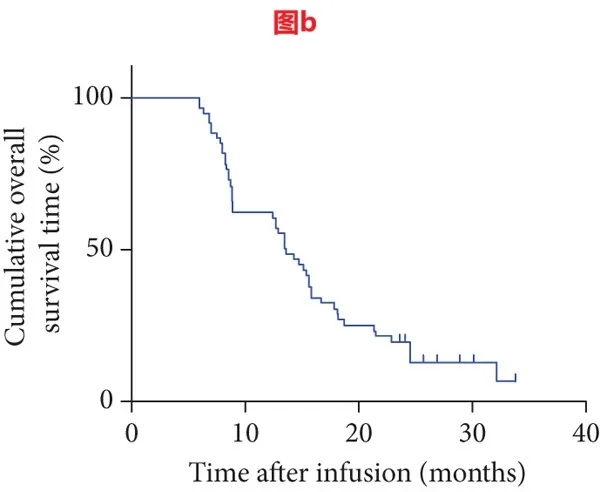
▲图源“J Immunol Res”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
值得关注的是,22例CR/PR患者的疗效更显著,其mPFS达8.85个月(详见下图a)、mOS达23.7个月(详见下图b),且20例PR患者中8例在末次随访时仍存活。
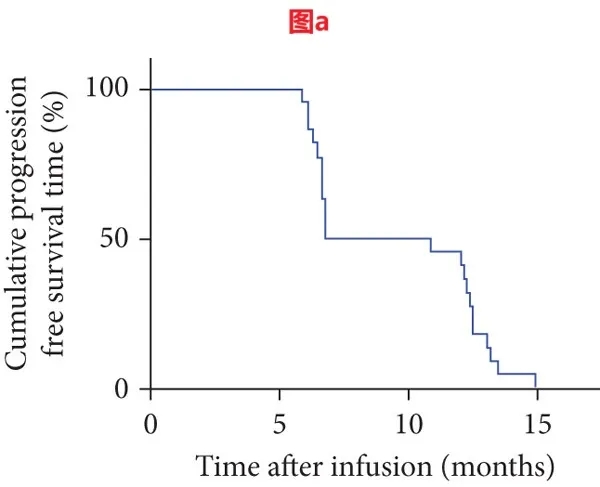
▲图源“J Immunol Res”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
值得一提的是,两例典型CR案例的情况值得广泛关注,截至数据统计时止,两例患者均存活:
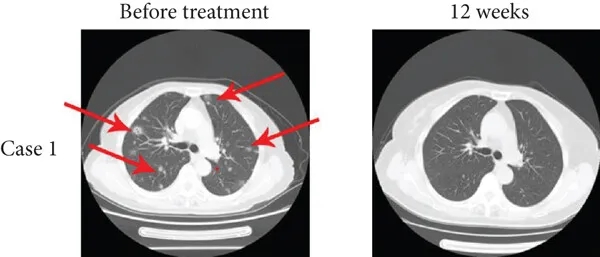
其中1例为一位15岁男性肺转移患者,在接受TIL疗法联合抗PD-1疗法12周后,达到完全缓解(CR),多发性肺转移灶消失(详见下图a),中位无进展生存期(PFS)为15个月。
▲图源“J Immunol Res”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
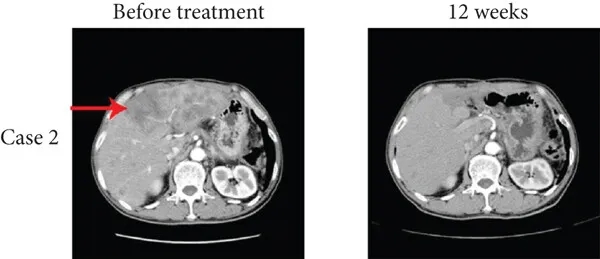
另一例为20岁男性肝转移患者,经12周TIL联合纳武利尤单抗治疗后,达到完全缓解(CR),肝转移灶消失(详见下图b),中位无进展生存期(PFS)为12.1个月。
▲图源“J Immunol Res”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
全球首创!TIL三联疗法缔造晚期肝癌生存奇迹:突破4年生存大关、2年持续无瘤
近日,国际权威期刊《肝癌》报道了两例全球首创“TIL+PD-1+AI”三联疗法治疗晚期肝癌的成功案例:两名患者目前分别生存超48个月和24个月,无需后续抗肿瘤治疗,已回归正常生活。
患者1为一例49岁男性,因肝细胞癌破裂入院。上腹部CT示左肝叶多发病灶(最大71×48mm),左侧门静脉癌栓形成;肺部CT检出多发结节,甲胎蛋白(AFP)超60,500ng/mL,确诊为乙型肝炎病毒(HBV)相关性肝细胞癌(BCLCC期)。该患者入组I期临床试验(NCT03658785)后,先接受左半肝切除术,术中获取肿瘤组织用于TIL培养;后续依次接受淋巴细胞清除方案(环磷酰胺+氟达拉滨)、TIL细胞回输、白细胞介素-2(IL-2)治疗及两次托珠单抗注射。
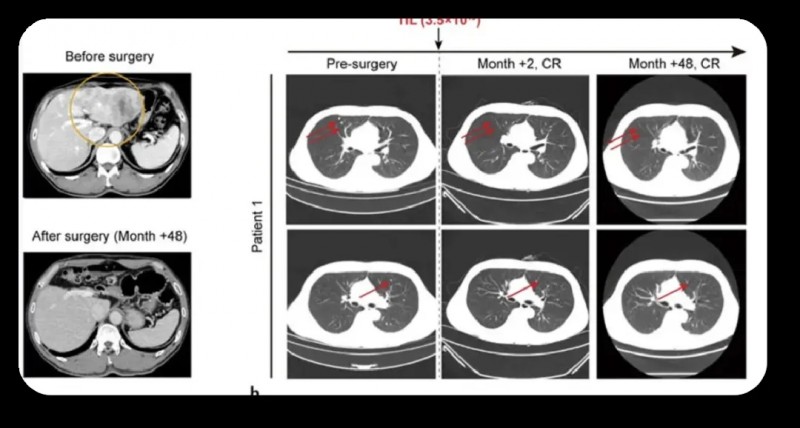
结果显示:肝切除术后2个月,所有肺转移灶完全消退,截至目前随访48个月(4年),患者持续无瘤生存(详见下图a、b)。
▲图源“Liver Cancer”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
患者2为一例67岁女性,因肝癌破裂出血接受经肝动脉栓塞术后1周入院。CT示肝左叶147×79mm混合信号肿块,双肺多发散在结节(右肺中叶最大18mm),甲胎蛋白(AFP)14,529ng/mL,确诊为HBV相关性肝细胞癌(BCLCC期)。该患者入组后接受姑息性左半肝切除术,肿瘤组织经29天培养获得TIL细胞;后续依次接受淋巴细胞清除治疗、自体TIL细胞单次输注、IL-2治疗及特瑞普利单抗治疗(共18个疗程)。
结果显示:肝切除术后1个月肺转移灶出现进展(右肺结节增大至25mm);但经TIL联合抗PD-1治疗后,术后10个月肺病灶完全消退,截至随访24个月,患者持续无瘤生存(详见下图c、d)。
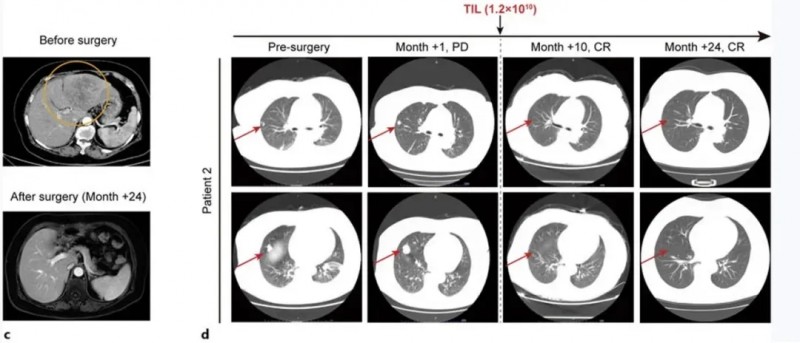
▲图源“Liver Cancer”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
Lifileucel TIL疗法以"更高缓解率+更持久疗效"完胜多西他赛,疾病控制率高达71.8%
Lifileucel是一款肿瘤浸润淋巴细胞(TIL)疗法,IOV-LUN-202二期临床研究(NCT04614103)的最新中期结果显示,Lifileucel TIL疗法在既往接受过治疗的非鳞状非小细胞肺癌(NSCLC)患者中,展现出持久疗效。
结果显示:中位随访时间达25.4个月,患者中位缓解持续时间(mDOR)尚未达到(详见下图)。
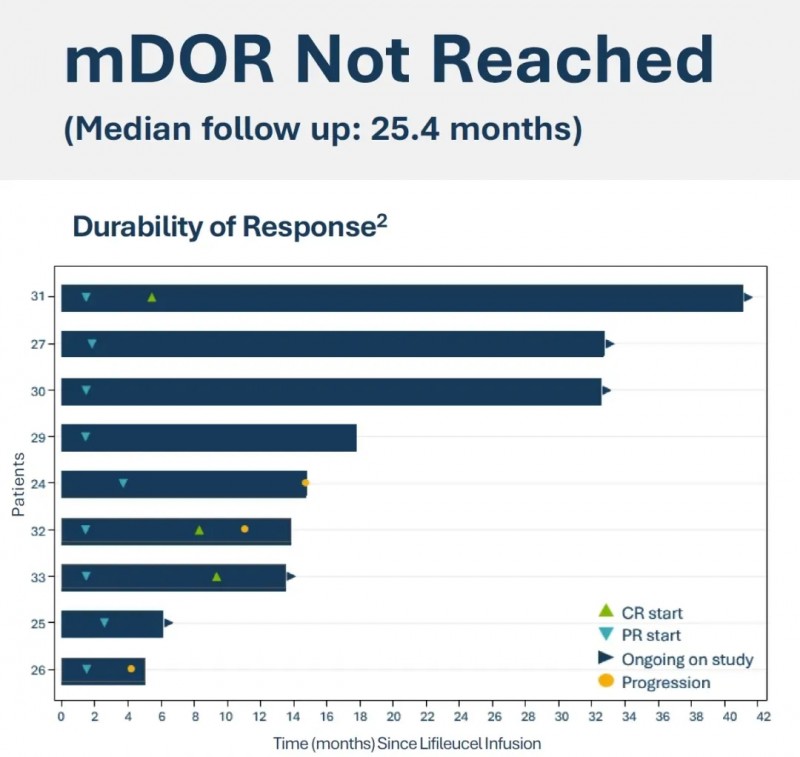
▲图源“Iovance”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
经中心审查标准评估的前39例晚期非鳞状NSCLC患者中,疾病控制率(DCR)高达71.8%,客观缓解率(ORR)达25.6%,包括2例完全缓解(CR)、7例部分缓解(PR)及1例待确认部分缓解(详见下图)。
值得一提的是,与标准治疗药物多西他赛相比,Lifileucel优势显著:多西他赛用于同类患者的ORR仅12.8%、mDOR为5.6个月、总生存期12.3个月,且无完全缓解病例;而Lifileucel不仅缓解率更高,疗效持久性也远超前者,为改善晚期非鳞状NSCLC患者预后提供了新潜力。
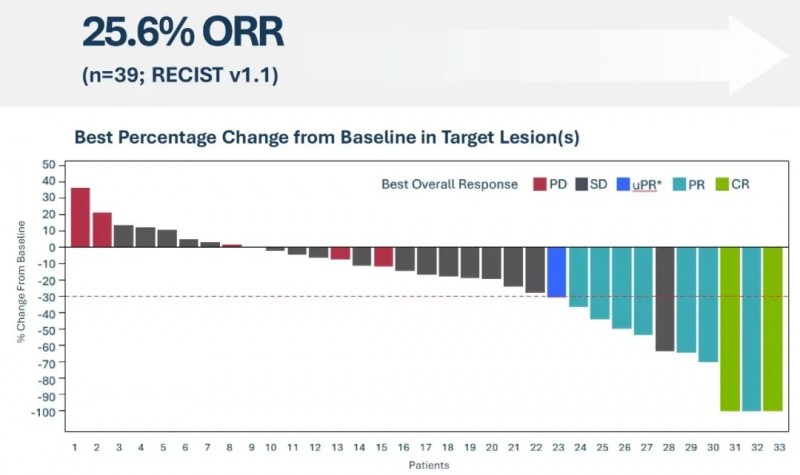
▲图源“Iovance”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
“看到既往接受过治疗的NSCLC患者能获得如此显著的缓解率和持久疗效,令人振奋。这类患者目前治疗选择有限,尚无任何疗法能达到这般效果”。
——德国德累斯顿大学医学博士
马丁・沃姆克(MartinWermke)
小编寄语
肿瘤浸润淋巴细胞(TIL)疗法自1988年首次应用于临床以来,已走过30余载的发展历程。相较于其他免疫细胞疗法,TIL疗法独具将患者自身肿瘤组织“变废为宝”的神奇功效,堪称实体瘤治疗领域当之无愧的抗癌黑科技。它既适用于早期癌症患者,可有效预防肿瘤的复发与转移;又能作为晚期患者的挽救性治疗手段,为癌症患者带来一线生机。
值得关注的是,TILs细胞数量会随着肿瘤的进展而逐渐减少,并且在术后接受辅助性治疗(如放疗、化疗)时,不仅癌细胞会受到杀伤,体内的免疫细胞也可能受到影响。因此,建议患者务必珍惜这或许仅有一次的宝贵抗癌机会。在术前应积极与主治医师进行沟通,尽可能地保留新鲜的肿瘤标本组织,并联系专业机构对TIL细胞进行分离和冻存,做到未雨绸缪。
想寻求TILs疗法帮助或了解TILs细胞制备或冻存更多信息的患者,可将治疗经历、近期影像学检查及病理报告等资料,提交至医学部,进行初步评估获了解详细的入排标准。
参考资料
[1]Jiang Y,et al.1652P A phase I clinical trial of autologous tumor-infiltrating lymphocytes FAST-TIL (HS-IT101) with low-dose IL-2 for the treatment of advanced solid tumors: Subgroup analysis of melanoma[J]. Annals of Oncology, 2025, 36: S979.
https://www.annalsofoncology.org/article/S0923-7534(25)03200-4/fulltext
[2]Zhou X,et al.Retrospective analysis of adoptive TIL therapy plus anti‐PD1 therapy in patients with chemotherapy‐resistant metastatic osteosarcoma[J]. Journal of Immunology Research, 2020, 2020(1): 7890985.
https://onlinelibrary.wiley.com/doi/10.1155/2020/7890985
[3]Xia T,et al.Autologous Tumor-Infiltrating Lymphocyte Infusion plus Anti-Programmed Cell Death Protein 1 Therapy to Cure Advanced Hepatocellular Carcinoma following Palliative Hepatectomy. Liver Cancer. 2025 Feb 20;14(4):497-505.
https://pmc.ncbi.nlm.nih.gov/articles/PMC12360740/

































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城