TIL细胞疗法联合溶瘤腺病毒长期疗效亮眼,抗癌成功活过4年,为肺癌、黑色素瘤、妇瘤等点亮希望
2025年11月4日,《癌症免疫治疗杂志》报道了TUNINTIL1期临床试验结果:采用TILT-123溶瘤腺病毒联合肿瘤浸润淋巴细胞的创新方案治疗难治性转移性黑色素瘤,展现出显著长期疗效,患者中位总生存期达447天!
这一突破为深陷抗癌困境的患者点亮希望,推动难治性肿瘤免疫联合治疗迈出关键一步。更让我们坚信,未来会有更多患者从中受益,在抗癌之路上迎来新的生机!
ICI难治性黑色素瘤迎低毒高效新方案:溶瘤病毒+TILs强强联合控病率47%,中位总生存447天,最长CR超4年
开篇提及的这项研究(NCT04217473)共纳入17例免疫检查点抑制剂(ICI)难治性黑色素瘤患者,包含8例皮肤型、5例黏膜型、4例葡萄膜型,这些患者既往接受过1-7线治疗。入组后接受了TILT-123溶瘤腺病毒的静脉联合瘤内注射,该病毒经基因工程改造,可在癌细胞中选择性复制并产生肿瘤坏死因子(TNF)与白细胞介素-2(IL-2),以此替代毒性较强的预处理及后处理方案。
结果显示:PET成像评估中,总体疾病控制率(DCR)达47%(7/15),完全或部分代谢缓解率为27%(4/15),其中最高剂量组缓解率达40%;依据RECIST1.1标准评估,客观缓解率(ORR)为11.7%(2/17),疾病控制率(DCR)为35%(6/17)。患者中位总生存期(OS)为447天,6例患者生存期超600天,另有1例黏膜黑色素瘤患者实现完全缓解,且持续时间已超4年。
综上,TILT-123联合肿瘤浸润淋巴细胞(TILs)治疗ICI难治性黑色素瘤,不仅展现出良好的安全性,更取得了令人鼓舞的疗效——既成功规避了高毒性预处理方案,还实现了持久缓解,对难治性非皮肤亚型黑色素瘤同样有效。

▲截图源自“BMJ”
TIL疗法用自身免疫利刃,精准斩杀癌细胞
肿瘤浸润淋巴细胞(TIL)疗法是过继性免疫细胞疗法的重要类型,其核心是从患者肿瘤样本中采集浸润淋巴细胞,经体外培养扩增后回输体内,依托自身免疫系统实现对癌细胞的精准杀伤。
该疗法的临床应用需遵循以下规范步骤:首先,从转移性皮肤黑色素瘤患者的活检样本中,分离出自然浸润到肿瘤组织内的淋巴细胞;随后在实验室中对这些淋巴细胞进行培养和扩增,核心目标是富集并激活具有肿瘤抗原特异性的Tc细胞与Th1表型淋巴细胞(具体过程见图2);扩增完成后,将大量活化的淋巴细胞联合高剂量IL-2一同输注至患者体内;而在TIL输注前,患者需先接受非清髓性淋巴细胞清除方案,为后续治疗创造条件。
▼TIL疗法的实施流程示意图
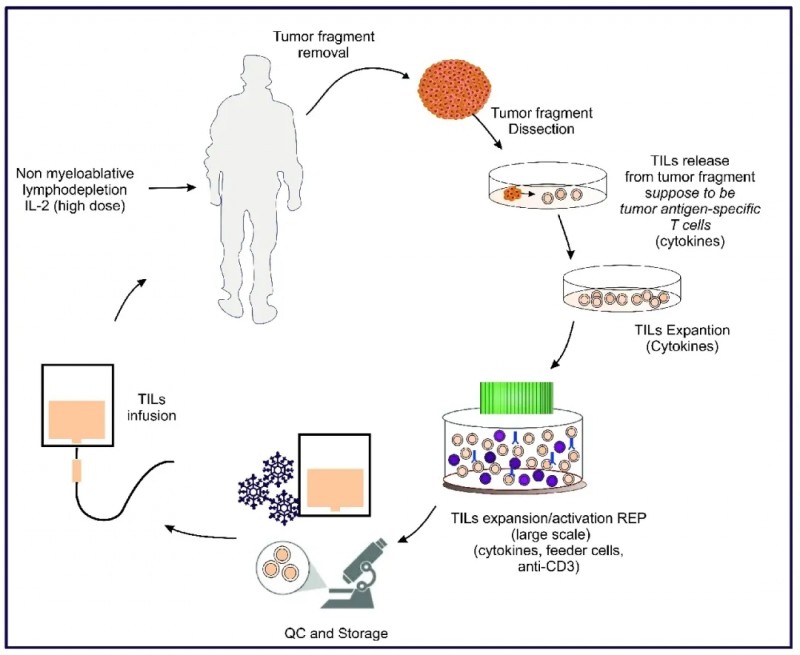
▲图源“MDPI”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
全球首款非病毒载体TIL疗法GC203,用68.8%年生存率+83.3%疾病控制率,为卵巢癌患者续写生命华章
GC203是我国自研的全球首款非病毒载体基因修饰TIL细胞疗法,以颠覆性创新重塑卵巢癌治疗格局。2024年4月,其获国家药品监督管理局(NMPA)临床研究批件;同年,Ⅰ期临床数据在全球顶级医学盛会美国临床肿瘤学会(ASCO)大会惊艳亮相。
该研究纳入18例可评估疗效的复发性卵巢癌患者,入组患者病情复杂:转移灶平均3.3个(1-9个),靶病灶平均直径58.7mm(13-146mm);且均为多线治疗失败患者,此前平均接受2.5线化疗,已用过免疫检查点抑制剂、PARP抑制剂等前沿疗法,病情均未得到有效控制,遂入组接受GC203治疗。
结果显示:6个月总生存(OS)率高达75.6%(57.4%~99.6%),12个月OS率为68.8%(49.3%~95.9%),中位无进展生存期(PFS)达5.5个月(范围:1.0-14.1个月)。经研究者评估,客观缓解率(ORR)为33.3%(95%CI:16.3%~56.3%),疾病控制率(DCR)更是高达83.3%(95%CI:60.8%~94.2%)。其中2例患者更是奇迹般实现完全缓解(CR),4例达到部分缓解(PR),9例维持病情稳定(SD)(详见下图)。
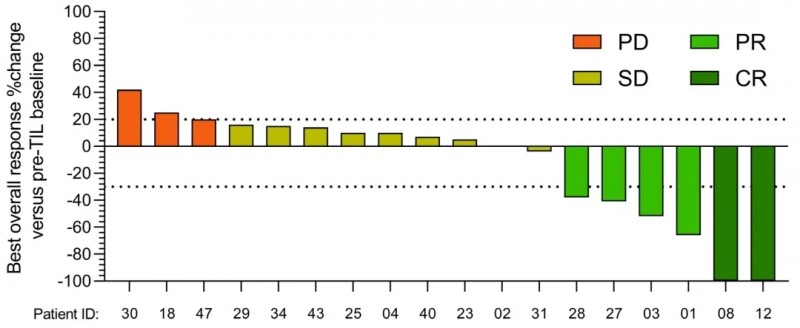
▲图源“JUN CELL官网”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
典型案例中,一位卵巢子宫内膜样癌患者入组前经化疗、PARP抑制剂等5种全身治疗,病情仍恶化。在接受GC203TIL细胞治疗后,奇迹正式上演:肝脏和肺部转移灶显著缩小,次月复查靶病灶缩小66%,达部分缓解(PR)标准,为患者重燃生存希望!
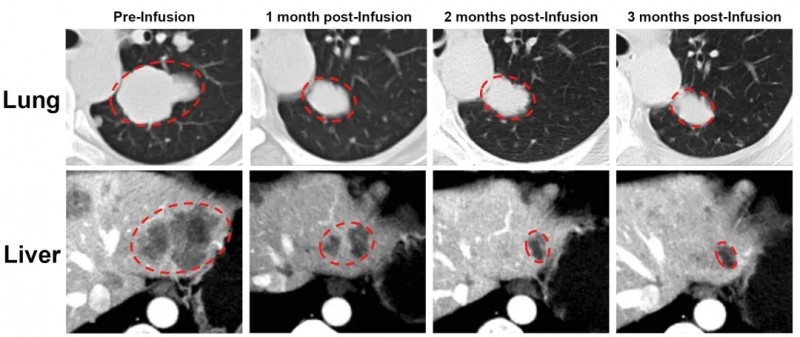
▲图源“JUN CELL官网”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
告别高强度清淋!全球首款天然TIL疗法GC101暴击实体瘤,缓解率超35%,最长无瘤生存超3年
GC101是上海君赛生物研发的全球首款无需清淋预处理、无需IL-2注射的天然TIL疗法,它摒弃了传统TIL疗法所需的高强度清淋化疗(如环磷酰胺+氟达拉滨)及IL-2输注,有效降低感染、器官功能损伤等治疗相关毒性。患者仅需在普通病房即可完成治疗,大幅简化了TIL细胞治疗流程,同时显著提升了疗法的安全性与可及性。2022年4月,获国家药监局批准进入Ⅰ期临床。
临床表现亮眼:GC101用于治疗肺癌、黑色素瘤、宫颈癌等晚期实体瘤时,客观缓解率(ORR)超35%,其中4例患者实现完全缓解(CR),最长无瘤生存时间已超3年。
值得关注的是,其中一位晚期肺腺癌案例,该患者确诊为肺腺癌,同时伴随淋巴结、胸膜、骨转移,经GC101治疗后,靶病灶缩小36%,成功达到部分缓解(PR),且治疗24周时仍维持缓解状态。下图展示了该患者在接受GC101 TIL回输治疗前,以及治疗6周、12周、18周、24周的CT影像对比(详见下图)。
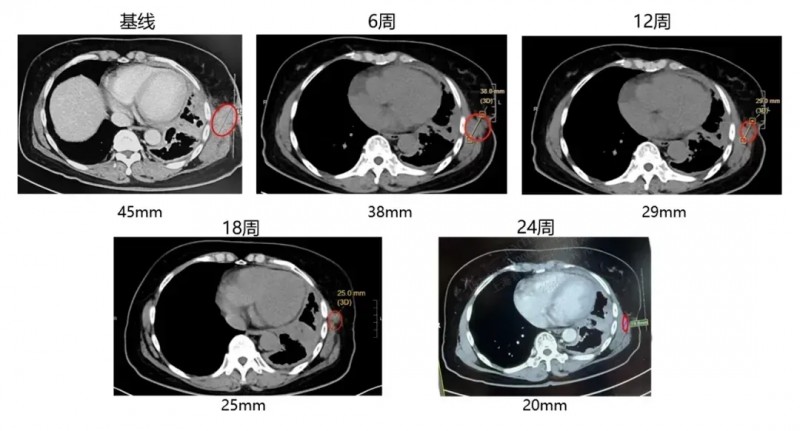
▲图源“JUNCELL”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
TILs联合抗PD-1疗法精准狙击化疗耐药转移性宫颈癌,开启25.8个月超长生存期,疾病控制率62.5%
对于PD-L1阴性且微卫星不稳定性(MSI)低表达的转移性宫颈癌患者,单用抗PD-1治疗疗效欠佳,这类患者亟需更有效的治疗方案。过继性T细胞疗法(ACT)作为新兴的癌症治疗方式,其原理是通过体外扩增具有抗肿瘤活性的治疗性T细胞,再将其全身输注给患者。
一项应用“肿瘤浸润淋巴细胞(TILs)+抗PD-1抗体,联合治疗化疗耐药宫颈癌”的临床研究,共纳入80例一线化疗耐药后出现持续性转移的宫颈癌患者,中位年龄为45岁(范围:35-65岁),入组后均接受TILs联合纳武利尤单抗治疗。
结果显示:客观缓解率(ORR)达25.0%(20/80),其中4例实现完全缓解(CR),16例达到部分缓解(PR);另有50例患者(62.5%)实现疾病控制(DCR)。截至2020年7月随访结束,患者整体中位无进展生存期(PFS)为6.1个月,总生存期(OS)为11.3个月。尤为突出的是,20例获得客观缓解(CR/PR)的患者,中位PFS达12.8个月,中位OS更是长达25.8个月,其中7例部分缓解患者在随访期间仍存活。
值得关注的是两例完全缓解的典型患者:
病例1为一例35岁患者,治疗前伴随肺转移,接受免疫联合治疗3个月后,多发性肺转移灶完全消失(详见下图,黄色箭头所示),PFS达15.4个月。
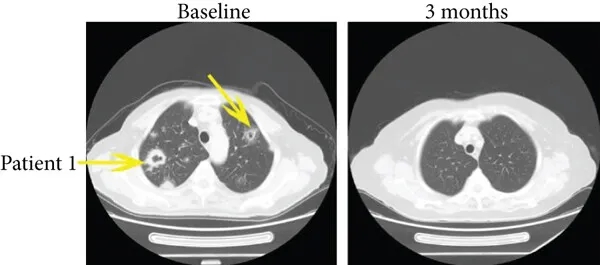
▲图源“J Immunol Res”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
病例2为一例50岁患者,治疗前存在肝转移,经4个月免疫联合治疗后,多发性肝转移达到完全缓解(详见下图,黄色箭头所示),PFS达10.9个月。
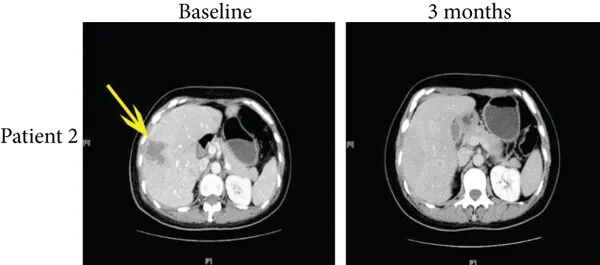
▲图源“J Immunol Res”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
中国TILs产品百家争鸣,多款在研产品启动临床
过去,TIL疗法这一先进治疗技术长期被医疗发达国家掌握,不少病友在等待中抱憾离去。让中国病友振奋的是,“天价”疗法不再遥不可及——我国已成功研发多款针对实体瘤的TIL细胞疗法,如前文提及的GC101、GC203均是其中代表。除此之外,还有多款在研TIL细胞疗法剑指实体瘤:
1、GT101(沙砾生物):2022年4月22日,沙砾生物研发的GT101注射液获国家药监局(NMPA)临床试验默示许可(受理号:CXSL2200061),是我国首个获批临床的TIL细胞产品,在黑色素瘤、非小细胞肺癌、宫颈癌等实体瘤治疗中展现良好效果。
2、GT201(沙砾生物):沙砾生物第二款TIL产品GT201,于2023年7月11日获NMPA临床试验默示许可,也是我国首款进入注册临床试验的基因编辑型TIL产品,适用于复发或转移性实体瘤。
3、C-TIL051(西比曼生物):西比曼生物研发的C-TIL051,2022年10月新药IND申请获美国FDA批准,用于PD-1抗体难治或复发性晚期非小细胞肺癌(NSCLC)治疗,还适用于黑色素瘤、宫颈癌、头颈部鳞状细胞癌等泛癌种实体瘤。
4、BST02(百吉生物):百吉生物研发的BST02,2023年10月26日Ⅰ/Ⅱ期临床试验申请获美国FDA批准,用于各类肝癌治疗,是全球首个进入临床阶段的肝癌TIL细胞产品。
5、ZLT-001(智瓴生物):智瓴生物自主研发的ZLT-001注射液,2023年1月28日获NMPA临床试验默示许可(受理号:CXSL2200552),是华南地区首个获批临床的TIL产品,适用于晚期复发或转移性宫颈癌。
6、HV-101(天科雅生物):天科雅生物与杭州厚无生物医药联合研发的HV-101注射液,2023年1月29日获NMPA临床试验默示许可(受理号:CXSL2200574),用于晚期复发或转移性实体瘤治疗。
7、HS-IT101(华赛伯曼):华赛伯曼研发的自体天然加强TIL产品HS-IT101注射液,2023年11月29日新药IND申请获NMPA批准(受理号:CXSL2300599),用于晚期实体瘤治疗。
8、LM103(蓝马医疗):苏州蓝马医疗研发的LM103注射液,是国内首个获临床许可的滋养细胞(Feeder)工艺TIL产品,2023年7月13日获NMPA临床试验默示许可,用于晚期实体瘤治疗。
更令人振奋的是,目前我国有多款TIL疗法在招募实体瘤患者,涵盖卵巢癌、胰腺癌、胆管癌、宫颈癌、肺癌、恶性黑色素瘤、肝细胞肝癌、肾癌、头颈鳞癌、食管鳞癌、三阴性乳腺癌、结直肠癌等癌种!想了解详细入排标准或参与临床试验的患者,可咨询医学部,进行初步评估。
小编寄语
TIL疗法是从癌症患者自身的肿瘤病灶中,找到“抗癌突破口”的一款新型T细胞免疫疗法,又被喻为“实体瘤利器”。
由于TILs细胞数量,会随患者的肿瘤进展而逐渐降低;且术后一旦接受辅助性放化疗,则可能会影响体内免疫细胞及正常细胞,因而,建议患者在肿瘤新诊断,且尚未接受放化疗等其他治疗前,储存TIL细胞为宜,一般来说,越早储存越好,以达到预期的抗癌效果。想寻求TIL疗法帮助或了解TIL细胞储存更多讯息的患者,可将近期病理检查结果、治疗经历等,提交至医学部,进行初步评估。
参考资料
[1]Kudling T V,et al.514 Biomarker insights and long-term outcomes of TILT-123 oncolytic adenovirus combined with tumor-infiltrating lymphocytes in refractory metastatic melanoma: results from the TUNINTIL phase 1 trial[J]. 2025.
https://jitc.bmj.com/content/13/Suppl_2/A583?utm_source=researchgate.net&utm_medium=article
[2]Nisimoto M Y S M,et al.Advances in Tumor-Infiltrating Lymphocyte (TIL) as a Prognostic Factor and for Treating Invasive Cutaneous Melanoma[J]. International Journal of Molecular Sciences, 2024, 25(23): 12596.
https://www.mdpi.com/1422-0067/25/23/12596
[3]Yin H,et al.TILs and Anti‐PD1 Therapy: An alternative combination therapy for PDL1 negative metastatic cervical cancer[J]. Journal of Immunology Research, 2020, 2020(1): 8345235.
https://onlinelibrary.wiley.com/doi/10.1155/2020/8345235

































 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城