Xpovio(selinexor)
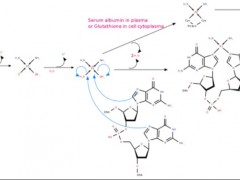
塞利尼索(selinexor)是口服选择性核输出蛋白抑制剂(SINE),通过抑制XPO1的功能,能够让肿瘤抑制蛋白存留在细胞核内继续发挥作用,从而抑制肿瘤细胞的增殖。该药物与地塞米松一起使用,通常用于那些已经接受治疗且不再对至少5种其他骨髓瘤药物有反应的人,包括蛋白酶体抑制剂,免疫调节药物和CD38单克隆抗体。
Xpovio(selinexor)靶向药物介绍
有条件的上市许可得到了2B期STORM阳性研究数据的支持,该研究评估了塞利尼索 (selinexor) 用于严重预处理的三类难治性多发性骨髓瘤成人患者,并于2019年08月发表在新英格兰医学杂志(New England Journal of Medicine)上. 根据 EC有条件批准的规定,对该适应症的继续授权取决于验证性试验中对临床益处的验证。
关于2b 期STORM 关键试验,Karyopharm 在欧洲的有条件授权请求基于美国相同的患者群体,该患者群体是XPOVIO在美国FDA加速批准的患者群体,该群体(n= 83)的总体反应率为25.3 %(95% 置信区间 [CI] ], 16.4, 36)。
NEXPOVIO(Selinexor)塞利尼索 是一款口服选择性核输出抑制剂 (SINE) 。塞利尼索(selinexor)通过选择性结合并抑制核输出蛋白1(XPO1,也称为 CRM1)来发挥作用。NEXPOVIO阻断肿瘤抑制蛋白、生长调节蛋白和抗炎蛋白的核输出,导致这些蛋白在细胞核中积累并增强它们在细胞中的抗癌活性。这些蛋白质的强制核保留可以抑制多种致癌途径,这些不受控制的途径允许具有严重DNA损伤的癌细胞,继续以不受限制的方式生长和分裂。
- 在美国,NEXPOVIO以XPOVIO商品名销售。
1. 添加医学顾问微信,扫描二维码
2. 备注【癌种】申请方舟援助金

患者咨询电话:400-666-7998