苏特替尼临床试验,马来酸苏特替尼胶囊治疗局部晚期或转移性非小细胞肺癌Ⅱa期临床研究
1、试验目的
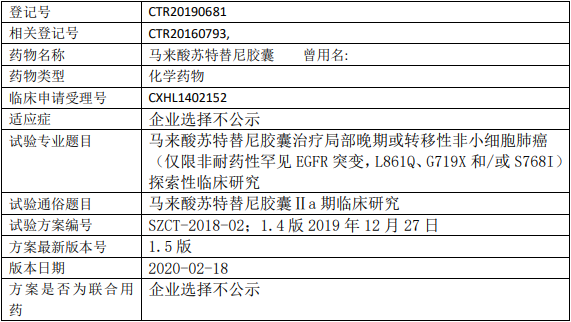
初步探索马来酸苏特替尼胶囊治疗局部晚期或转移性非小细胞肺癌(NSCLC)患者【仅限非耐药性罕见表皮生长因子受体(EGFR)突变,包括 L861Q、G719X 和/或 S768I】的有效性和安全性。
2、试验设计
试验分类:安全性和有效性
试验分期:II 期
设计类型:单臂试验
随机化:非随机化
盲法:开放
试验范围:国内试验
3、受试者信息
年龄:18 岁(最小年龄)至 75 岁(最大年龄)
性别:男+女
健康受试者:无
入选标准
1.年龄 18 ~ 75(含 18、75)周岁,性别不限。2.经病理组织学和/或细胞学确认的局部晚期或转移性 NSCLC 患者。
3.患者的 EGFR 具有 L861Q、G719X、S768I 突变中的一种或几种,且不具有 T790M 突变、19 号外显子缺失突变、20 号外显子插入突变、L858R 突变。
4.ECOG 体力评分为 0、1 或 2 分。
5.预期生存时间>3 个月。
6.根据实体瘤疗效评价标准(RECIST)1.1 版,至少有一个可评估的肿瘤病灶。
7.有足够的血液系统功能、肝功能、肾功能和凝血功能:中性粒细胞绝对计数≥1.5×109/L,血小板计数≥90×109/L,血红蛋白≥90g/L;总胆红素≤1.5×正常值上限(ULN),丙氨酸转氨酶(ALT)≤2.5×ULN,天冬氨酸转氨酶(AST)≤2.5×ULN(肝转移患者总胆红素≤3.0×ULN,ALT≤5.0×ULN,AST≤5.0×ULN); ? 肌酐≤1.0×ULN,或者肌酐清除率≥60mL/min(采用Cockcroft-Gault 方法); 国际标准化比值(INR)≤1.5。
8.有生育能力的合格患者(男性和女性)必须同意在试验期间和末次用药后至少 90 天内使用可靠的避孕方法(激素或屏障法或禁欲);育龄期的女性患者在入选前 7 天内的血人绒毛膜促性腺激素(HCG)妊娠检查必须为阴性;男性患者在首次给药至末次给药后 90 天内不能进行精子捐献。
9.所有患者必须在开始接受任何本试验规定的检查之前对本研究知情,并自愿签署经伦理委员会批准的书面知情同意书(ICF)。
排除标准
1.入组前接受过任何表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)抗肿瘤治疗。
2. 既往接受过化疗、抗血管生成等系统性抗肿瘤治疗患者,需要4周及以上洗脱期;既往接受过抗 PD-1/PD-L1 等免疫治疗,未出现过免疫性肺炎的患者,需要 4 周及以上洗脱期;既往接受过以缓解症状为目的对非靶病灶的放疗、抗肿瘤中成药的患者,需2周及以上洗脱期。
3. 入组前 4 周内接受过主要脏器外科手术(不包括穿刺活检)或出现过显著外伤。
4. 筛选时,既往任何治疗的不良反应(ADR)尚未恢复到不良事件通用术语标准(CTCAE)5.0 等级评价≤1 级(脱发除外)。
5. 无法口服药物,有严重(CTCAE 5.0 等级评价≥3 级)的慢性胃肠功能紊乱,存在吸收障碍综合征或其他任何对胃肠道吸收有影响的状况(例如:消化性溃疡、肠梗阻、肠易激综合征、克罗恩病、胃食管反流病等)。
6. 有免疫缺陷,包括但不限于人类免疫缺陷病毒(HIV)抗体检测(酶联免疫法或 Western 斑点法)阳性,有活动性风湿免疫性疾病。
7. 存在不稳定的具有临床症状的中枢神经系统转移或脑膜转移,或有其他证据表明患者中枢神经系统转移或脑膜转移灶尚未控制,经研究者判断不适合入组;8. 有严重(CTCAE 5.0 等级评价≥3 级)的大疱性或剥脱性皮肤病病史。
9. 筛选时,有未控制的活动性感染【如梅毒、HIV、乙型肝炎病毒(HBsAg 阳性,HBV-DNA>1000cps/ml 且 AST/ALT>2.0xULN)或丙型肝炎病毒(HCV)感染】。
10. 有严重【美国纽约心脏病学会(NYHA)心脏功能分级为Ⅲ级或IV 级】的心血管疾病史,包括但不限于需要临床干预的室性心律失常;入组前 6 个月内有急性冠脉综合征、充血性心力衰竭、脑卒中或其他 III 级及以上心血管事件;筛选时,NYHA 心功能分级≥II 级或左室射血分数(LVEF)<50%。
11. 有其它严重(CTCAE 5.0 等级评价≥3 级)的系统性疾病史,经研究者判断不适合参加临床试验。
12. 入组前 4 周内参与过其它临床试验。
13. 已知有酒精或药物依赖。
14. 精神障碍类疾病患者或研究者认为依从性差者不适合参加研究。
15. 妊娠期或哺乳期女性。
16. 已知对试验药物的活性成分或辅料过敏。
17. 需要长期服用肾上腺类固醇激素治疗(相当于泼尼松龙每日剂量≥20mg,剂量换算表详见附录四)。
18. 既往 5 年内或同时患有其他恶性肿瘤(已治愈的皮肤基底细胞癌和宫颈原位癌除外;乳腺癌根治术后>3 年无复发者除外)。
研究者信息
1、主要研究者信息
| 姓名 | 学位 | 职称 | 单位名称 |
| 周彩存 | 医学博士 | 主任医师 | 上海市肺科医院 |
| 韩宝惠 | 医学博士 | 主任医师 | 上海市胸科医院 |
2、各参加机构信息
| 序号 | 机构名称 | (国家)研究者 | 国家 | 省(州)-城市 |
| 1 | 上海市肺科医院 | 周彩存 | 中国 | 上海市 -上海市 |
| 2 | 上海市肺科医院 | 韩宝惠 | 中国 | 上海市 -上海市 |
| 3 | 蚌埠医学院第一附属医院 | 赵福友 | 中国 | 安徽省 -蚌埠市 |
| 4 | 苏北人民医院 | 汪步海 | 中国 | 江苏省 -扬州市 |



























 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城